Clear Sky Science · zh
基于拓扑中断相位纳米光学的极高灵敏度无标记生物传感平台
看见“不可见”为何重要
许多疾病,包括癌症和神经退行性疾病,会在症状出现之前很久向血液释放出指示性分子。现有的诊断检测往往错过这些早期信号,因为这些分子体积太小或浓度太低,难以可靠检测。本文报道了一种新型光学传感器,能够在不使用荧光标记或化学标签的情况下,探测极其微量的生物分子。通过在仅数个原子尺度上设计材料,作者利用光的微小相位变化,将细微的生化事件放大为易于测量的大信号。
把光变成超灵敏检测器
传统的等离子体生物传感器通过把光照射到薄金属膜上,并观察分子吸附时反射光的变化来工作。这类器件已相当灵敏,但面对非常小的分子或极低的浓度仍然棘手。新平台不再仅跟踪亮度或颜色,而是关注光的相位——波的精确时序。在特殊条件下,反射光几乎消失,其相位会发生极为剧烈的变化。这些点称为光学“暗态”或相位奇点,使系统对金属表面附近的细微变化异常敏感。
构建纳米尺度的光阱
为产生这些奇点,研究团队设计了一个厚度仅数十纳米的分层结构。玻璃基底上支撑着一层12纳米的氧化铝,内含小于3纳米直径的超小银纳米粒子,上面覆盖一层平滑的48纳米金膜。银粒子被精细制备并嵌入,使其保持晶体状、近球形并以亚纳米尺度均匀间隔排列。这种构型使得颗粒的局域等离子体模态能够强烈耦合彼此并与金层中的传播等离子体波耦合。结果形成一种纳米级的光学腔,光能被紧密束缚,其相位对周围介质极为敏感。
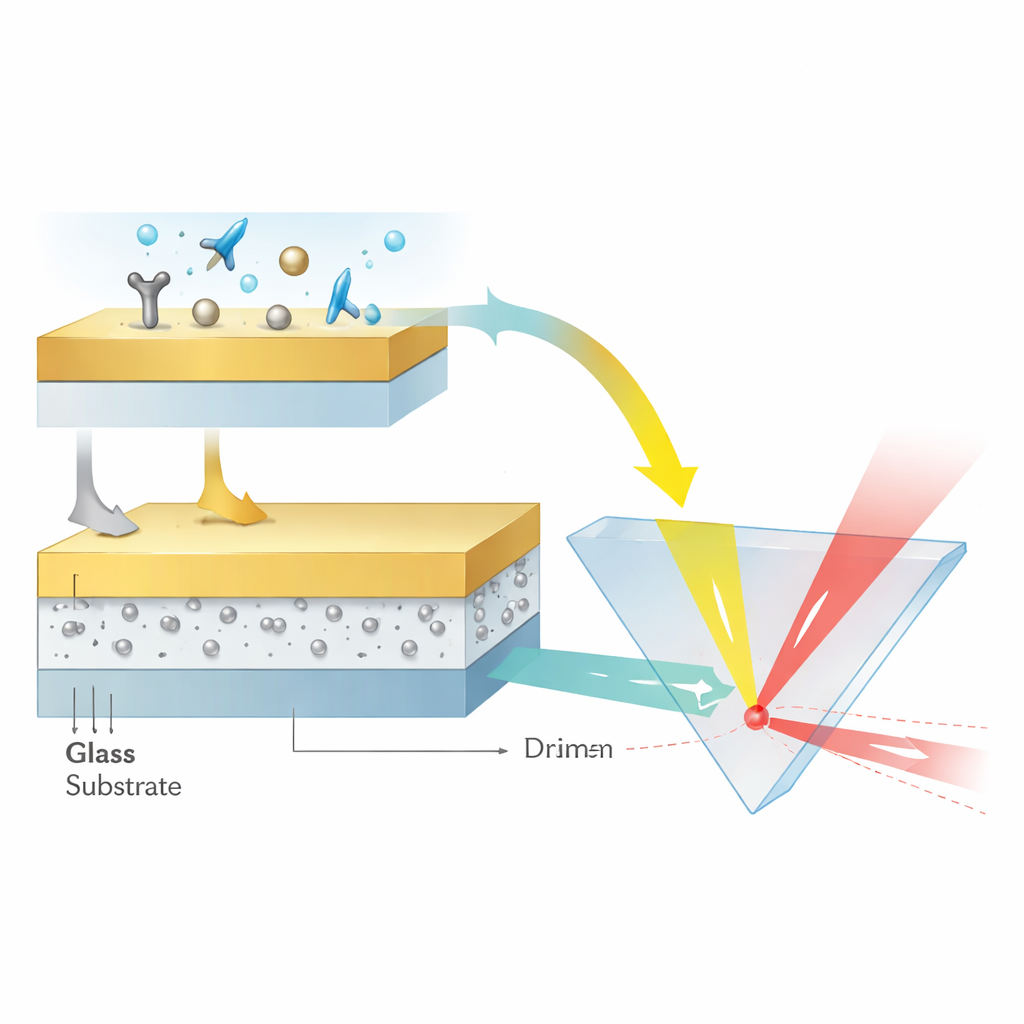
让光侧向滑动
作者并不测量角度或颜色,而是通过跟踪反射光束沿表面侧向位移的距离来读出传感器——这一现象称为Goos–Hänchen位移。当激光束在合适条件下反射时,其能量峰值会稍微偏离简单几何预测的位置。在相位奇点附近,这种位移会急剧放大。通过将银纳米粒子浓度调至约16%,团队将反射率驱近零并使相位跳变变得极为陡峭,以至于由分子在金表面结合引起的微小折射率改变会产生数百微米量级的横向光束位移。在使用稀释甘油溶液的校准测试中,该器件达到相当于每单位折射率变化产生3.27 × 10^8纳米光束位移的灵敏度,并能分辨约千万分之四的微小变化。
在极低浓度下检测极小分子
为展示实际生物传感能力,研究人员首先以生物素为靶标——这是一种分子量很小的维生素。标准表面等离子体传感器即便在微摩尔水平也难以可靠检测生物素。在本工作中,通过在金表面修饰亲和结合生物素的链霉亲和素,新的平台能够清晰地实时追踪到低至1飞摩尔的结合事件——大约相当于在10^15个溶剂分子中只有一个目标分子。信号随浓度每十倍增加而稳步上升,证实光束位移与此类微量分析物的覆盖程度呈可预测标度关系。
在阿托世界中追寻癌症标志物
团队随后转向临床相关的靶标:肿瘤坏死因子α(TNF-α),这是一种与炎症和癌症相关的细胞因子,在患者血清中的浓度约为10^−13摩尔。他们用可特异捕获TNF-α的短DNA链(适配体)功能化金表面,并对剩余区域进行阻断以抑制非特异性结合。在这些条件下,传感器在低至0.1阿托摩尔(10^−19摩尔)的浓度下记录到了清晰、稳定的信号,并在10^−13摩尔时产生了近47微米的位移,落在临床相关范围内。与另一种细胞因子白细胞介素-6的对照测试几乎没有持久信号,证实了响应既高度灵敏又具有选择性。
这对未来医学检测意味着什么
简而言之,这项工作表明,将精心排列的银纳米粒子隐藏在一层薄金之下,可以把表面几乎不可察觉的变化转化为易于测量的大幅侧向光位移。通过在相位奇点处工作,该平台无需荧光标记即可将灵敏度推进到针对真实生物靶标的泽托(zepto)到阿托(atto)摩尔级别。如果能将其转化为稳健且易于使用的设备,这类传感器可能使血液检测在现有方法之前很久就能发现疾病标志物,为早期诊断和实时健康监测打开新窗口。
引用: Du, F., Gireau, M., Youssef, J. et al. Extreme sensitivity label-free biosensing platform based on topologically disruptive phase nano-optics. Microsyst Nanoeng 12, 106 (2026). https://doi.org/10.1038/s41378-026-01222-3
关键词: 无标记生物传感, 等离子体传感器, 纳米粒子, 早期疾病检测, 癌症生物标志物