Clear Sky Science · zh
PEG化掺铜WS2杂化纳米片用于靶向多模态癌症治疗
为什么更智能的癌症治疗很重要
许多乳腺癌患者仍然面临可能损伤健康组织且无法完全阻止肿瘤的严酷治疗。本研究描述了一种新型微小工程化薄片,肉眼无法看见,设计用于在体内运输、识别乳腺肿瘤并通过多种协调方式同时攻击肿瘤。通过将热、化学作用和一种经典化疗药物整合到单一的靶向载体中,研究者旨在使治疗更强效,同时对机体其他部位更温和。 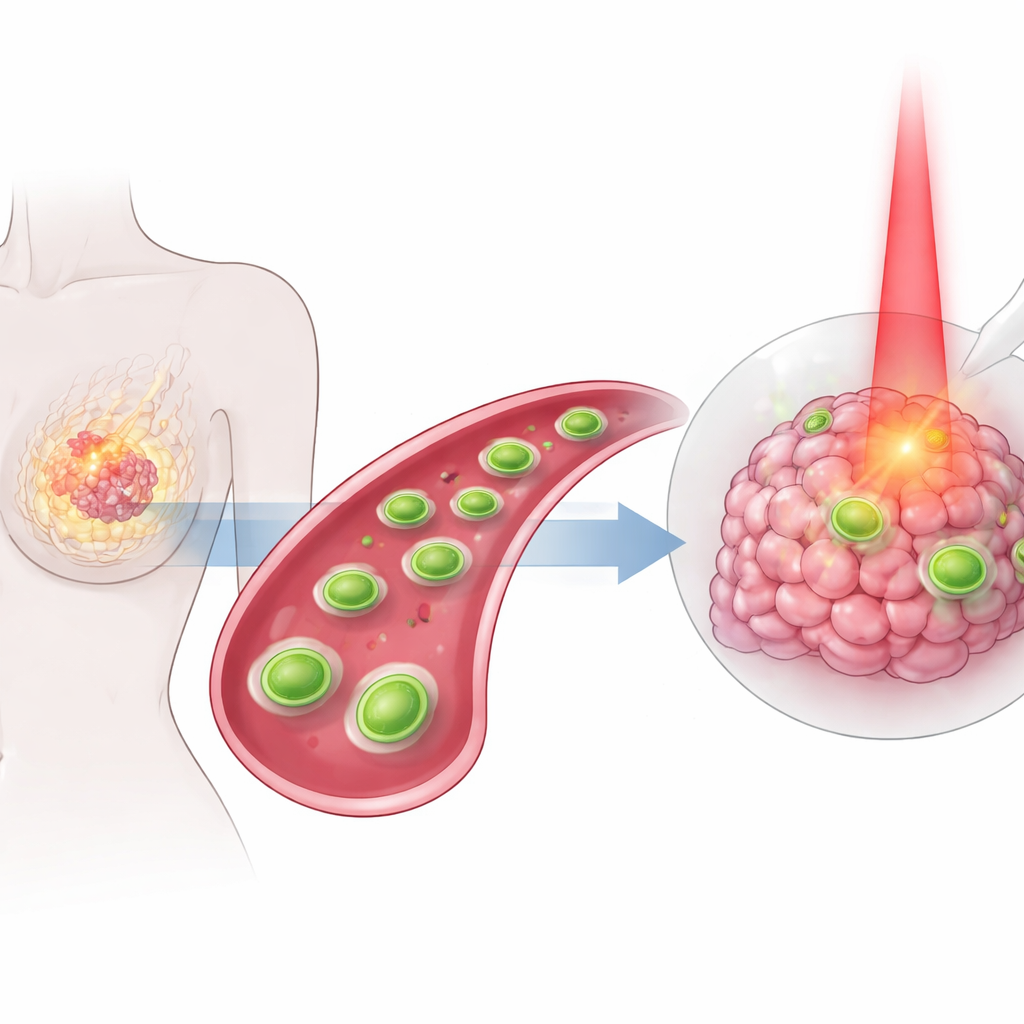
为承载和释放疗法而制造的微型薄片
该方法的核心是一种由钨和硫构成的超薄材料,呈纳米级薄片状。这些薄片天然吸收近红外光并将其转化为热能。研究团队首先制备这些薄片,然后精细粗糙化其表面以便容纳其他有用成分。铜原子以高度分散的方式锚定在薄片上,并添加了一层柔软、灵活的涂层,类似分子级的“雨衣”,以帮助颗粒在体液中良好分散并避免聚集。最后,他们连接了叶酸——许多肿瘤细胞积极摄取的一种维生素,作为定位装置,并在表面负载了常用化疗药物多柔比星。最终得到的是一个微小的多层平台,能够在血液中循环、识别肿瘤细胞并携带大量治疗负载。
光、化学与药物如何协同作用
一旦这些颗粒到达肿瘤部位,会发生多重协同反应。当肿瘤区域被温和的红色激光照射时,钨-硫薄片高效升温,将局部温度提高到足以使癌细胞承受应激并受损而又不会使全身过热。同时,薄片上的铜原子与肿瘤内本就较高水平存在的过氧化物分子发生反应,将过氧化物转化为极具攻击性的短寿命氧化剂,从内部打击细胞组分。肿瘤通常也比健康组织更酸性;在这种酸性环境下,且在激光加热的共同作用下,薄片与多柔比星之间的键变弱,使更多药物在需要之处释放出来。这三种效应——热、化学攻击与聚焦化疗——彼此增强,协同发挥作用。 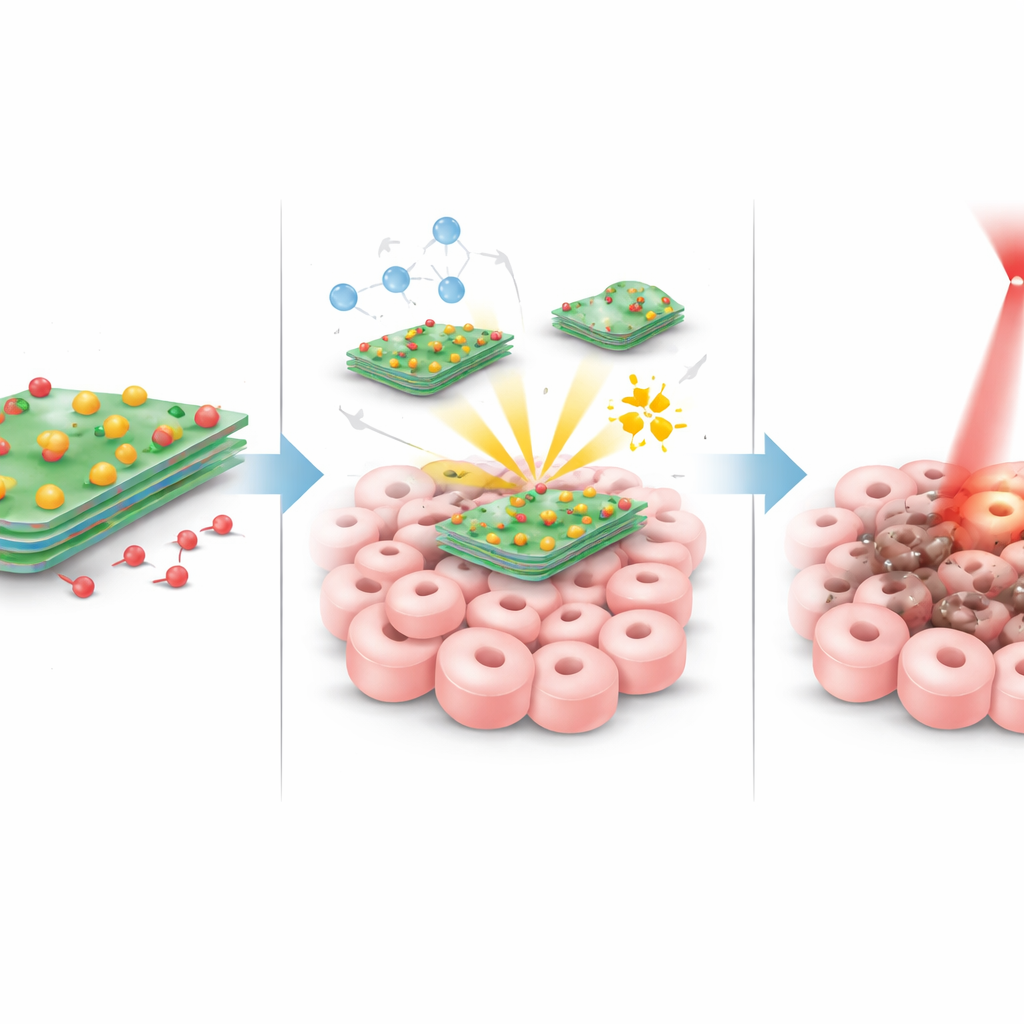
来自细胞与携瘤小鼠的证据
在体外培养中,带涂层的薄片单独对正常细胞几乎没有损害,提示其具有良好的基本安全性。但当负载多柔比星并在过氧化物存在下接受激光照射时,它们对乳腺癌细胞造成了强烈的细胞死亡,远超任何单一疗法。研究人员还证明这些颗粒在肿瘤细胞内产生了大量反应性氧化物,证实了铜催化化学的活性。在携带乳腺肿瘤的小鼠中,带叶酸涂层的颗粒在肿瘤组织中的积累明显更强且持续时间更长,优于非靶向颗粒。当小鼠接受完整组合治疗——靶向颗粒加红光照射——肿瘤显著缩小,存活时间延长,体重及器官健康基本保持正常,表明与常规药物治疗相比副作用有限。
这对未来癌症治疗的可能意义
总体来看,这些工程化薄片表现得像一种多功能工具:它们寻找肿瘤、加热肿瘤、通过反应化学从内部“毒害”肿瘤,并更精确地递送经验证的药物,同时尽量保护身体其他部位。该工作仍处于动物研究阶段,关于长期安全性、降解行为以及如何将此类颗粒规模化制造以用于人体仍有重要问题。但这一设计展示了如何将若干适度疗法整合到单一智能载体中,利用肿瘤自身环境来产生更强的整体疗效。如果后续研究证实其安全性和有效性,此类多功能纳米平台有望使乳腺癌治疗更具靶向性、更高效、对患者造成的折磨更小。
引用: Li, D., Wen, C., Wu, H. et al. PEGylated Cu-doped WS2 hybrid nanosheets for targeted multimodal cancer therapy. Microsyst Nanoeng 12, 121 (2026). https://doi.org/10.1038/s41378-026-01218-z
关键词: 乳腺癌治疗, 纳米医学, 光热治疗, 靶向药物递送, 化学动力学治疗