Clear Sky Science · zh
基于微吸管电阻建模的机器人细胞转运系统
无需显微镜即可搬动微小细胞
现代生物学常常依赖一项看似简单的任务:用玻璃管夹起单个细胞并把它放到别处。这对辅助生殖、胚胎冷冻、基于细胞的疗法以及基础研究至关重要。然而目前几乎总是需要体积庞大的显微镜和受过高度训练的人员全程监视。本文介绍了一种新的机器人系统,能够在完全没有显微观察的情况下,将单个细胞在液滴之间搬运,从而为完全封闭的自动化“细胞工厂”打开可能,这类系统运行更快、成本更低,而且对脆弱细胞的损伤更小。
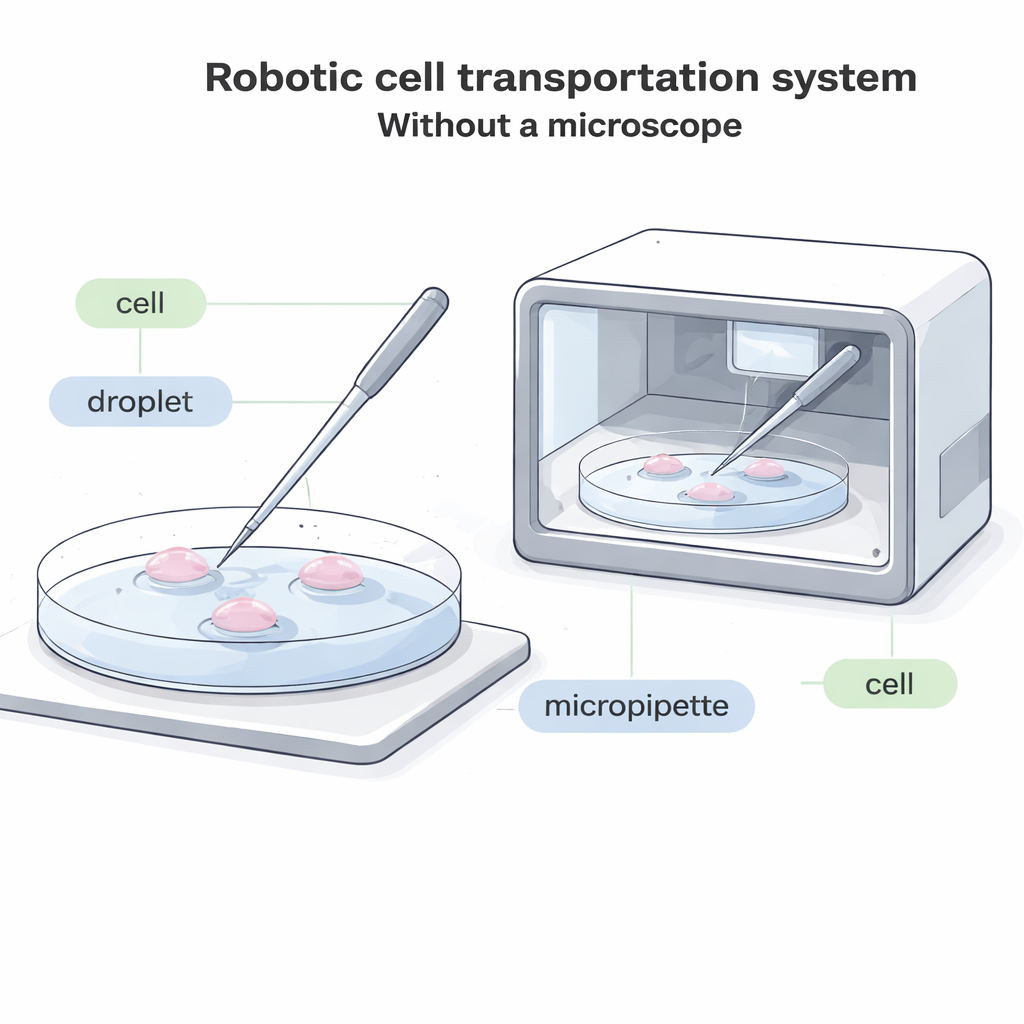
为什么细胞搬运需要改头换面
在现有实验室里,操作者通过显微镜观察,使用一根细长玻璃管(称为微吸管)贴近培养皿底部,轻轻吸入一枚细胞,将其移动到新的液滴中,然后再推出来。这个过程速度慢、视觉负担大且难以实现自动化。在许多未来系统中——例如在封闭盒内培养胚胎或其他细胞的紧凑设备——根本没有足够空间放置传统显微镜。在其他情况下,细胞被染以易褪色或受光损伤的荧光染料,因此应尽量减少强光显微观察。现有那些不依赖图像的“盲”系统仅适用于异常大的细胞,大多数常见细胞类型仍缺乏良好的自动化解决方案。
带内径缩颈的特殊“吸管”
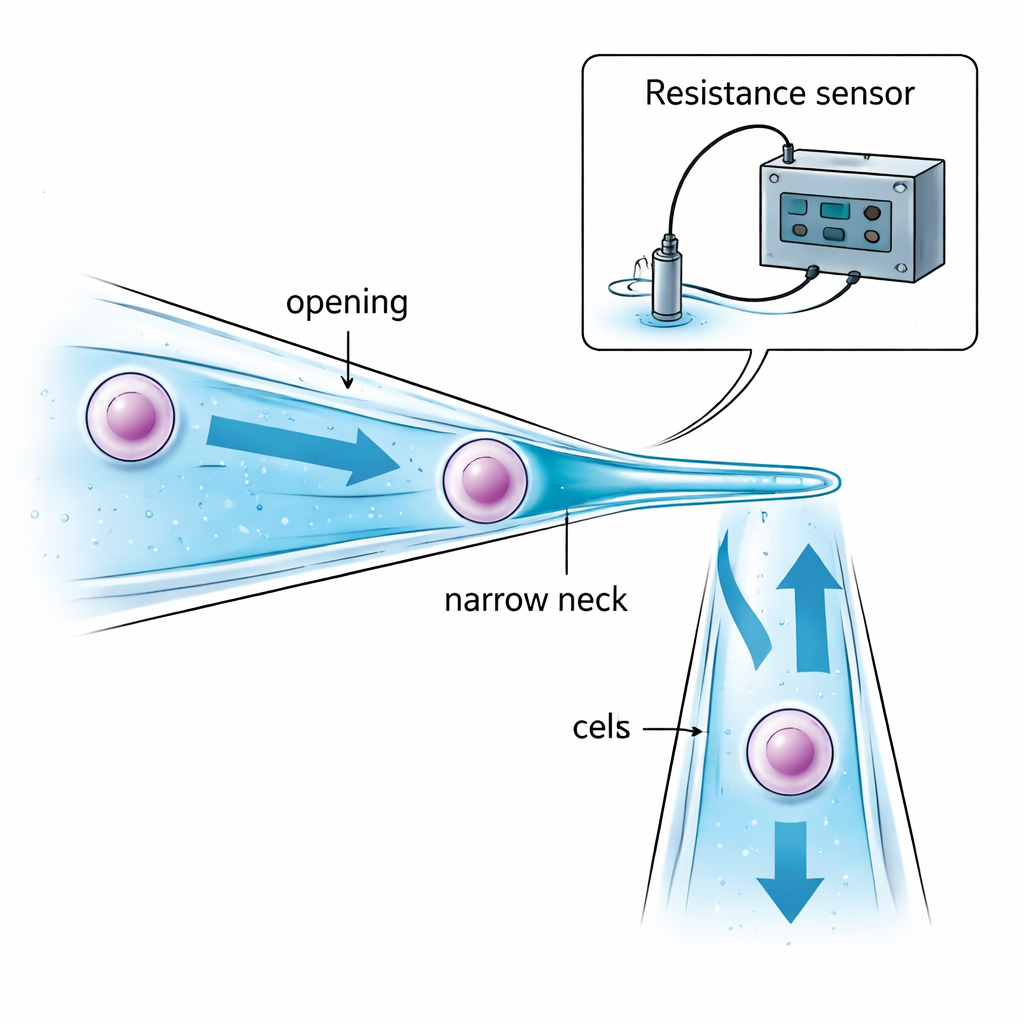
作者通过重新设计微吸管本身来解决这一问题。他们不再使用直径恒定的玻璃管,而是制造出带有狭窄颈部的微吸管。其开口略大于目标细胞,以便将细胞吸入;在更深处,管腔逐渐变窄形成一个比细胞更小的“颈”。当吸力将细胞拉向该收缩处时,细胞会在管内被卡住并固定——而不是悬挂在尖端并在液滴之间暴露于油或空气中。通过谨慎选择开口尺寸、颈部尺寸及两者之间的距离,可以在不对细胞施加过度挤压的前提下可靠捕获细胞,同时仅携带极少量液体从一个液滴到另一个液滴,从而减少污染。
不看而“听”电信号
没有显微镜,机器人仍需知道三件事:玻璃尖端何时足够接近皿底、何时细胞已在颈部处被成功捕获、以及何时已完全释放到新液滴中。研究团队通过监测微吸管内外液体中极小的电阻变化来解决这一点。当斜置的吸管接近皿底时,两者之间的液体间隙缩小,电阻以可预测的方式上升,表明即将在接触前安全着陆。当细胞堵住狭窄的颈部时,通过液体的电流路径受限,电阻会突然跳升;当细胞被推送出来时,电阻则同样明显下降。对这些“间隙”、“吸取”和“注入”电阻的数学建模使得计算机能够实时解释这些信号并决定何时停止抽吸或加压,全部无需视觉反馈。
将机器人付诸实测
为验证该方法的可行性,研究者构建了集运动控制、压力控制、电阻感测和主控计算机于一体的完整机器人系统。他们对小型癌细胞(称为HeLa细胞,直径约10微米)和更大的猪卵细胞(约150微米)进行了测试。系统能够在广泛的吸管尺寸范围内,仅凭电阻信号可靠检测到着陆、捕获和释放。在直接比较中,机器人搬运HeLa细胞的成功率为90%——优于此前基于视觉的自动方法;对猪卵细胞的运输成功率为95%,高于标准显微镜方法。每个细胞的操作时间与人工控制方法相当或更短,主要因为狭窄颈部减少了为将细胞定位而反复微调吸力的需要。
保持细胞存活并实现规模化
任何进入生物实验室的机器人辅助设备都必须避免损害其处理的细胞。经该新系统运输后,对HeLa细胞和猪卵细胞在培养一天后用只在活细胞中显色的染料染色,结果显示新方法的存活率与传统显微镜引导的转移以及未处理的对照细胞相当或接近,表明在正确设置阈值时,颈部的温和机械挤压不会明显降低细胞活力。展望未来,作者建议同样基于电阻的感测和压力控制可以集成到紧凑的微流控芯片中,从而允许许多通道并行运行,实现高通量、完全封闭的细胞处理系统,适用于自动化辅助生殖、细胞疗法以及显微镜难以进入的长期细胞培养设备。
这对未来细胞工作意味着什么
对非专业读者而言,主要信息是:搬运单个细胞不再必须依赖人通过显微镜盯着看。通过精心塑形的玻璃管并“倾听”周围液体中电流的流动,机器人可以感知何时着陆、何时抓住细胞以及何时放开——全部在黑暗和狭小空间中进行。这使得设计封闭、自运行的细胞培养系统更加可行,这类系统能保护脆弱样本、简化临床流程,并把实验室级别的细胞操作带向更自动化、工厂化的运作模式。
引用: Zhao, Q., Liu, M., Zhu, R. et al. Robotic cell transportation system based on micropipette resistance modeling. Microsyst Nanoeng 12, 65 (2026). https://doi.org/10.1038/s41378-026-01193-5
关键词: 细胞操作, 微吸管, 机器人技术, 微流控, 自动化