Clear Sky Science · zh
基于单管CRISPR的现场检测平台,可在无预扩增下快速、特异且高灵敏地检测HPV16
为何识别单一病毒亚型至关重要
宫颈癌常与人乳头瘤病毒(HPV)感染相关,但并非所有HPV亚型具有相同风险。因此,医生需要能够可靠区分这些高度相似病毒的检测方法,尤其是被认为高危的HPV16。问题在于,当今的基因检测有时会将近亲亚型混淆,导致误报或漏诊。该研究提出了一种新的检测方法,显著提升了准确性和可操作性,旨在将精确的HPV亚型判别带入临床和现场检测环境。
一种智能的分子“锁与钥匙”
研究人员构建了一种称为CASTSA的单管检测方法,将两种强大理念结合起来:源自细菌的基因靶向系统CRISPR的高特异性,以及用于复制DNA的标准方法PCR的信号放大能力。在CASTSA中,名为Cas12a的CRISPR蛋白由一段短RNA“钥匙”引导以识别HPV16的基因序列。当它找到精确匹配并且附近存在其所需的短序列模式(PAM)时,Cas12a会在可预测的位置切割病毒DNA。该切割在一条DNA链上产生一个独特的末端,作为特异性的扩增起点。即使其他HPV亚型序列非常相似,它们要么不会被切割,要么不会产生正确的起始末端,因此不会被放大。
把微小切口转化为强烈信号
为将CRISPR切割转化为可检测信号,团队设计了一种特殊的DNA引物,称为端点特异性引物。该引物仅能正确地与Cas12a切割产生的那条链配对,然后像发卡一样折回自我配对,帮助构建一个稳定的PCR模板。接着,额外的“通用”引物序列结合并驱动常规的实时PCR反应。关键在于,只有当Cas12a先完成切割且引物正确折叠时才会发生扩增,从而形成两重校验。这种设计大幅降低了部分匹配的非靶DNA被误扩增的风险,解决了早期依赖预扩增步骤的CRISPR检测方法常见的弱点。
同管完成,减少误差
一项重要的实用进展是将CRISPR切割和PCR扩增在同一密闭试管中同时进行,避免了步骤间打开试管——这在许多实验流程中是导致污染的主要来源。作者精心调校了反应条件,特别是镁离子浓度,使Cas12a和DNA复制酶在不促成非特异反应的情况下均能良好工作。他们证明,这种单管体系能够在几种其他高危型(包括HPV18、33、45和52)之间可靠地区分HPV16,尽管这些病毒在一些基因区域高度保守。与单独的实时PCR或先扩增再进行CRISPR检测的方法相比,CASTSA对非靶HPV亚型产生的误导性信号要少得多。
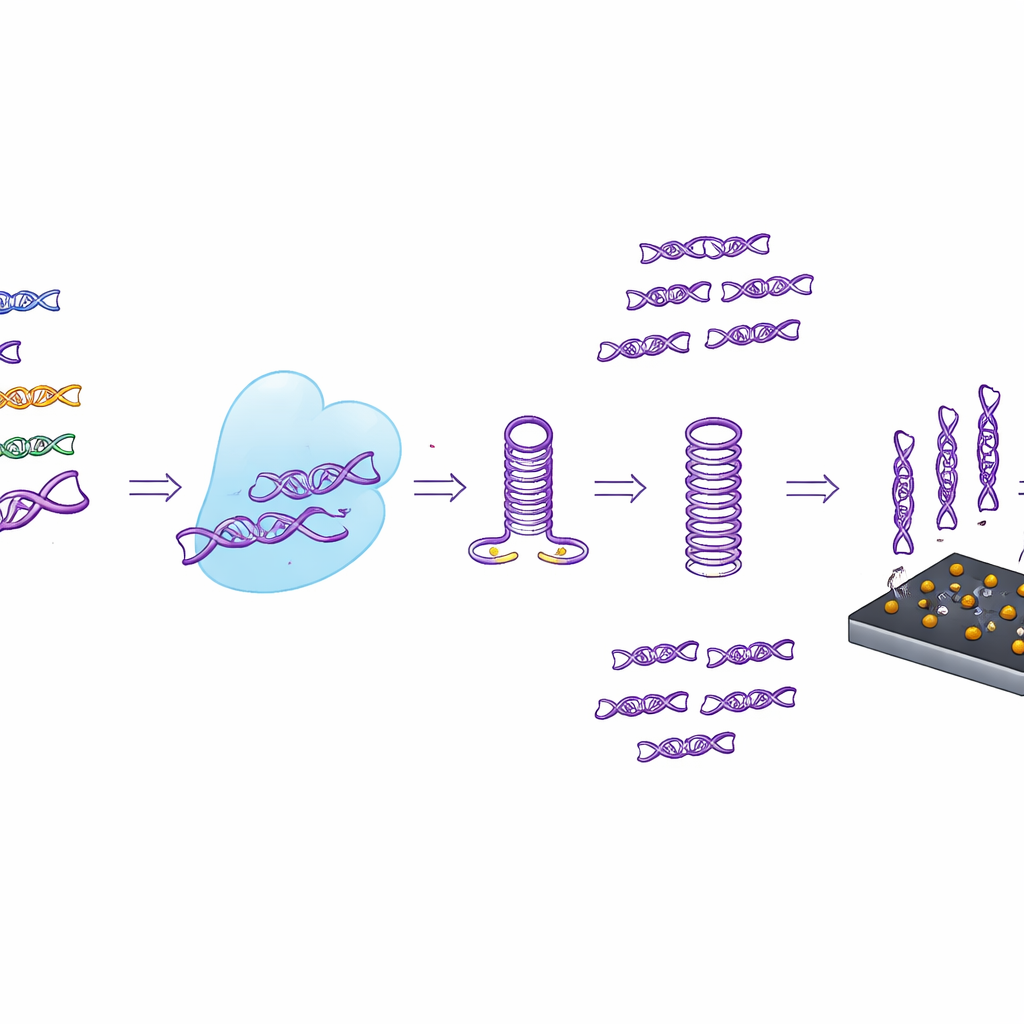
从试管到手持传感器
研究人员不仅依赖荧光读数,还将CASTSA与一种由激光诱导石墨烯制成的紧凑电化学传感器相结合。这种多孔且高导电的碳表面装饰有携带捕获链的金纳米颗粒,这些捕获链仅设计用于结合来自HPV16的CASTSA扩增产物。当这些产物结合时,通过传感器的电流发生可测量的变化。通过使用四电极阵列——三个检测点和一个内置背景控制——该设备可以从非特异性吸附中扣除噪声。在试验中,该集成系统能够检测到每反应最低18份HPV16目标拷贝,灵敏度优于单纯荧光读数,并保持良好的重复性。
这将如何改变HPV检测
为评估该方法在真实样本中的表现,团队检测了20份已知含HPV16的临床样本和10份健康供者样本。无论是荧光形式的CASTSA,还是与石墨烯传感器配套使用,结果均与医院标准PCR检测完全一致。同时,CASTSA在忽略常引起混淆的其他高危HPV型方面表现更佳。对于患者而言,这可能意味着更少的可疑结果和更明确的后续诊疗决策。更广泛地讲,CASTSA策略——先CRISPR识别、再扩增、且在同一密闭试管中完成——为高度特异、低污染的基因检测提供了蓝图,可适配于多种病原体和突变的检测,尤其适合需要快速可靠答案的场景。
引用: Chen, Y., Chen, Y., Zhang, C. et al. One-pot CRISPR-based point of care platform for rapid, specific and sensitive detection of HPV 16 without pre-amplification. Microsyst Nanoeng 12, 81 (2026). https://doi.org/10.1038/s41378-025-01130-y
关键词: HPV16 检测, CRISPR 诊断, PCR 检测, 电化学生物传感器, 即时检测(现场)检测