Clear Sky Science · zh
在侵袭性B细胞淋巴瘤中,MCL-1抑制与CAR-T疗法的合成致死性
这对癌症治疗的重要性
侵袭性B细胞淋巴瘤是增殖迅速的血液癌,常在治疗后复发。即便像CAR-T细胞疗法这样强大的新方法——通过重新编程患者自身免疫细胞以攻击癌症——随着时间推移也约有一半患者出现失败。本研究探索了一种将这一弱点转化为优势的方法:使用一种针对淋巴瘤细胞关键存活蛋白的药物,既直接杀伤肿瘤,又使残存细胞更易被CAR-T细胞彻底清除。
难缠的淋巴瘤细胞问题
侵袭性B细胞淋巴瘤常由MYC基因过度活化驱动,MYC促进细胞快速分裂并帮助肿瘤细胞躲避免疫监视。标准治疗甚至CAR-T疗法都可能留下少量耐药或耐受的淋巴瘤细胞,这些细胞后来会引发复发。这些“持续存活”或耐药细胞通常位于充斥抑制性免疫细胞的肿瘤环境中,使效应性T细胞难以发挥作用。作者提出阻断MCL-1——淋巴瘤细胞依赖以避免自我凋亡的蛋白——是否能暴露该系统的潜在弱点。
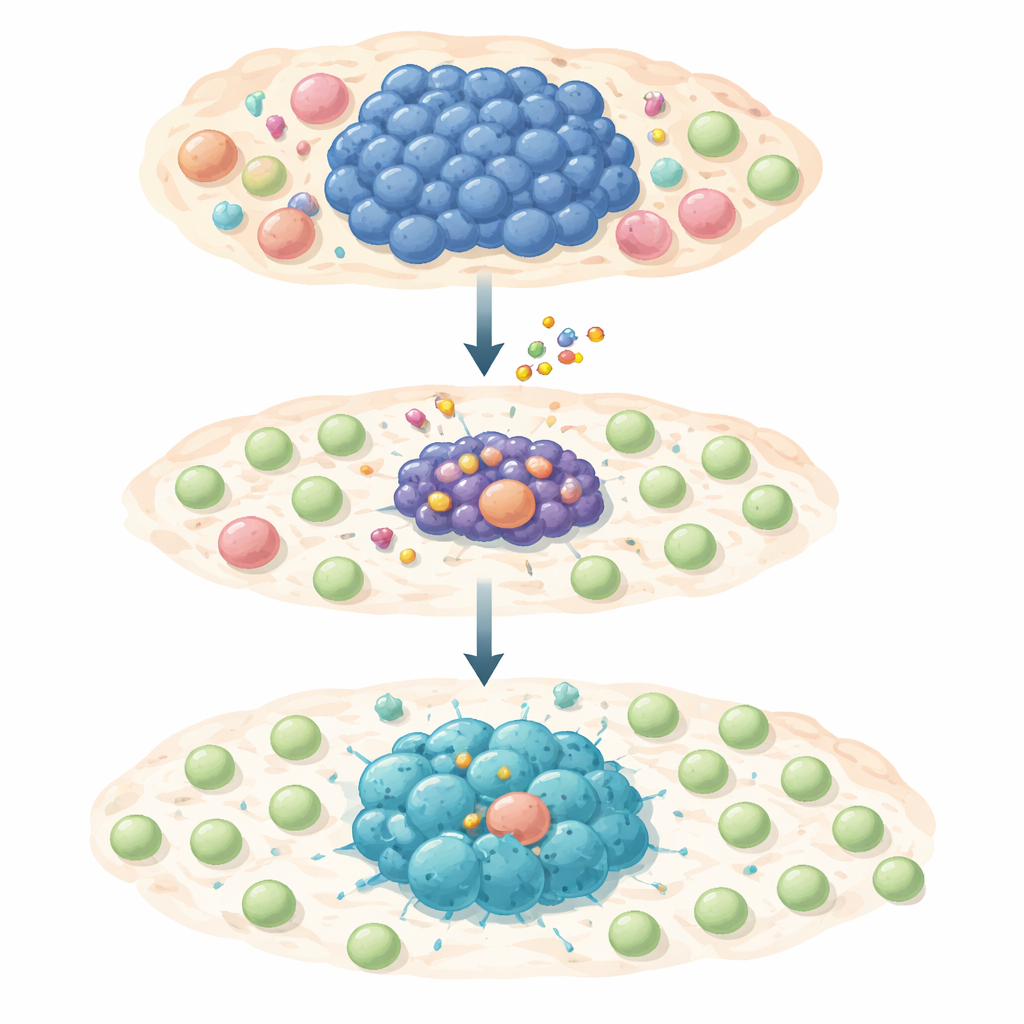
对肿瘤存活与伪装的两步打击
研究团队在大量依赖MYC的人类淋巴瘤细胞系中测试了一种选择性MCL-1抑制剂S63845。大多数癌细胞对该药物高度敏感,MCL-1被抑制时发生程序性细胞死亡。然而,有一小部分细胞在短期或长期暴露后存活下来,表现为药物耐受或完全耐药。对这些幸存细胞的深入分析显示,MYC活性被抑制,而另一种分子STAT1及其相关的干扰素警报通路被激活。这一转换上调了驱动炎性信号和趋化因子的基因——这些分子相当于能招募T细胞进入肿瘤区域的“信号弹”。
重唤醒免疫邻里
为了观察这一过程在体内的表现,作者用低剂量MCL-1抑制剂处理携带MYC驱动淋巴瘤的小鼠。该药物在减少肿瘤负担的同时保留了正常B细胞,但其影响不仅仅是简单缩瘤。被处理的肿瘤显示出更多的CD4和CD8 T细胞、更少的耗竭T细胞、更少的调节性T细胞以及更少的抑制性髓系细胞,均为免疫更友好的环境标志。对肿瘤及周围细胞进行单细胞RNA测序证实,残存的淋巴瘤细胞MYC降低、STAT1增加、干扰素和炎症信号增强,而周围组织则被活跃的T细胞和自然杀伤细胞重新占据,而非抑制性细胞。
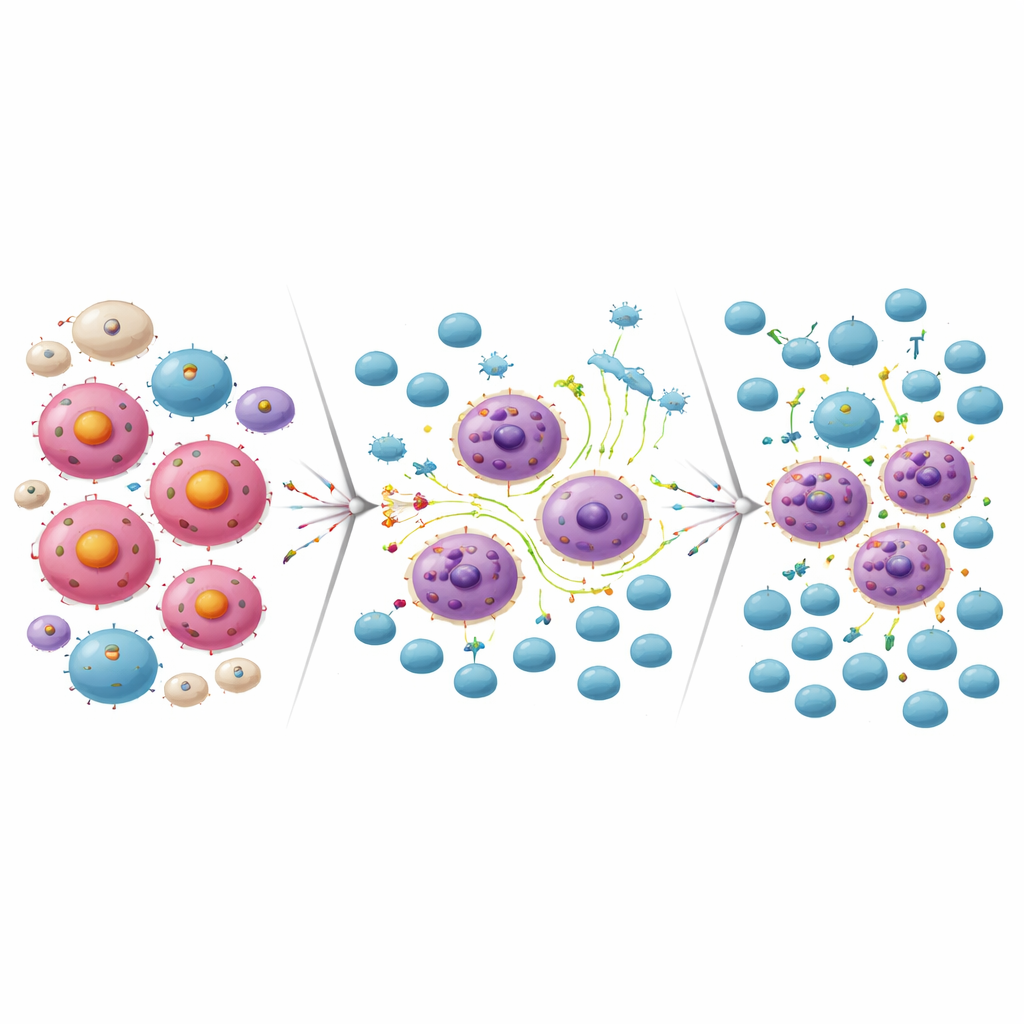
将耐药转为CAR-T细胞的突破口
同样的炎性重编程不仅帮助部分淋巴瘤细胞在MCL-1抑制下存活,也使它们更易受免疫攻击。在体外实验中,针对CD19的CAR-T细胞能够有效清除那些对MCL-1药物产生耐药性的淋巴瘤细胞。相反,对CD19 CAR-T疗法产生耐药的淋巴瘤细胞对MCL-1抑制剂表现出高度敏感性。当研究者在细胞培养中将亚致死剂量的MCL-1抑制剂与CAR-T细胞联合使用时,两种治疗共同消灭的淋巴瘤细胞远多于任一单独治疗。在小鼠模型中,先给予MCL-1抑制剂随后输注CD19 CAR-T细胞,较单一治疗带来了近乎完全的肿瘤清除并显著延长生存期。
具有治愈潜力的一击制胜
简言之,该研究提出了一种“先发后击”的策略。首先,MCL-1抑制剂击倒大部分淋巴瘤并迫使残存癌细胞进入一种被炎症化、易被识别的状态,从而吸引T细胞并剥夺其保护屏障。其次,CD19 CAR-T细胞利用这一新暴露的弱点清除剩余疾病。通过同时打击肿瘤的内部存活线路和其保护性的微环境,这种联合方法有望减少复发,使侵袭性B细胞淋巴瘤更接近长期缓解。
引用: Gao, J., Zhao, X., Yin, Q. et al. Synthetic lethality of MCL-1 inhibition and CAR-T therapy in aggressive B-cell lymphoma. Leukemia 40, 638–648 (2026). https://doi.org/10.1038/s41375-026-02884-8
关键词: B细胞淋巴瘤, CAR-T疗法, MCL-1抑制, 肿瘤微环境, 药物耐受性