Clear Sky Science · zh
通过MYC抑制miR-29导致转化性滤泡性淋巴瘤中CD40信号增强
当细胞间对话变得危险
滤泡性淋巴瘤是一种生长缓慢的血液癌症,可能潜伏多年,但在部分患者中会突然加速,转变为快速且危及生命的疾病。本研究提出了一个简单但关键的问题:在这些癌细胞以及它们的细胞邻里中,哪些改变会触发这种开关?通过在转化过程跟踪癌细胞的基因和微小RNA调节因子,研究者们发现了一个隐藏的调控回路,它调整了肿瘤细胞对来自邻近免疫细胞帮助的响应强度——并显示当此回路失灵时,癌症更难以治疗。
一种有时会加速的沉寂型癌症
滤泡性淋巴瘤起源于B细胞,即通常产生抗体的免疫细胞。大多数患者患有惰性或生长缓慢的疾病,但每年有一部分病例转化为表现更类似弥漫性大B细胞淋巴瘤的侵袭性淋巴瘤。尽管遗传突变被关联到这种变化,但它们并不能完全说明问题。肿瘤细胞生存在一个丰富的微环境中,充满了辅助性T细胞和其他免疫伙伴,持续进行信号交换。作者推测,被称为微小RNA的小型调节分子可能是癌细胞如何适应这一变动邻域并跃迁到更危险状态的关键,它们精细调控基因的使用。
小RNA的刹车消失
为检验这一想法,团队在配对样本中首次对信使RNA和微小RNA同时进行了匹配表达谱分析,这些配对样本来自同一患者在转化前后的取材。比较11例滤泡性淋巴瘤样本与其11例转化样本,他们发现有超过一千个基因和19种微小RNA发生了变化。其中一个家族尤为突出:miR-29家族的三位成员在转化肿瘤中均持续降低。早期在其他血液癌症中的研究表明,miR-29曾作为细胞生长和存活的刹车。在这里,其丧失成为转化的一个特征,暗示下调该微小RNA家族可能解除淋巴瘤细胞中促进生长的通路的抑制。
来自辅助细胞的增强信号
深入基因表达数据,研究者们发现转化肿瘤中CD40通路的活性显著上升,CD40是一条在辅助T细胞与B细胞接触时被触发的信号通路。在健康的淋巴结以及惰性滤泡性淋巴瘤中,这种相互作用以受控方式帮助B细胞生长和存活。令人惊讶的是,在转化样本中,大约90%的病例显示与CD40相关的基因被激活,尽管肿瘤区域中T细胞的总体数量实际上更低。单细胞分析证实,仍有一部分T细胞提供了激活CD40的信号,但淋巴瘤细胞本身似乎对该信号变得更加敏感。
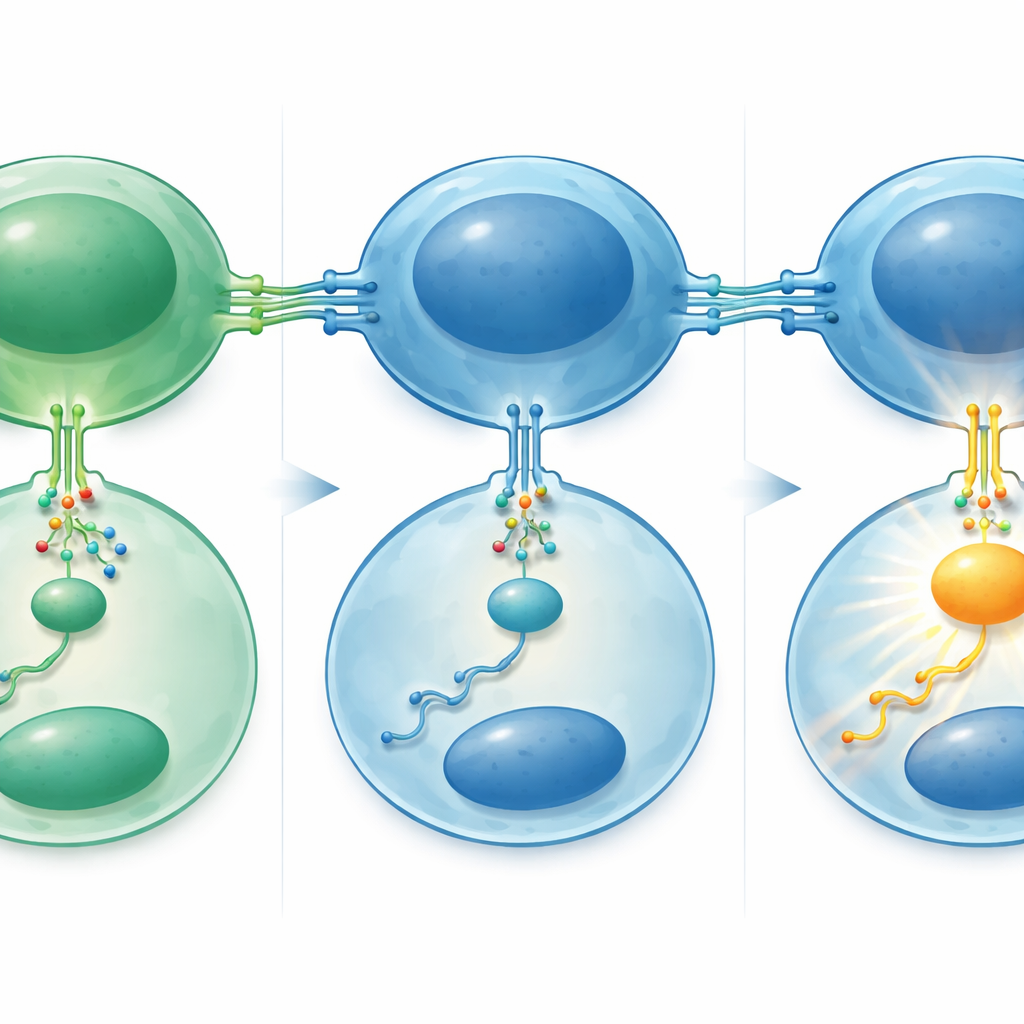
一个放大生长的三步回路
作者随后拼合出导致这种敏感性增强的分子回路。实验室实验表明,miR-29通常在B细胞内抑制一种名为TRAF4的蛋白水平;TRAF4是一个内部适配子,有助于将CD40信号向细胞内部传递。当在淋巴瘤细胞系中人为提高miR-29水平时,TRAF4下降,细胞对CD40刺激的响应减弱,下游信号激活较弱且增殖减慢。在患者样本中则出现相反模式:转化肿瘤和较高级别的滤泡性淋巴瘤中TRAF4更多、细胞分裂率更高。另一个重要角色是众所周知的促癌蛋白MYC,它位于上游。转化过程中MYC的水平和活性上升,并被证明直接结合控制miR-29的DNA区域,作为一个开关将该微小RNA家族下调。
对患者意味着什么
将这些片段拼接在一起,本研究勾勒出一条三步链:MYC活化抑制miR-29,miR-29的丢失解除对TRAF4的抑制,而额外的TRAF4使淋巴瘤细胞对来自少数残存辅助T细胞的CD40信号高度敏感。这种放大的“帮助”推动更强的生长和存活,促进了转化。在临床上,肿瘤miR-29水平较低的患者——尤其是miR-29c成员——往往生存期更短并更快复发,这一发现已在独立的治疗试验中得到确认。由于miR-29即使在久保存的活检样本中也可可靠测量,且模拟miR-29或阻断CD40信号的药物已在探索中,这项工作指向了识别高风险滤泡性淋巴瘤患者与设计切断肿瘤细胞与其免疫邻居危险对话的治疗新途径。
引用: Filip, D., Litzmanova, K., Michaelou, A. et al. Repression of miR-29 via MYC leads to increased CD40 signaling in transformed follicular lymphoma. Leukemia 40, 759–772 (2026). https://doi.org/10.1038/s41375-026-02868-8
关键词: 滤泡性淋巴瘤, 微小RNA, CD40信号, MYC, 肿瘤微环境