Clear Sky Science · zh
CSF1R 标记一部分具有急性髓性白血病扩增特性的胎儿造血多能前体细胞
这项研究为何对患白血病的婴儿重要
婴儿期的白血病虽罕见但常常具有毁灭性,许多婴儿对现有治疗反应不佳。本研究提出了一个看似简单却意义重大的问题:胚胎早期哪些造血细胞最先出问题,引发一种特别侵袭性的婴儿白血病?我们能否为这些细胞找到明确的靶点以开发针对性治疗?
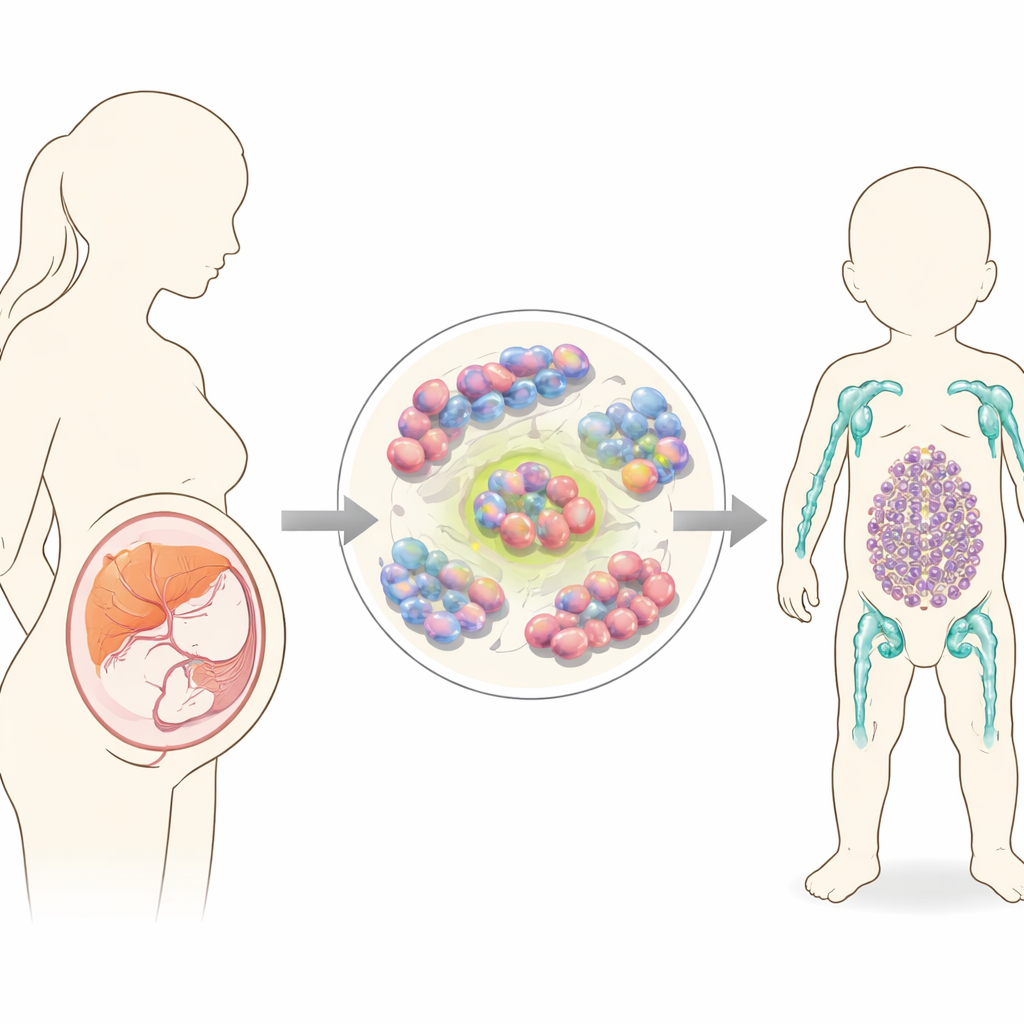
问题在出生前就已萌发
临床医生长期怀疑许多婴儿白血病起始于子宫内。线索来自新生儿血斑样本以及在双胞胎中发现相同致癌突变的病例。发育早期,造血在多个器官间迁移——包括卵黄囊和靠近主动脉的区域,随后定居于胎肝,后来转移到骨髓。在每个部位,不同类型的不成熟造血细胞先出现后消失。婴儿白血病中一个常见的基因事件是 KMT2A 与如 MLLT3 等伙伴的断裂重连,这种重排可驱动淋巴系白血病(类似儿童急性淋巴细胞白血病)或髓系白血病(急性髓性白血病),但尚不清楚究竟是哪类胎儿细胞首先被转化,以及是什么因素将其引向某一种疾病类型。
具有髓系倾向的特殊胎儿造血前体
研究者将注意力集中在一种称为淋巴系启动的多能前体细胞(LMPP)的胎肝细胞群体上。这类早期造血细胞仍能分化为淋巴系和髓系。在该群体中,他们锁定了携带表面蛋白 CSF1R 的一部分细胞——CSF1R 是一种通常与髓系分支相关的生长信号感受器。利用一种可以在胎儿期开启 KMT2A::MLLT3 融合基因的小鼠模型,研究者比较了 CSF1R 阳性与 CSF1R 阴性 LMPP。在体外培养中,两者都能生成淋巴系集落,但 CSF1R 阳性细胞在髓系条件下形成的集落显著更多,且更经常产生兼具髓系与淋巴系特征的“混合”集落,暗示其具有更高的可塑性和致瘤潜力。
从可塑性前体到白血病发动机
为了检验活体内的结果,团队将这些被改造的胎儿细胞移植到免疫缺陷小鼠中。接受表达 KMT2A::MLLT3 的 CSF1R 阳性 LMPP 的动物发展出侵袭性的急性髓性白血病:它们的血液、骨髓、脾脏、肝脏乃至中枢神经系统都充满不成熟的髓系原细胞,并且可以用首批患病动物的骨髓将疾病传给新的受体小鼠。相比之下,接受 CSF1R 阴性 LMPP 的小鼠起初血液中主要显示不成熟的 B 细胞,更像是淋巴系疾病,且发病较慢。基因组分析显示,CSF1R 阳性 LMPP 表现出与自我更新相关的“类干细胞”基因程序,并与儿科患者中已知的白血病干细胞相一致,而 CSF1R 阴性细胞的基因特征更接近急性淋巴细胞白血病。
生存策略:自噬与生长信号
团队进一步探查使这些 CSF1R 标记的胎细胞得以存活并驱动疾病的机制。他们发现与自噬——细胞内部回收与自我清理系统——相关的基因在 CSF1R 阳性细胞中更为活跃。用药物阻断自噬会显著降低它们形成集落的能力。干扰 CSF1R 信号本身会使髓系产出减少,而当自噬抑制与 CSF1R 通路抑制联合使用时,几乎完全消除了集落生长。重要的是,人类白血病数据集表明,类似的 CSF1R 阳性 LMPP 样群体仅在早期人类发育阶段存在,并且 CSF1R 及若干自噬相关基因在携带 KMT2A 重排的急性髓性白血病中尤其活跃。在一条携带 KMT2A::MLLT3 的儿科白血病细胞系中,CSF1R 抑制剂诱导了显著的细胞死亡,支持这些细胞仍依赖该通路的观点。
从胎儿起源到未来治疗
综合各项证据,该研究表明一种短暂存在、由 CSF1R 标记的胎儿造血前体很可能是 KMT2A::MLLT3 驱动的婴儿急性髓性白血病的起始点和发动机。这些细胞将类干性耐久性与内在的髓系偏向相结合,并依赖 CSF1R 信号与自噬来扩增和维持白血病。由于 CSF1R 是一种已在成人靶向治疗(包括工程化 CAR-T 细胞)中被探索的表面分子,这项工作指向了一个具体且有生物学依据的靶点,可能为那些在出生前就已起病的脆弱婴儿开发适配的治疗策略。
引用: Camiolo, G., González Silvera, D., Leah, T. et al. CSF1R marks a subset of foetal haematopoietic multipotent progenitor cells with acute myeloid leukaemia propagation properties. Leukemia 40, 540–552 (2026). https://doi.org/10.1038/s41375-025-02856-4
关键词: 婴儿白血病, 急性髓性白血病, 胎儿血液发育, CSF1R, 白血病干细胞