Clear Sky Science · zh
JAK2V617F 重新编程缺氧诱导因子‑1,在骨髓增殖性肿瘤中诱导一种非常规的缺氧调控程序
这对血液癌症为何重要
某些生长缓慢的血液癌症,被称为骨髓增殖性肿瘤,可以在多年内处于隐匿的低活性状态,随后突然转化为侵袭性白血病。本研究提出了一个简明但至关重要的问题:一种常见的致癌突变如何劫持细胞的氧感知系统?是否可以在不损伤健康细胞的情况下有针对性地阻断这种劫持?答案可能为高风险患者开辟新的治疗途径,同时保护同样依赖氧感信号的正常组织。
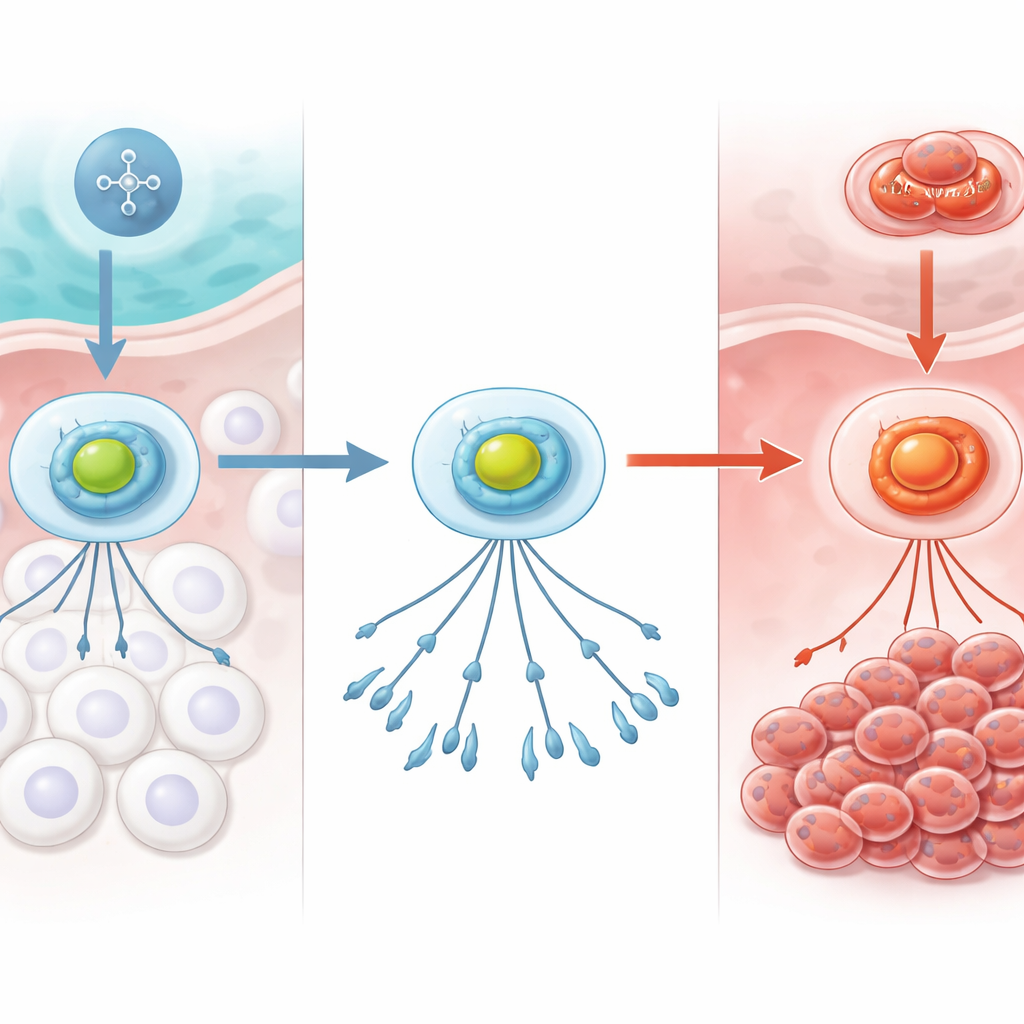
身体的氧气警报系统
细胞持续监测可用氧气的多少。该系统的核心是名为 HIF‑1 的蛋白复合体,它像一个氧气警报器。在正常、富氧的条件下,HIF‑1 的一个亚基会被迅速降解,使警报保持关闭。当氧气下降时,这种降解停止,HIF‑1 稳定下来并进入细胞 DNA,激活帮助细胞适应的基因,例如改变能量利用方式或促进新血管生长。在癌症中,这一系统也可能被肿瘤利用,帮助恶性细胞在如低氧的骨髓等压力环境中存活。
当突变改写警报器
研究者关注一种称为 JAK2V617F 的突变,该突变在骨髓增殖性肿瘤中非常常见。早期研究表明,这一突变使 HIF‑1 在富氧条件下仍处于开启状态。作者使用工程化细胞系,比对了两种条件下 HIF‑1 在 DNA 上的结合:真实低氧状态与在正常氧气下存在 JAK2V617F 突变的情况。他们发现,在突变细胞中 HIF‑1 结合的基因组区域更少,对氧气变化的响应性降低,并且与一组不同的伙伴蛋白相互作用,其中许多与 RNA 加工有关。换言之,这一突变并非单纯把 HIF‑1 永久“打开”——而是将警报器重新调音,使其指向一组不同的靶点。
一种癌症特异性的基因程序
基于这些实验,作者定义了若干依赖 HIF‑1 的基因集合,其中包括他们称之为 JAK2V617F 缺氧特征的基因组。他们进一步考察了这些特征在 172 名 JAK2V617F 阳性骨髓增殖性肿瘤患者的血细胞中被激活的程度。令人意外的是,通常的低氧 HIF‑1 基因程序并不能预测患者的病情严重程度或生存期。相反,突变特异性的缺氧特征能够清晰地区分出病情更严重的患者,并与较差的总生存相关。该集合中的许多基因在巨核细胞祖细胞中尤为活跃——这些骨髓细胞在这些疾病中异常增生并驱动纤维化——其中一些基因参与 DNA 损伤修复这一过程,可能帮助癌细胞抵御有害压力。
疾病突然恶化的线索
患者最担心的情形之一是慢性病程突然转化为侵袭性的“爆发期”白血病。通过分析患者在转化前后配对样本,团队提炼出一个更小的 13 基因子集,称为 HIF1‑MPN‑BP 特征,该子集在转化时会上调或下调。该子集与更高的风险评分、更差的生存率以及更严重的骨髓纤维化强相关。重要的是,这一模式似乎是特异于由 JAK2V617F 驱动的疾病,而非所有白血病的通用特征。该子集中许多基因是合理的药物靶点,提示未来有针对性阻断进展的治疗候选名录。
发现突变的隐秘帮手
JAK2V617F 如何使 HIF‑1 在不依赖氧气的情况下保持活性?通过蛋白化学方法,作者发现,在突变细胞中 HIF‑1 在通常控制其降解的区域带有两个此前未知的化学标记(磷酸化位点)。他们将这些修饰追溯到 PIM1,一种在 JAK2 突变下游被激活的激酶。用试验性药物抑制 PIM1 会导致突变细胞中 HIF‑1 水平下降,但对正常的低氧反应影响较小。抑制 PIM1 还选择性地降低了风险 HIF1‑MPN‑BP 基因的表达并促使突变细胞走向细胞死亡,同时较好地保留了未突变细胞。
这对患者意味着什么
这项工作表明,同一氧感蛋白 HIF‑1 的行为取决于它被如何激活。在由 JAK2V617F 驱动的骨髓增殖性肿瘤中,JAK2–PIM1 信号轴以一种使 HIF‑1 脱离正常氧调控并将其活动收窄到促进疾病的基因集合的方式稳定 HIF‑1。因为这一改变的程序与疾病严重程度和转化风险紧密相关,且可通过阻断 PIM1 得到抑制,它提供了一条有前景的路径,可在保留 HIF‑1 在健康组织中必要功能的同时,有针对性地抑制其在恶性细胞中的活性。未来利用这一差异的疗法或能帮助阻止缓慢进展的血液癌症向危及生命的白血病转变。
引用: Kealy, D., Ellerington, R., Bansal, S. et al. JAK2V617F reprograms Hypoxia Inducible Factor-1 to induce a non-canonical hypoxia regulon in myeloproliferative neoplasms. Leukemia 40, 609–621 (2026). https://doi.org/10.1038/s41375-025-02843-9
关键词: 骨髓增殖性肿瘤, JAK2V617F, HIF-1, PIM1 激酶, 爆发期转化