Clear Sky Science · zh
可溶性 Notch 激动剂促进人源成釉细胞成熟并在牙齿再生中形成类釉质组织
为什么修复牙釉质如此困难
釉质是覆盖牙齿的光亮白色外壳,是人体最坚硬的物质——但一旦损失,便难以自我修复。超过90%的成年人存在不同程度的釉质流失或损伤,然而我们的牙齿没有自然重建这层保护层的机制。本研究描述了一种在实验室中培育人源产釉细胞、推动其完全成熟并在动物体内诱导形成类釉质矿物的方法。这项工作为未来可能用活体组织而非填充物或牙冠来修复牙齿的治疗方案开辟了道路。
从干细胞构建牙釉质
釉质由一种称为成釉细胞的专门细胞制造,这些细胞在牙齿突破牙龈后会死亡。没有它们,成年牙齿无法生成新的釉质。研究人员利用人诱导多能干细胞(即将成年细胞重编程回一种更具可塑性的类胚胎状态)来制造“诱导成釉细胞”。在早期工作中,这些体外培养的细胞能开始类似天然产釉细胞的特性,但在达到完全成熟前停滞,而且仅在与形成基质牙本质的牙本质细胞密切接触时才能正常发挥功能。这提出了一个关键问题:牙本质细胞到底提供了什么,成釉细胞才得以完成其发育?
牙齿细胞之间缺失的对话
为了解码这种细胞对话,团队挖掘了发育中人类和小鼠牙齿的单细胞基因表达图谱。他们寻找那些在釉质形成关键窗口期似乎从牙本质细胞特异性传递到成釉细胞的信号通路。一条通路显著突出:Notch,这是胚胎发育中广泛使用的直接细胞间通信系统。在这些牙齿图谱中,类 Delta 配体(尤其是 DLL1 和 DLL4)主要位于牙本质细胞上,而 Notch 受体则集中在正在成熟的成釉细胞上。当研究者在其共培养体系中用药物阻断 Notch 活性时,成釉细胞显著降低了釉质蛋白 enamelin 的产量——这强烈表明 Notch 信号对于产釉细胞完成成熟至关重要。 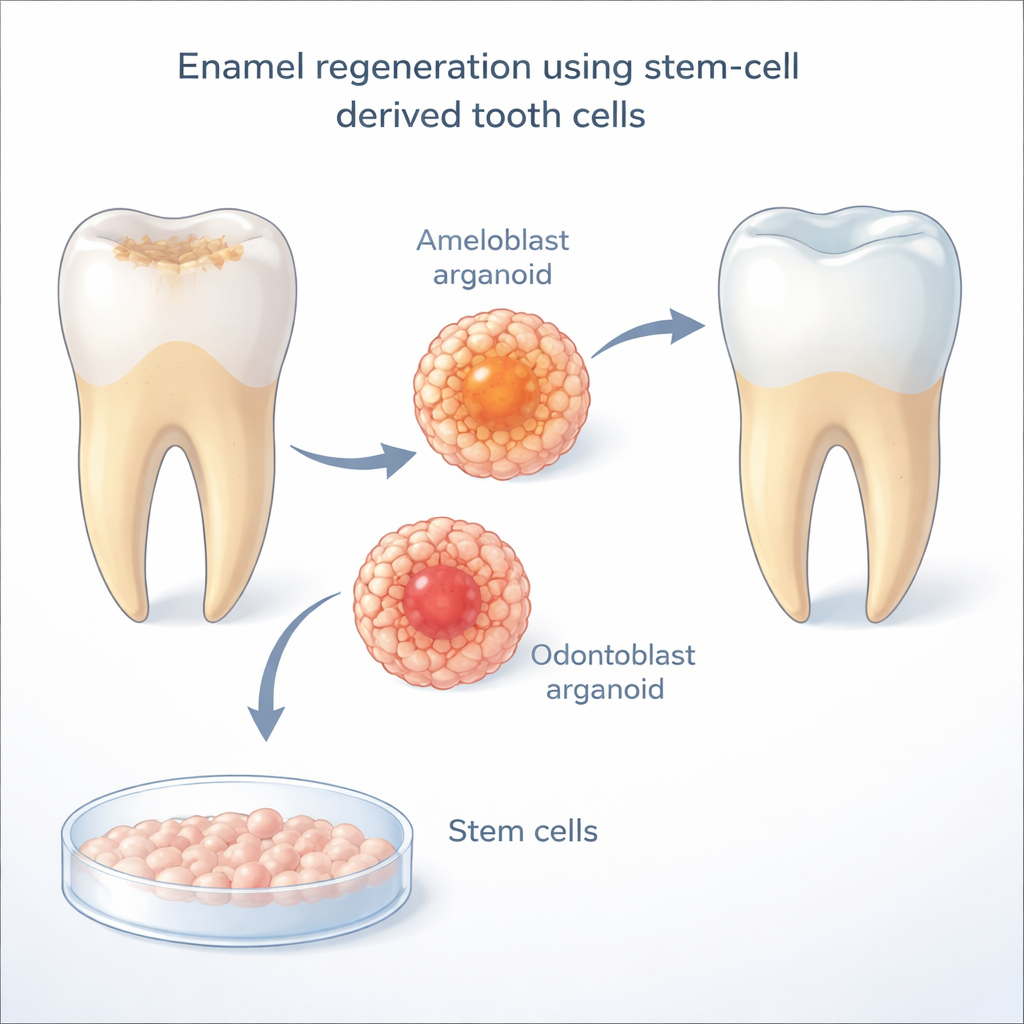
为产釉细胞设计的 AI 蛋白开关
为进一步推进,团队希望以精确且可控的方式激活 Notch,而不依赖真实的牙本质细胞。他们使用了一种通过计算工具设计的人造蛋白 C3‑DLL4。这种可溶分子将三个 DLL4 信号域以刚性三臂支架排列,使其能够像相邻天然细胞一样聚集并激活附近细胞的 Notch 受体。在报告细胞系中,C3‑DLL4 强烈开启了 Notch 依赖的基因表达。加入到早期成釉细胞类器官(由干细胞生长的微小三维细胞团)时,它驱动了一场广泛的基因活性转变。类器官从不成熟的表达谱转向与分泌期及完全成熟成釉细胞相匹配的状态,激活了标志性基因如 AMELX、ENAM、MMP20、ODAM、KLK4、TUFT1 和 WDR72。相反,去除 Notch 活性会阻碍成熟并破坏釉质蛋白的产生。
从类器官到类釉质组织
引人注目的是,当这些被 Notch 激活的成釉细胞类器官移植到免疫缺陷小鼠的肾被膜下这一常用的人源组织检测位点时,它们开始沉积致密的矿化物质。高分辨率微型 CT 扫描和传统的骨染色技术证实了在通常不存在此类组织的部位出现钙化结节。显微镜下可见有序的、极化排列的人源细胞层,表达关键的釉质蛋白和与正常釉质矿化相关的因子 WDR72。虽然这些物质应称为“类釉质”而非完全天然釉质,但它表明工程化的人成釉细胞原则上可以在活体内沉积坚硬的矿物。 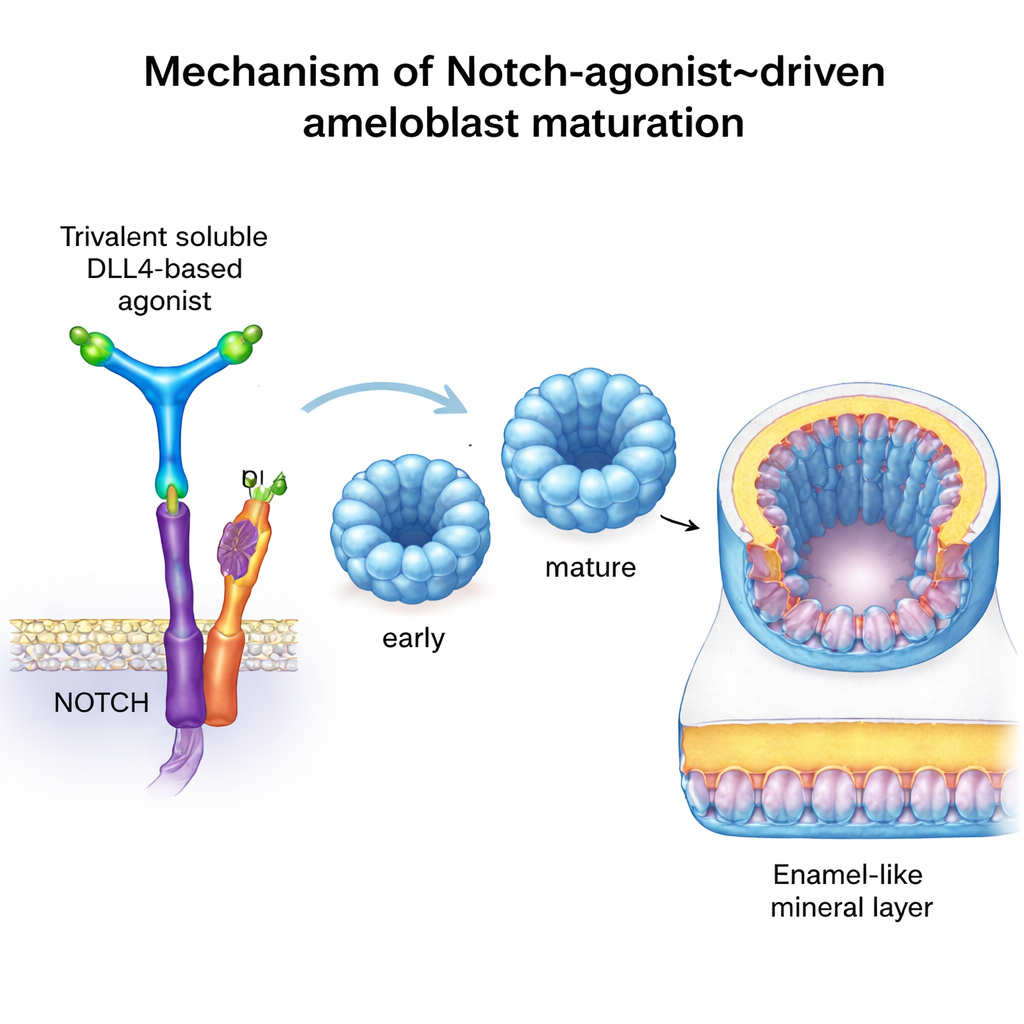
破解导致釉质薄弱的遗传之谜
该研究还解决了长期困扰的关于 DLX3 基因的谜题,该基因的突变会导致某些遗传性釉质缺陷并增加蛀牙风险。DLX3 在成釉细胞和牙本质细胞中均有活性,这使得难以判断在出现问题时哪种细胞类型受影响更大。通过使用他们不依赖牙本质细胞的类器官体系并结合 CRISPR 基因编辑,研究者特异性地在成釉细胞谱系中敲除了 DLX3。成釉细胞形成的早期步骤仍能发生,但最终成熟阶段崩溃:关键釉质蛋白如 enamelin、AMELX、MMP20、KLK4、TUFT1 和 WDR72 在 RNA 和蛋白水平上均显著减少。这表明 DLX3 在人类成釉细胞内部直接必需以完成产釉程序,有助于解释为何该基因附近的变异与釉质脆弱、易龋的牙齿相关。
这对未来牙科护理意味着什么
总体而言,这些发现勾勒出从干细胞到产釉细胞类器官再到体内类釉质组织的逐步路线图,该过程由可调控的 Notch“开启开关”和 DLX3 基因控制。尽管临床牙齿再生仍遥远,但这项工作为理解遗传性牙病、筛选新疗法以及完善用活体细胞而非惰性材料重建丢失釉质的策略提供了强有力的试验平台。对患者而言,长期的愿景是将来看牙可能涉及用生物工程釉质修复磨损或龋坏的牙齿,使其行为更接近天然牙釉质。
引用: Patni, A.P., Mout, R., Alghadeer, A. et al. Soluble Notch agonist enables human ameloblast maturation and enamel-like tissue formation for tooth regeneration. Int J Oral Sci 18, 25 (2026). https://doi.org/10.1038/s41368-026-00429-4
关键词: 釉质再生, 成釉细胞类器官, Notch 信号通路, DLX3, 牙源干细胞