Clear Sky Science · zh
Gli2 和 Gli3 协同介导间充质祖细胞中 HH–TGF-β 交叉通路以协调牙根形态发生
牙根的重要性:远比你想的更关键
大多数人只有在牙痛或照镜子时才会注意到牙齿。但固定牙齿于颌骨中的部分——牙根——与可见的齿冠同样重要。健康的牙根能在咀嚼和说话时保持牙齿稳定,伴随终生。本研究探讨了颌部组织内的微小信号如何告诉未成熟细胞去构建坚韧的牙根,这一机制未来可能用于预防或修复导致牙齿松动和脱落的牙根缺陷。
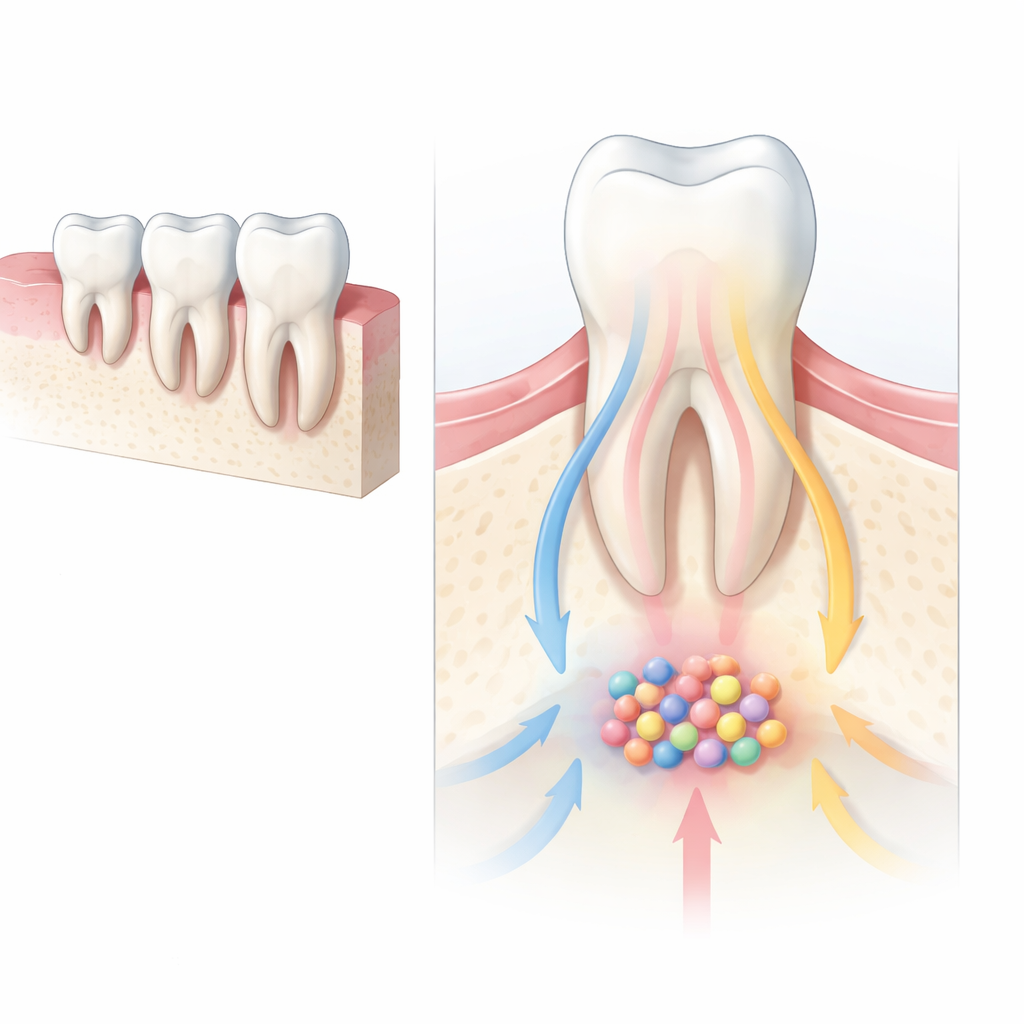
构建面部的迁徙细胞
早期发育时,一类称为颅神经嵴细胞的特殊细胞群迁移进入正在形成的面部和颌骨,并在那里分化为骨、软骨以及支撑牙齿的组织。当这种分化出现问题时,新生儿可能会出现严重的面部和牙科畸形。引导这些细胞的重要信号之一是 Hedgehog 通路,它像分子 GPS 一样,帮助细胞决定去向与命运。作者关注由 Hedgehog 控制的两个辅助蛋白 Gli2 和 Gli3,研究它们如何共同指挥最终构建小鼠臼齿牙根的细胞。
协同工作的两把基因开关
研究人员使用精细设计的小鼠模型,选择性地在位于牙根生长端附近的一组成根祖细胞中关闭 Gli2、Gli3 或两者。单独去除 Gli2 对牙根形成几乎没有影响,而去除 Gli3 则导致牙根明显缩短、牙齿萌出延迟以及牙齿周围支撑性颌骨减少。当同时缺失 Gli2 和 Gli3 时,问题更加严重:牙根约为正常长度的一半,牙齿萌出延迟,包裹牙根的骨组织显著减少。这些实验表明 Gli2 和 Gli3 并非各自为战,而是协作塑造牙根及其周围的支持结构。
将细胞引导到正确的“职业”
为弄清牙根失败的原因,团队仔细观察了成根祖细胞的正常命运。在健康牙齿中,这些细胞会分化为位于牙根内产生牙本质的成釉成牙本质细胞(odontoblasts)、将牙根与骨连接的纤维韧带细胞,以及牙槽骨中的成骨细胞。当缺失 Gli3,尤其是同时缺失 Gli2 和 Gli3 时,这些谱系受到了破坏:牙本质和韧带特征的关键标志物显著减少,靠近牙根的成骨细胞也变少。追踪这些祖细胞的后代显示,许多细胞并未进入牙根及其韧带区域,而是停留在更高的位置,表明它们的正常“职业选择”被干扰。同时,牙根区域的分裂细胞数量下降,可用于构建牙根的细胞基数减少。
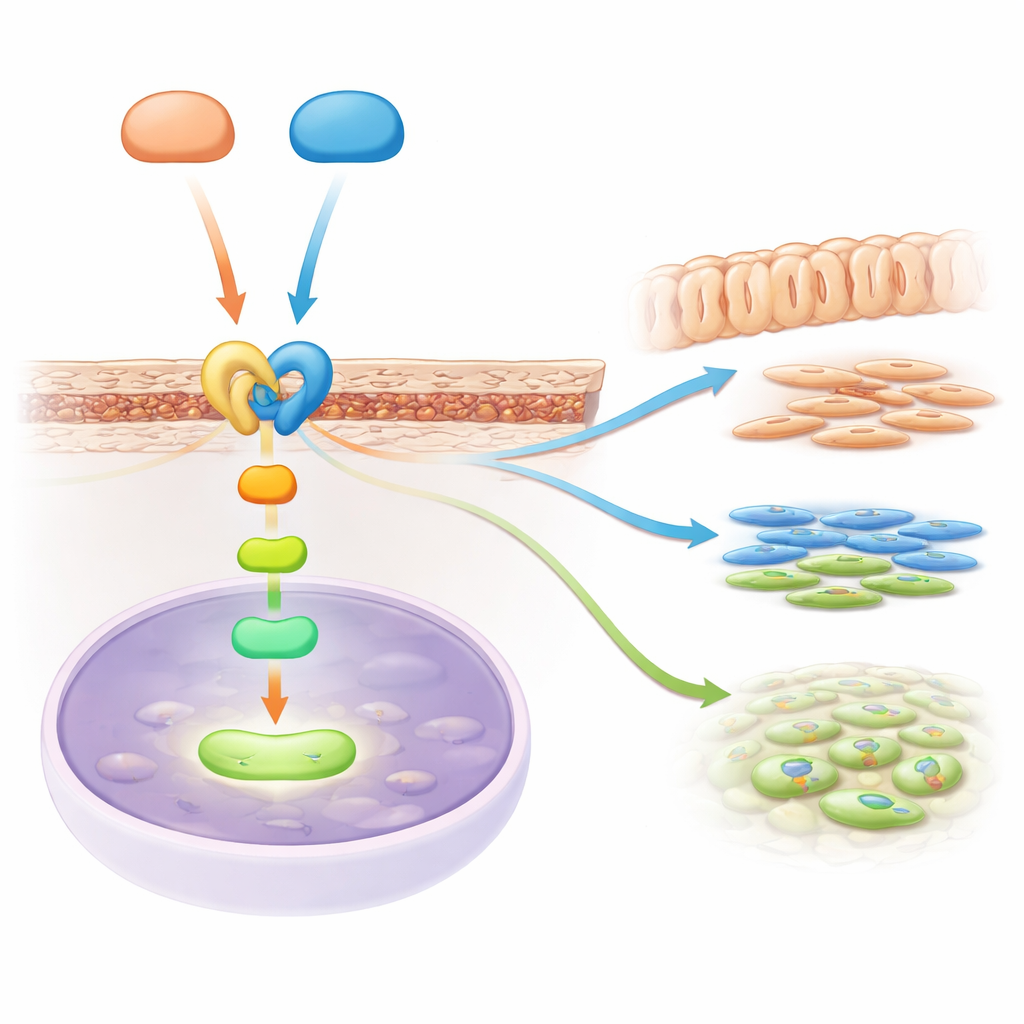
连接两条主要通路的信号中继
故事并不止于 Hedgehog 信号。通过分析哪些基因被激活或抑制,科学家发现当 Gli2 和 Gli3 缺失时,另一条主要通路——TGF-β 信号被削弱。TGF-β 众所周知可促进牙本质和骨的形成。团队定位到一个关键的中继分子——位于成根祖细胞表面的受体 Acvr2b,它有助于将 TGF-β 家族的信号传入细胞内。他们证明 Gli2 和 Gli3 都能物理结合到 Acvr2b 基因的调控区域,从而增强其活性。没有这些辅助因子,牙根区域的 Acvr2b 水平下降,细胞内下游的 TGF-β 传导分子活性减弱,削弱了驱动牙根生长与分化的指令。
部分重接失调的牙根构建程序
为了测试恢复 TGF-β 信号是否有帮助,研究者对同时缺失 Gli2 和 Gli3 的小鼠施用了一种刺激该通路的药物。尽管无法完全恢复正常牙根,治疗确实使牙根延长,周围骨量增加,并相比未治疗的突变体小鼠改善了牙本质和韧带组织的形成。这种部分救助表明 Gli2/Gli3–Acvr2b–TGF-β 链路是 Hedgehog 信号转化为牙根结构生长的主要途径之一。
对未来牙科护理的意义
简而言之,这项工作表明两把遗传“开关” Gli2 和 Gli3 协同工作,帮助年轻的颌部细胞感知 Hedgehog 信号,并通过涉及 TGF-β 的中继,决定分化为构建和支撑牙根的专门细胞。当这种通信中断时,牙根短小、牙齿萌出不良、支撑骨变薄。理解这一信号网络不仅澄清了正常牙根如何形成,也为将来指导干细胞或祖细胞修复受损牙根或全面再生牙根的策略提供了方向。
引用: Zhou, T., Huang, L., Xie, Y. et al. Gli2 and Gli3 synergistically mediate HH-TGF-β crosstalk in mesenchymal progenitor cells to orchestrate tooth root morphogenesis. Int J Oral Sci 18, 30 (2026). https://doi.org/10.1038/s41368-026-00427-6
关键词: 牙根发育, 颅神经嵴细胞, Hedgehog 信号通路, TGF-β 通路, 牙科干细胞