Clear Sky Science · zh
通过 Snx5–EGFR 轴介导的机械传导,植入激活种植体周围的成骨潜能
为何拔牙后保留颌骨至关重要
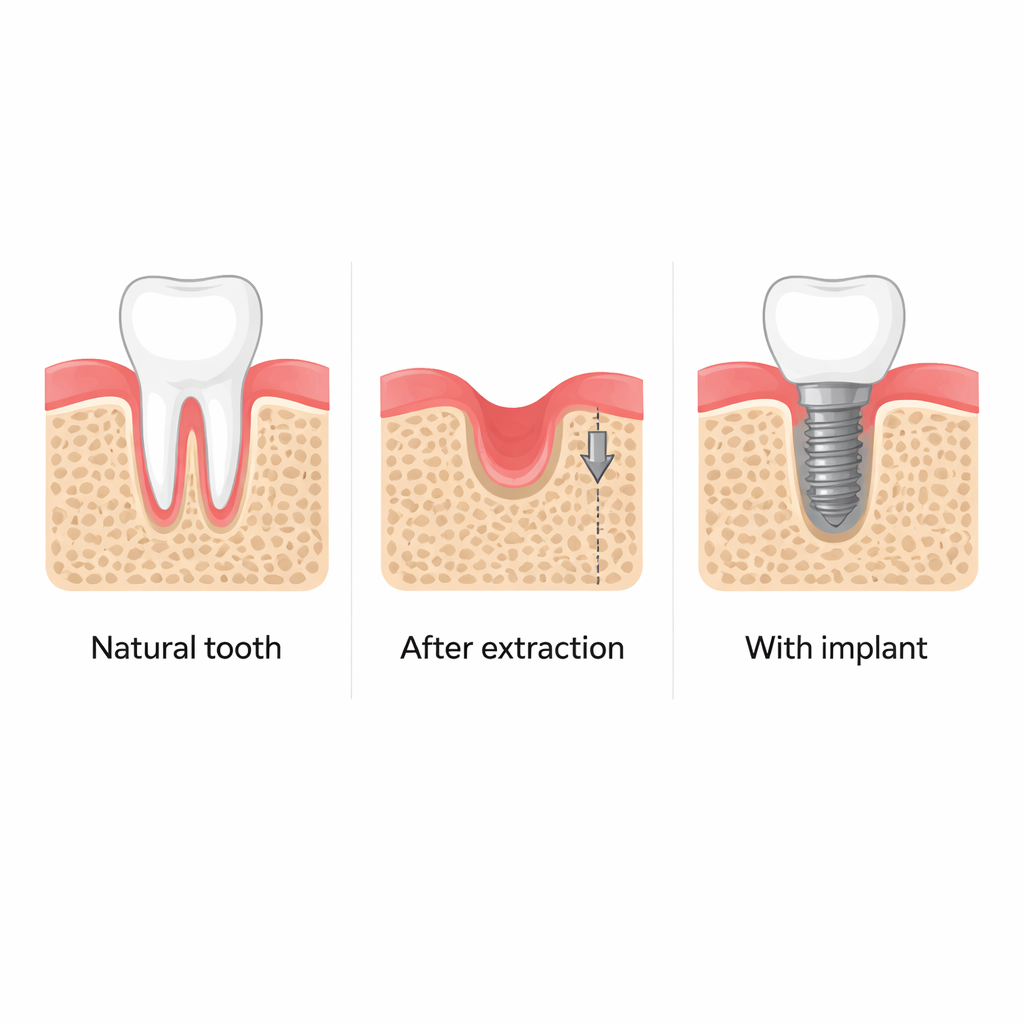
拔牙后,周围的颌骨常常萎缩,这会让日后放置稳固的牙种植体更加困难,并影响面部外观。临床医生早就注意到,仅仅在新鲜牙槽内放入种植体似乎就能帮助保护这部分骨骼,即使在植体尚未用于咀嚼前也是如此。本研究提出一个简单但重要的问题:植入操作本身如何“唤醒”骨组织的修复系统,我们能否利用这一过程来改进颌骨再生?
作为静默骨保护者的种植体
来自患者的临床扫描与小鼠的精细实验均证实,拔牙后尽早放置牙种植体有助于维持周围颌骨的高度和厚度。相比之下,自行愈合的牙槽在几个月内会丧失大量骨量。研究人员在植体周围发现更多不成熟的成骨前体细胞(osteoprogenitors),表明金属柱周围的组织在生物学上更为活跃。这种增强的活性似乎并非由咀嚼力驱动,而是由将略小于槽孔的种植体拧入时产生的非同寻常的机械应力所引发。
骨干细胞内的一个隐蔽开关
研究团队聚焦于一类以 LepR 蛋白为标记的骨髓干细胞——它们是成人新生骨的重要来源。通过比较这些细胞在正常骨、靠近植体的骨以及在体外受应力条件下的基因活动,他们锁定了一个分子:分选蛋白 5(sorting nexin 5,Snx5)。当存在机械信号时,Snx5 水平持续下降。在植体周围,低 Snx5 的 LepR 细胞更可能带有早期成骨细胞的标志,提示下调 Snx5 有助于将这些处于静默状态的干细胞推向活跃的成骨状态。
当该开关失灵,骨组织无法正确感知力
为检验 Snx5 的实际作用,研究者使用了缺失该蛋白的小鼠和干细胞。缺少 Snx5 的干细胞表现出强烈的内在成骨倾向,即使没有额外刺激也会生成更多骨。然而,当科学家施加机械拉伸——模拟植体附近的应变——时,正常细胞会显著提高成骨活性,而缺失 Snx5 的细胞几乎没有响应。在活体小鼠中,正常动物的植体周围出现明显的新骨形成;相比之下,缺乏 Snx5 的小鼠在植入后未能获得额外骨量,这表明 Snx5 对于将机械信号转化为附加的骨修复至关重要,而非仅仅影响基线的成骨形成。
一个回收通路如何控制骨的信号
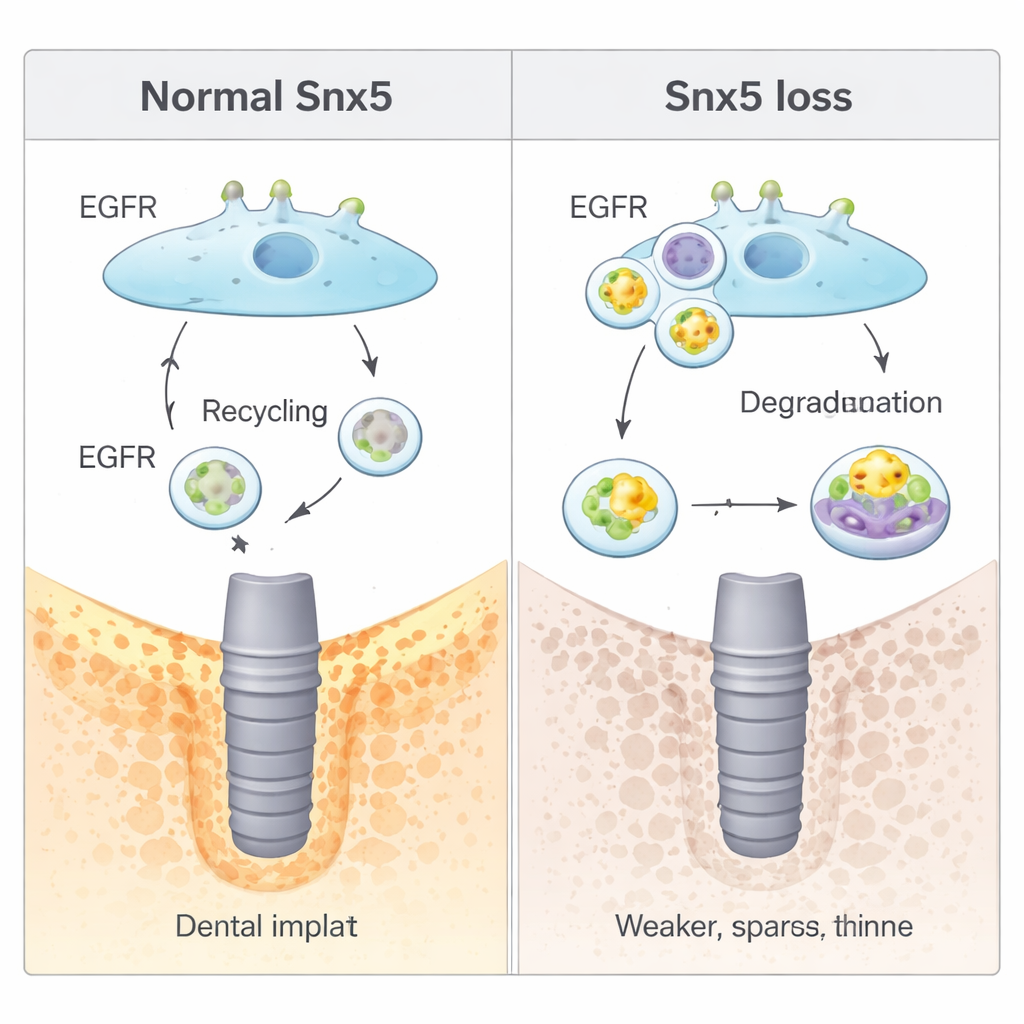
研究随后揭示了 Snx5 在分子水平上的工作机制。许多生长信号通过位于细胞表面的受体传递,这些受体不断被内吞并被回收或降解。Snx5 属于一类指导这种运输的“分选”蛋白。在本研究中发现,Snx5 将表皮生长因子受体(EGFR)在内吞后引导回到细胞膜。缺失 Snx5 时,更多的 EGFR 被送入细胞的“消化”隔室(溶酶体)并被降解。这种降低的 EGFR 信号出乎意料地提升了基线的成骨形成,但使细胞在机械力变化时难以调整其行为。人工激活 EGFR 的药物削弱了在无 Snx5 情况下观察到的额外成骨,而抑制溶酶体降解的药物则恢复了 EGFR 信号并再次降低了过度成骨。
这对未来种植患者意味着什么
对外行人来说,这些发现表明颌骨内存在一个内建系统,能够感知植入时产生的细微推拉并将其转化为额外的骨生长。Snx5 像一位交通指挥,维持关键生长受体 EGFR 在恰当的循环水平,使骨干细胞能够“听见”并响应这些机械信号。当该指挥被改变时,骨组织在静息状态下可能更易形成,但会失去对力的精细响应。理解这一 Snx5–EGFR 轴为开发新治疗手段打开了大门——比如药物或种植体表面涂层,可以调节骨组织的机械敏感性,帮助在复杂临床情况下保护颌骨并提高种植成功率。
引用: Jiang, X., Weng, Y., Feng, Y. et al. Implantation awakens peri-implant osteogenic potential via Snx5-EGFR axis-mediated mechanical transduction. Int J Oral Sci 18, 18 (2026). https://doi.org/10.1038/s41368-025-00423-2
关键词: 种植牙, 颌骨再生, 机械转导, 骨干细胞, EGFR 信号通路