Clear Sky Science · zh
基于 DNA 和 RNA 的扩增子测序:重度早幼儿龋患儿上皮下及牙本质病变牙菌斑的配对分析
为什么幼儿严重蛀牙很重要
幼儿期的龋齿远不只是美容问题。重度早幼儿龋(S-ECC)可以毁坏乳牙,导致剧烈疼痛,影响睡眠和进食,甚至需要在全身麻醉下治疗。本研究提出了一个简单但关键的问题:哪些微生物不仅存在于龋洞中,而且在深层真正损害儿童的牙齿?它们与牙面表层寄居的微生物有何不同?
超越常见嫌疑者
几十年来,一个主要“罪魁祸首”——变异链球菌(Streptococcus mutans)被认为是龋齿的元凶。但牙医和科学家现在知道,龋齿是由整套细菌群落驱动的,这些细菌以糖为食并产生酸。在 S-ECC 中,蛀蚀从外层釉质快速蔓延到较软的内层牙本质,基本上从内部掏空牙齿。本研究团队关注儿童(六岁以下)牙齿中那一深层受损区,比较严重龋坏牙齿牙本质内的细菌与邻近牙面——即齿颈上菌斑(supragingival plaque)上的细菌。
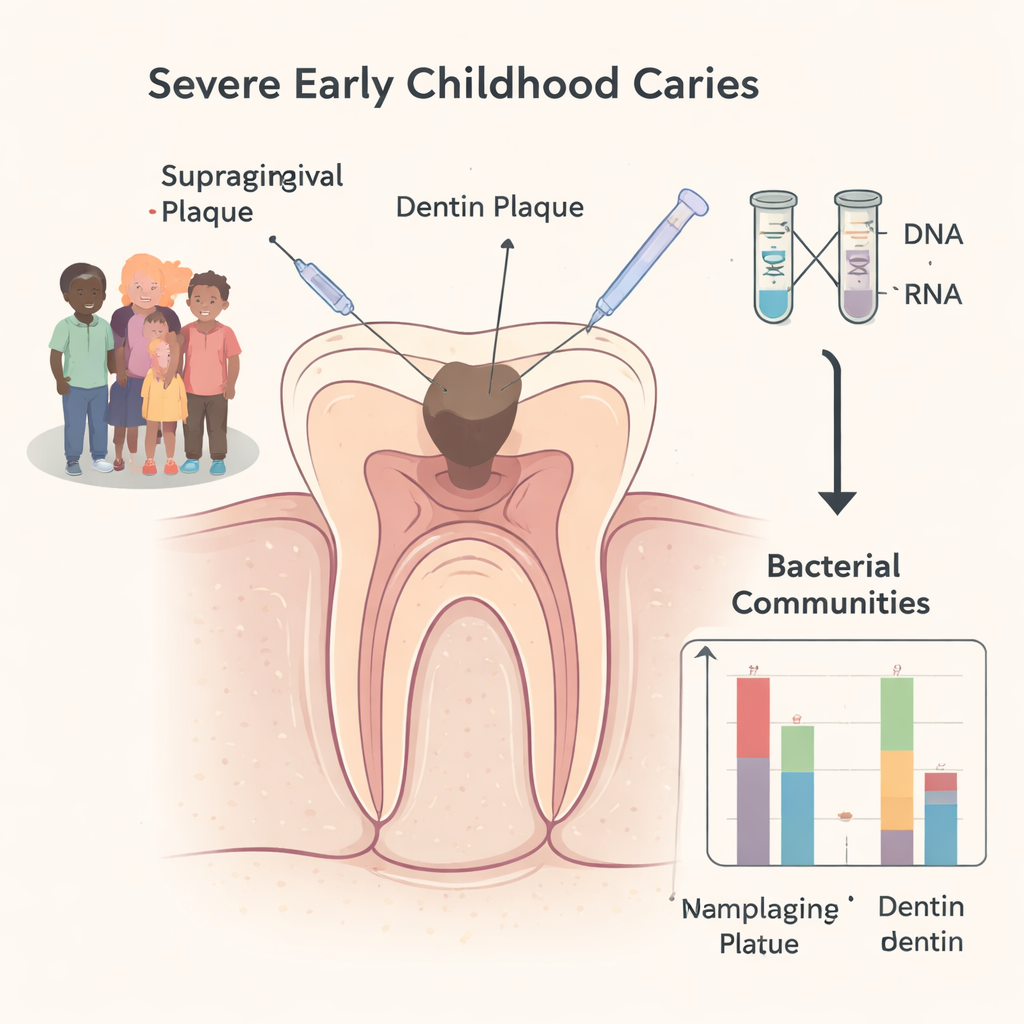
分层取样:来自小患者的微量样本
研究者与 13 名需要在全身麻醉下拔除多颗牙以治疗 S-ECC 的儿童合作。从每位儿童的同一颗牙上采集两份样本:来自外表面的菌斑和拔牙后从牙本质深处刮取的菌斑。随后他们使用现代基因技术读取细菌标志基因 16S rRNA 的两种形式。一种来自 DNA,可显示哪些物种存在(无论存活与否);另一种来自 RNA,RNA 在体内易降解且仅由代谢活跃的细胞产生,因此可反映哪些细菌当前处于活跃、代谢“启动”状态。
更简单但更严酷的牙本质深层环境
当团队比较表面和牙本质深层的微生物群落时,发现深层病变的细菌种类总体更少,但在不同儿童之间表现得更为相似。换言之,随着蛀蚀向内侵袭,群落变得多样性降低且趋于一致,更有利于少数耐受力强的微生物生存。这些幸存者适应了黑暗、保护性且缺氧的微环境,并长期浸泡在由持续糖分分解产生的酸中。相比之下,表面菌斑包含更丰富、多样的物种组合,且在儿童间差异更大,反映了口腔中不断变化的条件。
哪些细菌真正造成损害?
通过比较 RNA 与 DNA,研究者能够区分仅仅存在的细菌与那些特别活跃的细菌。若干已知与龋病相关的类群(包括 Streptococcus 和 Prevotella)在牙本质中富集,但它们的 RNA 水平表明在该处仅呈中等活性。相比之下,Lactobacillus 组的细菌——尤其是鼠李糖乳杆菌(Lactobacillus casei)——在牙本质中既表现出更高的丰度,又显示出显著偏高的 RNA/ DNA 比率,提示强烈的代谢活性。另一种物种,Oribacterium sp. HMT-078,也在深层病变中持续富集并更为活跃。综上,研究结果指向 L. casei 与该类 Oribacterium 为在极酸性条件下溶解牙本质、维持病变环境的关键参与者。
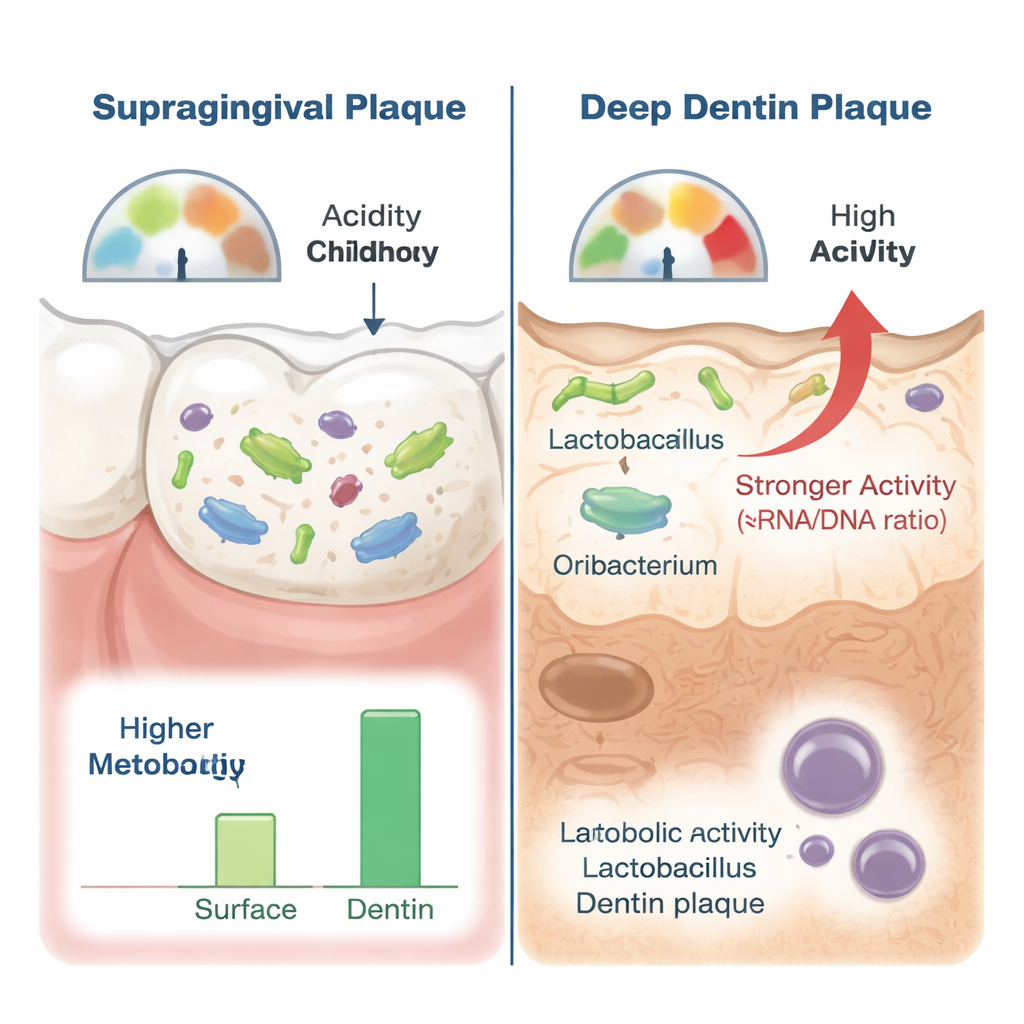
对保护幼齿的启示
对非专业读者来说,结论是:婴幼儿最严重的那类龋齿看来并非由任何常见的龋病细菌单独造成,而是由一群专门适应牙本质深处极酸环境的微生物驱动。鼠李糖乳杆菌(Lactobacillus casei)及其相关物种似乎是特别活跃的罪魁,与其他产酸菌协同作用。了解在牙齿崩解处哪些细菌最活跃,有助于指导未来的策略——从有针对性的预防和饮食建议,到旨在破坏这些深层嗜酸群落、在它们摧毁儿童牙齿之前制止其发展的新型治疗方法。
引用: Naumann, A.A., Elmorr, E.M., Lamont, E.I. et al. DNA and RNA-based amplicon sequencing of paired supragingival and dentin lesion plaque in children with severe early childhood caries. Int J Oral Sci 18, 19 (2026). https://doi.org/10.1038/s41368-025-00421-4
关键词: 早幼儿龋, 口腔微生物组, 牙本质菌斑, 鼠李糖乳杆菌(Lactobacillus casei), 儿童龋齿