Clear Sky Science · zh
对与疾病相关突变的微小RNA加工机器的结构洞察
微小的RNA“剪刀”如何影响健康与疾病
在每个细胞内,都存在一个隐秘的编辑系统,在基因信息被读取前对其进行修剪。该系统依赖于被称为微小RNA(microRNA)的微小RNA片段,它们像微调旋钮一样同时调节数千个基因。当产生微小RNA的分子“机器”正常工作时,细胞的生长、分裂和分化都在受控范围内进行。但当这些机器因突变受损时,基因活性的平衡可能倾向于癌症、血液疾病或大脑发育问题。本文解释了理解这些机器的三维形状如何帮助科学家定位出问题所在并探索可能的修复方法。
细胞的基因“调暗”工具箱
微小RNA是约22个核苷酸长的短RNA片段,本身不编码蛋白质。相反,它们附着于较长的信使RNA(mRNA)上,要么标记其被降解,要么阻止其被翻译,实际上是将基因的表达降低而非完全关闭。为了生成这些微小RNA,细胞将较长的RNA前体通过一个分阶段的加工流水线。首先,酶DROSHA在细胞核中将庞大的初级转录本修剪成较短的发夹状片段。随后这些片段移到细胞质,另一种酶DICER在此处以“尺子”式的距离测量并切割它们,产出微小RNA大小的双链体。最后,每个双链体的一条链被装载到名为Argonaute 2(AGO2)的蛋白中,AGO2以该微小RNA为向导去寻找匹配的信使RNA并使其沉默。 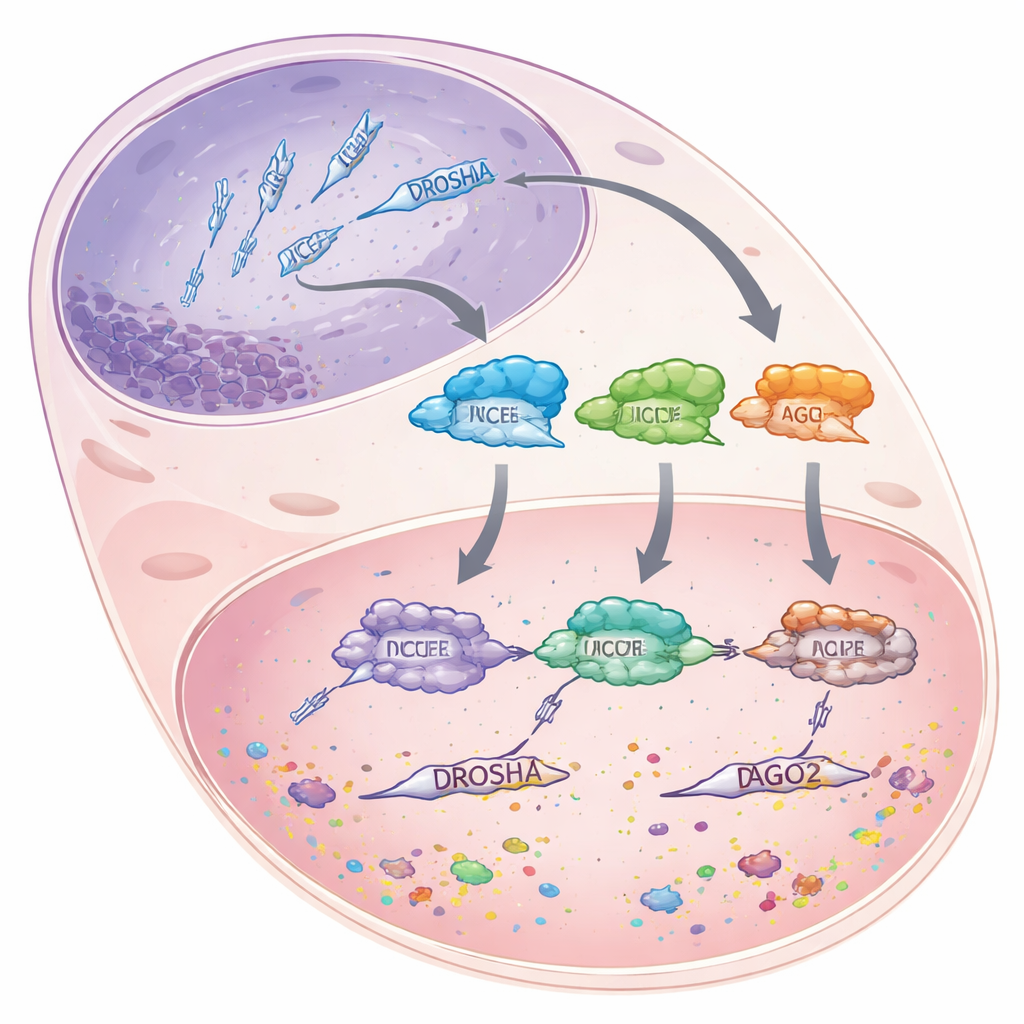
精细的构形与精确的任务
DROSHA、DICER 和 AGO2 并非简单的剪刀;它们由多个相互作用的部件构成,必须以协调的方式运动。DROSHA 与其搭档蛋白 DGCR8 协同工作,夹持初级微小RNA发夹的末端并准确判断切割位置。DICER 通过其结构域形成的一种内置“尺子”来设定从持端到催化中心固定的距离,从而确定切割位置。AGO2 将单链微小RNA包裹起来,使其“seed”序列完美暴露以识别目标信息,而金属离子与核心中的关键氨基酸排列就位,当配对足够强时即可切割那些目标。在这三种蛋白中,带正电的沟槽和柔性连接片引导RNA链就位,而金属结合口袋和催化残基则执行化学剪切。
当“剪刀”弯曲或钝化
来自癌症、血液疾病和神经发育综合征患者的遗传研究发现了这些微小RNA机器中的突变聚集区。许多最具破坏性的变化直接位于催化中心或紧密的RNA抓握表面。例如在 DROSHA 中,诸如 E1147K 和 D1219G 这样的取代发生在切割位点的核心,破坏了保持必要金属离子的能力,使酶无法加工初级微小RNA。其他 DROSHA 突变,例如移除切割区域的截短变体或使其支撑螺旋不稳定的改变,会削弱整个复合体,导致威尔姆斯肿瘤、骨髓疾病和神经系统疾病中微小RNA 水平的总体下降。在 DICER 中,反复出现的突变聚集在其两个切割结构域之一,使产物偏向性改变,从而导致微小RNA 双链的某一臂丢失,这会转变促生长与抑生长信号之间的平衡。 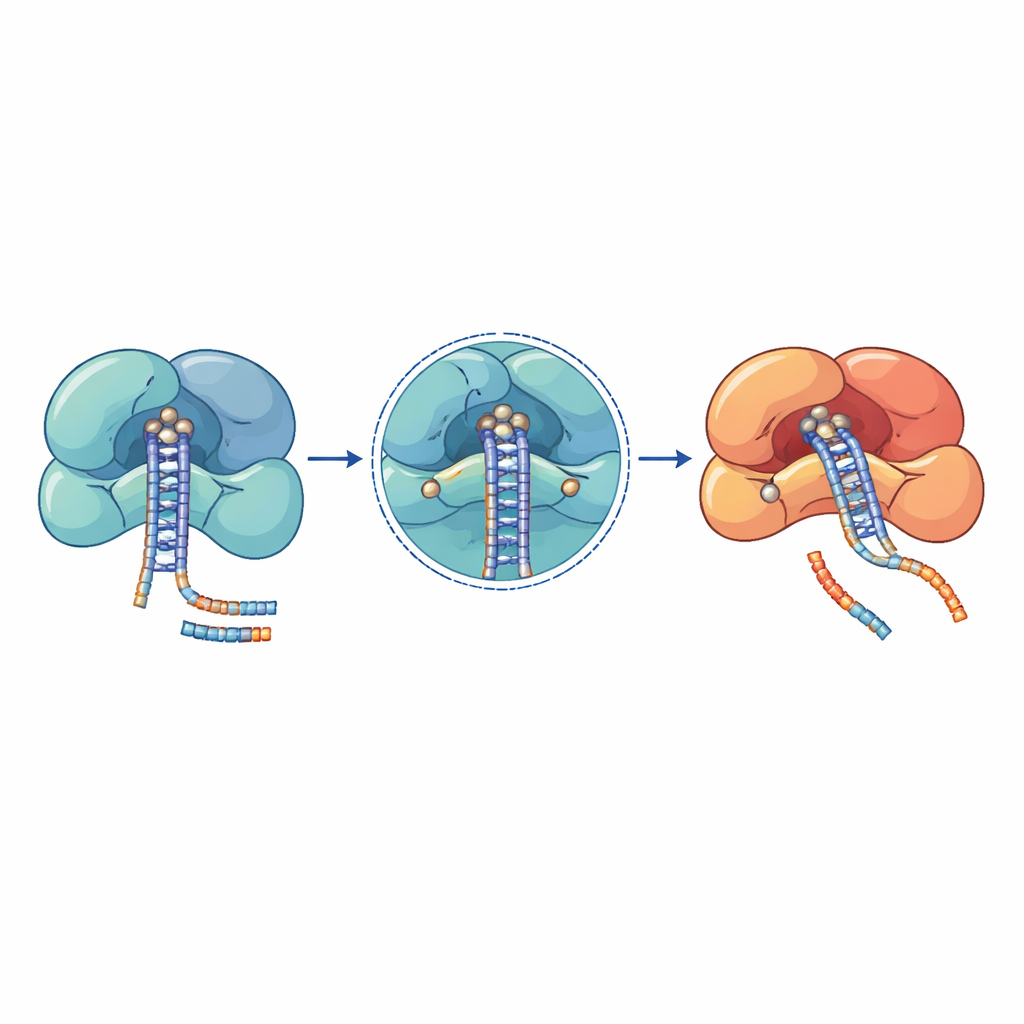
脑内及其他处的导向失准
AGO2 的突变讲述了一个不同但相关的故事。直接袭击其催化核心的突变很少见,可能因为这类缺陷在发育早期就会致命。相反,与疾病相关的变体倾向出现在柔性连接区和维持 AGO2 形状的结构域连接处。在 Lessel–Kreienkamp 综合征(一种神经发育疾病)中,这些连接区及其周围表面的突变会微妙地扭曲 AGO2 的 PAZ、MID 和 PIWI 结构域的排列与运动。这可能使向导微小RNA 失准或削弱其与目标 RNA 的结合,从而在大脑发育过程中模糊基因沉默的精确性。沿微小RNA 通路上的任何类似结构改变——无论发生在 DROSHA、DICER 还是 AGO2——都可能向外泛化,改变参与细胞生长、造血或神经回路构建的整个基因网络。
把结构线索转化为未来治疗
通过将疾病突变叠加到这些蛋白的高分辨率三维图谱上,研究者可以精确分类每一种变化如何造成问题——无论是削弱切割锋利度、松弛与搭档蛋白的重要接触,还是弯曲关键螺旋使其错位。这些结构见解为有针对性的干预打开了大门:稳定被削弱界面的低分子化合物、引导部分功能性酶回到正确底物的设计RNA,或能将突变蛋白推向更活跃构象的变构化合物。对于非专业读者而言,核心信息是:细胞RNA“剪刀”上的微小结构变化可以对健康产生巨大的影响,但它们也为设计面向突变的下一代精准疗法提供了明确的切入点。
引用: Lee, H., Lee, J. & Roh, SH. Structural insights into disease-associated mutations in the microRNA processing machinery. Exp Mol Med 58, 639–649 (2026). https://doi.org/10.1038/s12276-026-01669-4
关键词: 微小RNA, RNA 干涉, DROSHA DICER AGO2, 癌症遗传学, 神经发育障碍