Clear Sky Science · zh
Snail蛋白稳定性的调控机制:泛素–蛋白酶体系统与伴侣介导的自噬
为何癌症扩散仰赖一个脆弱的蛋白
当肿瘤细胞脱离原发肿瘤并迁移到远端器官时,癌症才真正变得危及生命。这种扩散或转移部分依赖于一种强大的“主开关”蛋白Snail,它帮助细胞放松相互间的连接并变得更具运动性。本文解释了细胞如何通过两大主要废物处理系统迅速降解Snail以将其控制在短暂水平。理解这种平衡为减缓或预防转移提供了新的思路。
从紧密堆积的细胞到游走的侵袭者
在健康组织中,上皮细胞形成有序、砖块状的层,保持固定并紧密粘附于邻近细胞。要让肿瘤细胞逃逸,它通常经历一种称为上皮–间质转化(EMT)的改造,在此过程中失去紧密接触并获得运动和侵袭能力。Snail是驱动这种改造的关键:当它存在于细胞核中时,会关闭维持细胞–细胞粘附的基因,并激活有利于运动和侵袭的基因。高水平的Snail与侵袭性癌症和较差的患者预后相关,因此细胞在正常情况下已经进化出让Snail稀少且寿命短的调控方式。
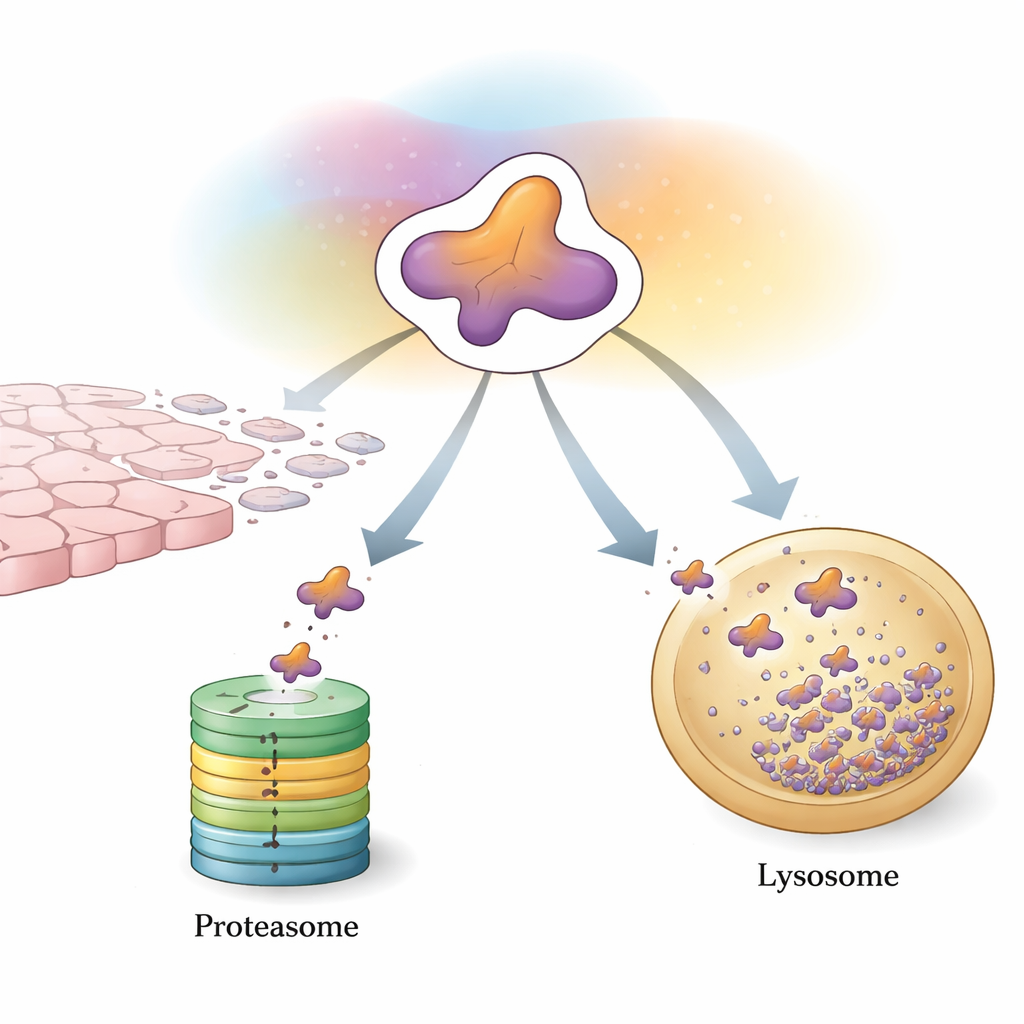
细胞的第一道控制线:标记并粉碎
细胞控制Snail的一个主要方式是通过泛素–蛋白酶体系统——一个为不需要蛋白质贴标签并粉碎它们的机器。专门的酶在Snail上附加由称为泛素的小蛋白组成的“旗标”。当这些旗标以特定模式积累到一定程度时,Snail会被引导进入蛋白酶体,一个桶状复合体,将其切割成片段。大量辅助蛋白对这一过程进行微调。有些酶附加促降解的链条,迅速将Snail送入粉碎机,有助于抑制肿瘤生长和扩散;而另一些则添加能稳定Snail或间接促进其基因表达的链条,使平衡向EMT和转移倾斜。磷酸化和乙酰化等化学修饰则像额外的开关,控制哪些辅助因子能结合Snail以及Snail是否会被降解或获赦。
解除刹车:救援Snail的酶
故事并不止于对Snail的标记。另一类称为去泛素化酶的酶可以剥离泛素旗标,将Snail从蛋白酶体拯救出来。许多此类酶在癌症中被开启或增强,使Snail得以避免降解并在细胞核中持续存在。它们的作用强烈依赖细胞环境:在某些情况下它们直接稳定Snail,而在另一些情况下则影响Snail在细胞中的定位或与伴侣蛋白的相互作用。来自与癌症相关通路的信号,如生长因子和应激反应,参与到这个网络中,决定Snail是被迅速清除还是被允许推动EMT程序。
第二道安全网:选择性递送到细胞的回收中心
除了蛋白酶体之外,细胞还依赖自噬——一系列将蛋白送入酸性隔室(溶酶体)进行降解的途径。本文综述强调一种高度选择性的形式,称为伴侣介导的自噬(CMA),作为控制Snail的第二条主要途径。CMA识别Snail中的一段短序列,并在运输伴侣蛋白的帮助下,将细胞质中的Snail递送到溶酶体进行破坏。在侵袭性较低的乳腺癌细胞中,该系统使Snail大多停留在细胞核外并易被溶酶体清除。而在更具侵袭性的三阴性乳腺癌中,Snail倾向于在细胞核中积累并避开CMA,从而增强其触发EMT和转移的能力。
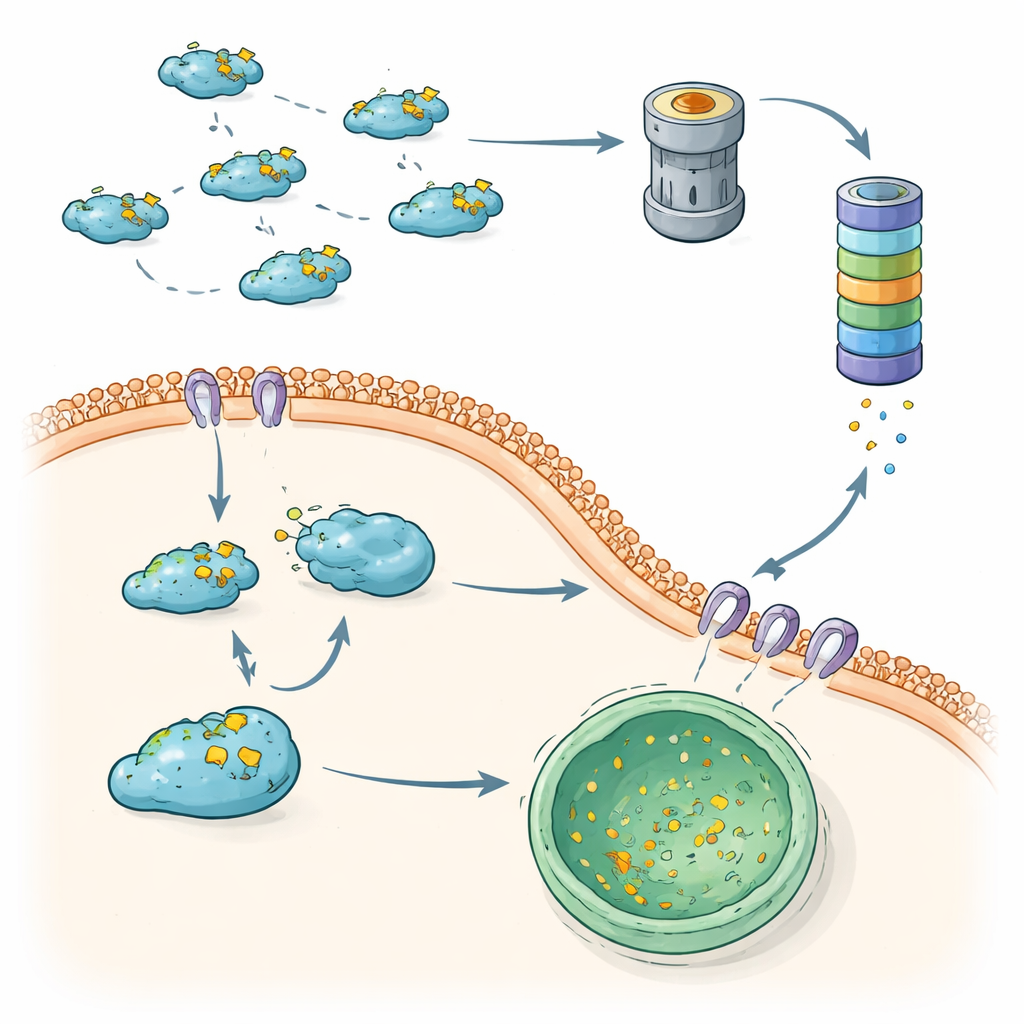
当质量控制失效,转移占上风
综合来看,这些发现表明细胞使用两条互补的“质量控制”轴来限制Snail:泛素–蛋白酶体途径和基于CMA的溶酶体降解。当两者正常工作时,Snail被迅速周转,限制了EMT并有助于防止肿瘤细胞扩散。当任一轴被削弱——通过标记酶、去泛素化酶或CMA组分的变化——Snail变得更稳定、在细胞核中积累并强烈促进侵袭性行为。通过绘制这些相互关联的降解路径,文章勾勒出新的治疗可能性:恢复或增强Snail降解的药物,或将Snail重新引导至CMA或蛋白酶体降解的策略,可能有助于在不完全关闭这些必要蛋白回收系统的情况下,重新施加对转移的制动。
引用: Kim, M., Hong, KS., Kim, T. et al. Regulatory mechanisms for Snail protein stability: ubiquitin–proteasome system and chaperone-mediated autophagy. Exp Mol Med 58, 408–415 (2026). https://doi.org/10.1038/s12276-026-01667-6
关键词: 癌症转移, 上皮–间质转化, Snail蛋白, 蛋白降解, 自噬