Clear Sky Science · zh
红细胞生成—肌苷代谢轴失调引发青光眼视网膜神经变性:新的诊断与治疗
这项研究为何与视力和健康相关
青光眼通常被描述为眼内压问题,逐步夺走视力。但本研究认为病程起点更早、且远在眼球之外:在骨髓和我们的红细胞中。作者展示了红细胞生成与供能失调会使视网膜缺氧和能量不足,同时发现一种意外的潜在帮手分子——肌苷,可能既能用于诊断也能用于治疗青光眼。
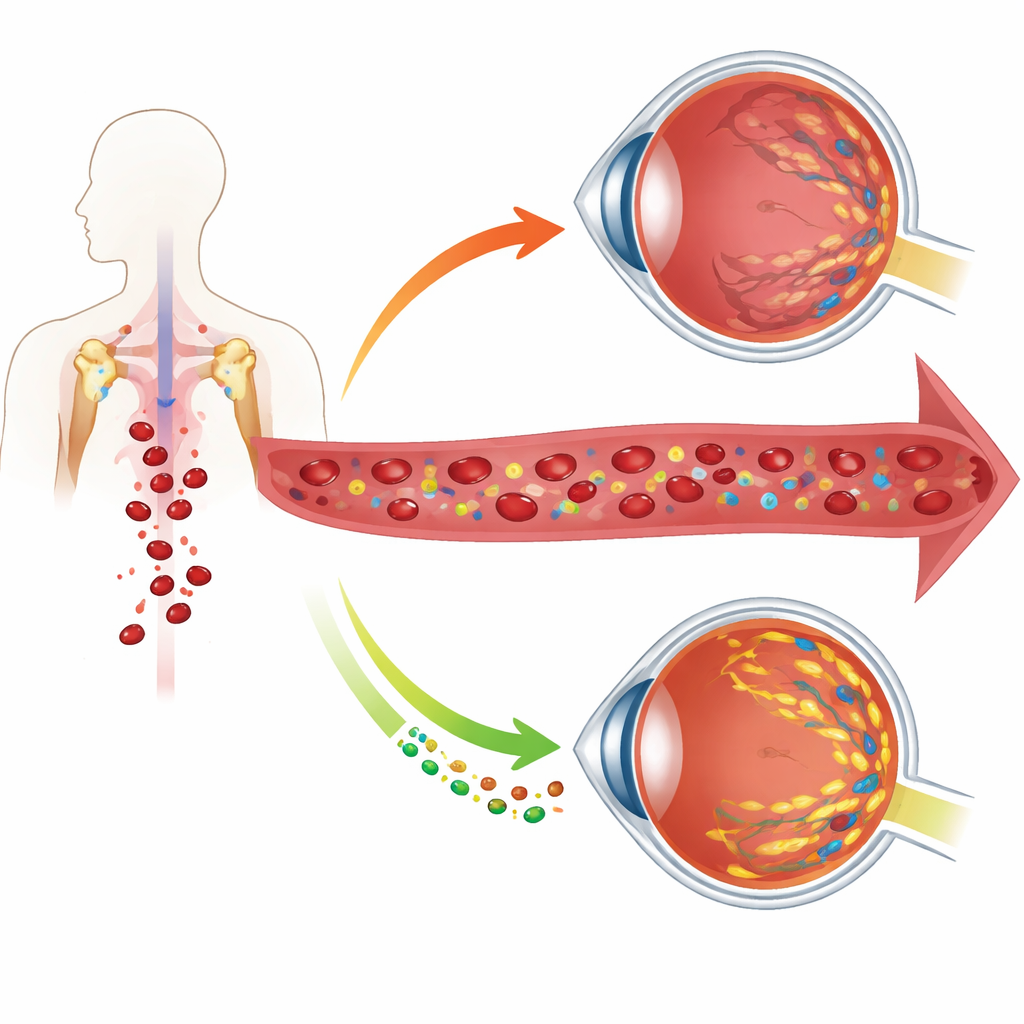
眼病为何始于血液
研究使用了超过127,000名来自英国生物样本库的数据以及一个独立医院队列,发现青光眼患者普遍红细胞数较少、血红蛋白和红细胞压积(红细胞体积分数)降低。这些变化在两种主要临床型的青光眼中均有观察到,并与更高的眼压、更薄的视网膜神经层以及更差的视野相关联。换言之,青光眼患者往往在携带全身包括眼部氧气的基本细胞上存在轻度但重要的不足。
处于代谢应激中的红细胞
青光眼患者的红细胞不仅数量减少——它们在生化上也已被耗竭。详细的化学谱分析显示,其常用燃料葡萄糖并未被有效利用。细胞外葡萄糖高于细胞内,膜上主要糖转运蛋白减少,关键能量通路处于低活性。同时,这些细胞具有更高的氧化应激和更低的能量分子储备如ATP。作为权宜之计,它们转而燃烧另一种小分子肌苷,来产生有助于血红蛋白更容易释放氧气的中间体。这一应急转换由一种能量感应酶AMPK驱动,短期内改善了脱氧氧气释放,但逐渐消耗了体内的肌苷储备。
从骨髓功能衰竭到视网膜损伤
由于红细胞构成了机体中大多数细胞,它们对肌苷需求的增加对其他组织也有影响。在小鼠实验中,如果在红细胞上去除主要肌苷转运蛋白(ENT1),这些动物会发生与年龄相关的青光眼:眼压升高、视网膜神经节细胞死亡,且红细胞释放氧气能力下降并产生更多活性氧。骨髓研究显示,早期造血祖细胞缺乏肌苷信号会损害新红细胞生成,迫使脾脏承担应急造血功能。总体来看,这些证据支持这样一条事件链:红细胞生成受损和代谢适应不良造成慢性氧供应不足,最终损害视网膜。
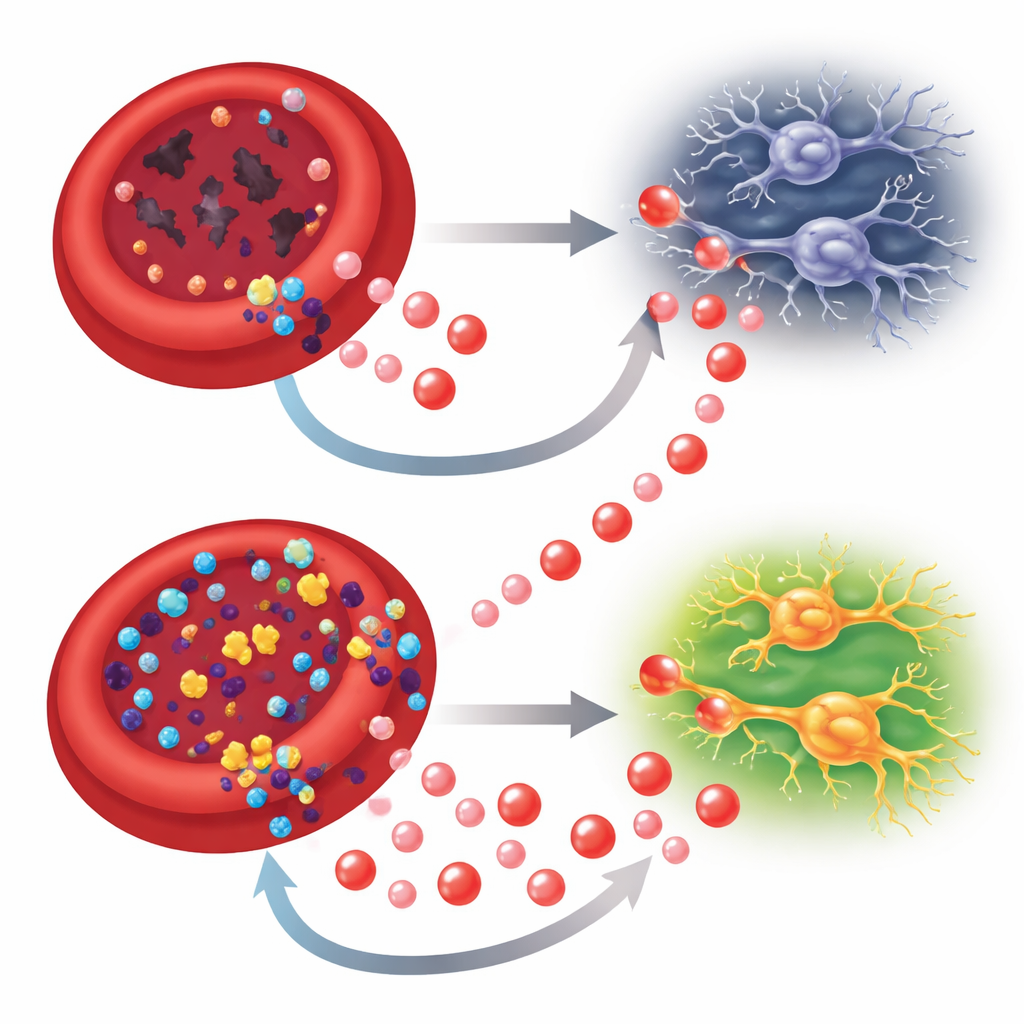
肌苷作为代谢生命线
研究团队接着探讨补充肌苷是否能打破这一恶性循环。在一种通过短暂升高眼压诱导的青光眼小鼠模型中,每日注射肌苷可改善红细胞的氧释放能力、降低氧化应激并恢复红细胞计数与血红蛋白水平——且不缩短红细胞寿命。在骨髓中,肌苷使干细胞和祖细胞重新向红细胞谱系分化,并使红细胞成熟晚期过程恢复正常。与此同时,经治疗的小鼠表现出更好的视网膜氧合、更厚的神经层、更多存活的视网膜神经节细胞以及更强的电生理和行为学视功能。在体外培养的暴露于低氧且无葡萄糖的视网膜神经元中,肌苷本身可作为备用燃料,进入多个能量通路,提升ATP水平并降低氧化损伤。
检测与治疗青光眼的新途径
通过将大规模人群数据与详细的动物与细胞实验结合,本研究将青光眼重新框定为一种系统性的血液—视网膜代谢疾病,而非纯粹局限的眼病。红细胞中以肌苷及其分解产物为核心的十种代谢物标志,可将青光眼患者与健康受试者区分,其准确性可与标准眼科检测相当,提示未来血液筛查的潜在作用。与此同时,肌苷显现为一种多功能的救援因子:它支持红细胞生成、改善氧输送,并直接为受压的视网膜神经元提供能量。尽管需要临床试验来评估人体的安全性与疗效,该研究指向肌苷代谢作为诊断与减缓由缺氧驱动的青光眼神经变性的一条有前景的新靶点。
引用: Chou, Y., Liu, W., Li, Y. et al. Erythropoiesis–inosine metabolic axis failure underlying retinal neurodegeneration in glaucoma: novel diagnoses and therapies. Exp Mol Med 58, 562–578 (2026). https://doi.org/10.1038/s12276-026-01654-x
关键词: 青光眼, 红细胞, 视网膜神经节细胞, 肌苷代谢, 眼部缺氧