Clear Sky Science · zh
与癌相关成纤维细胞、脂肪细胞和免疫细胞之间的代谢串话作为免疫抑制性肿瘤微环境的驱动因子
为何肿瘤“邻里”很重要
癌症并非孤立生长。它生存在一个由支持细胞、脂肪细胞和免疫细胞组成的繁忙邻里中,这些细胞不断交换营养和化学信号。本文解释了该邻里的“代谢”——细胞如何使用和共享燃料——如何在不知不觉中将战局倾向于肿瘤、不利于免疫系统。理解糖类、脂肪和氨基酸的这一隐秘经济学,正在开启改善免疫治疗效果和切断肿瘤支持系统的新途径。
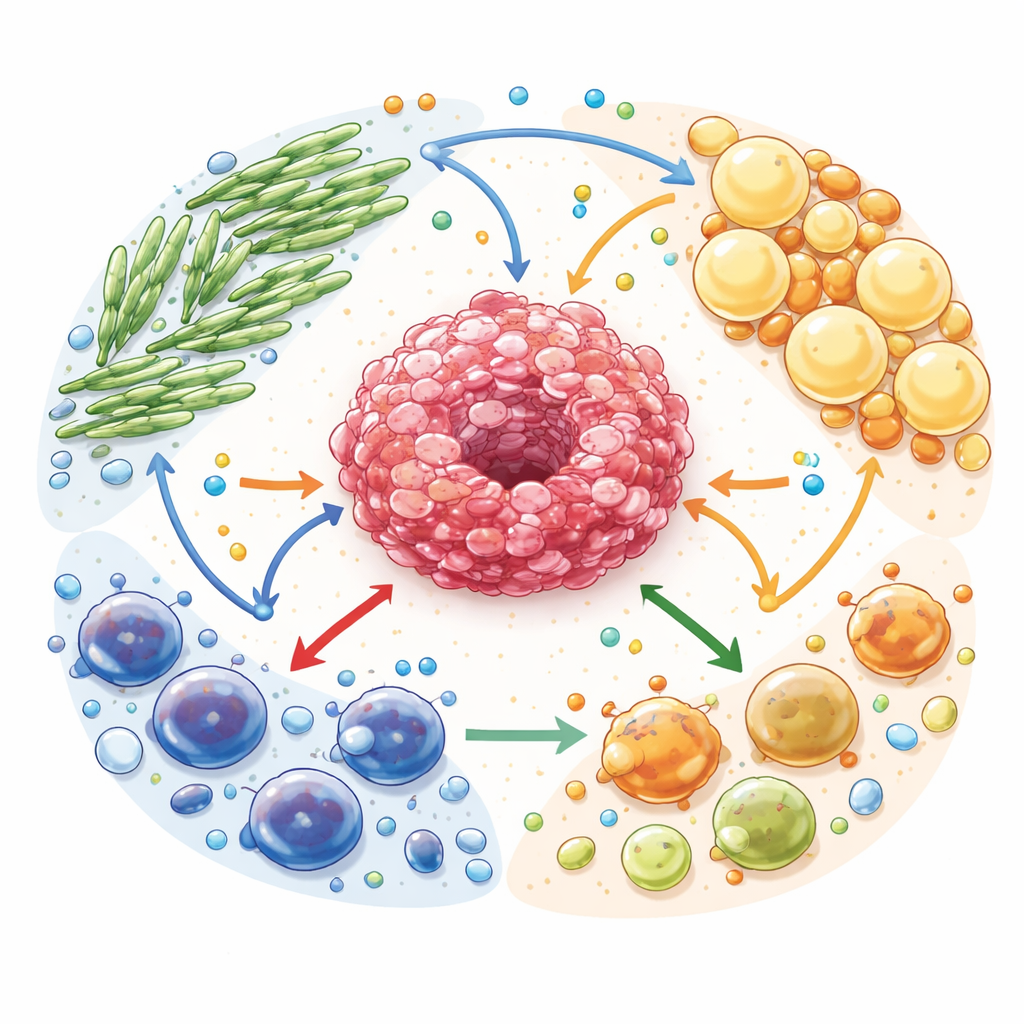
癌症生态系统中的燃料共享
作者将肿瘤微环境描述为一个复杂的生态系统。癌细胞被与癌相关的成纤维细胞(类瘢痕支持细胞)、与癌相关的脂肪细胞(被重编程的脂肪细胞)和多种免疫细胞所包围。所有这些细胞既竞争又交换葡萄糖、脂肪酸和氨基酸等燃料。但这种交易并非中性:支持细胞被重编程以分解自身储备并外排富含能量的分子来供养癌细胞。与此同时,乳酸和腺苷等类垃圾的代谢产物积累,作为强有力的信号削弱保护性免疫细胞,同时偏向那些抑制免疫攻击的细胞。
脂肪细胞如何帮助肿瘤并阻碍防御
邻近的脂肪组织远不止储存热量那么简单。在肿瘤信号和低氧的影响下,普通脂肪细胞会转变为与癌相关的脂肪细胞。它们缩小脂滴、加速脂解并释放游离脂肪酸、炎性分子和小型含货囊泡。癌细胞贪婪地摄取这些脂质并在其线粒体中燃烧,获得一种灵活且持久的能量来源,帮助其在应激、转移和耐药中存活。脂肪富集区域的免疫细胞则状况不佳:杀伤性T细胞和自然杀伤细胞脂质负荷过重,遭受氧化应激,进入“衰竭”状态,摧毁肿瘤细胞的能力受损。相反,调节性T细胞和某些髓系细胞则以这些脂质为养分,变得更加免疫抑制,进一步压制免疫反应。
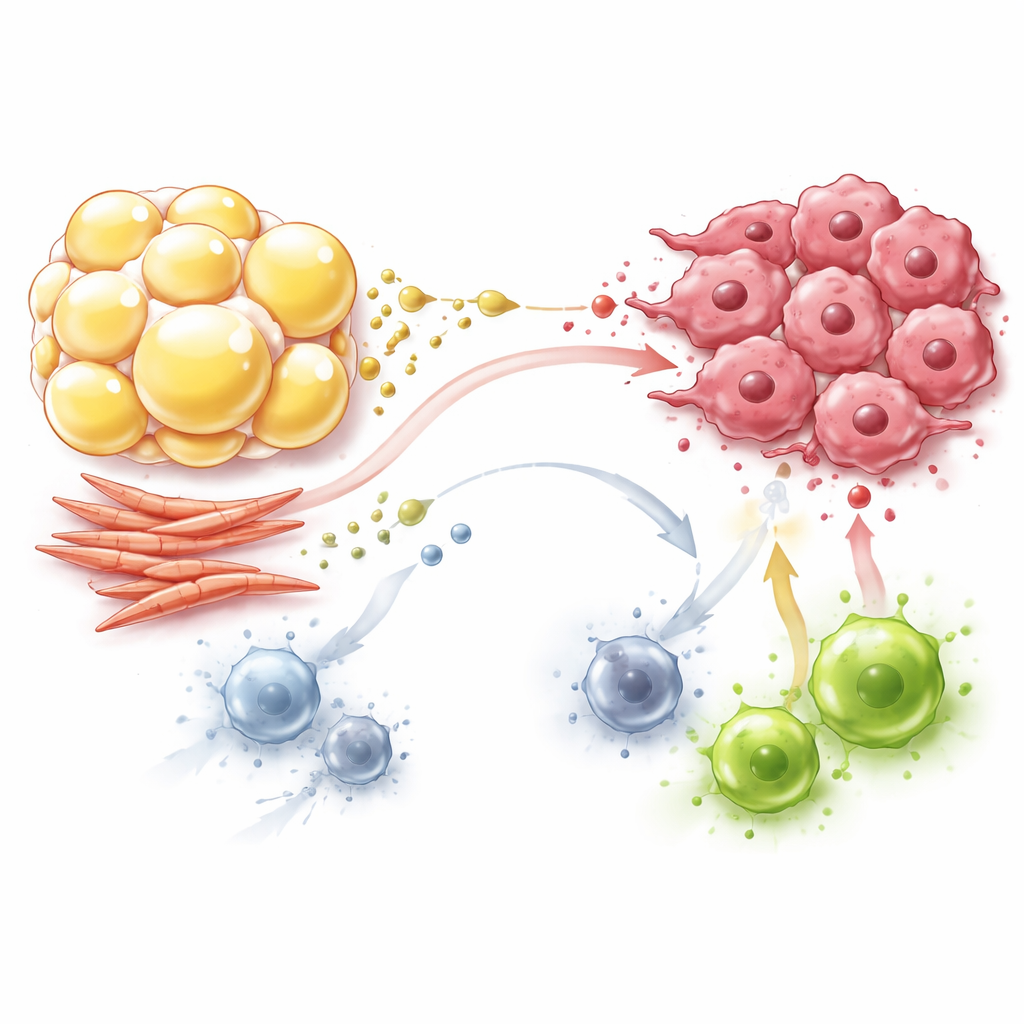
成纤维细胞:作为构建者也重编程代谢
成纤维细胞长期以来被视为环绕肿瘤的类瘢痕组织的构建者,但它们也是这一代谢戏码中的积极参与者。与癌相关的成纤维细胞趋向于糖类嗜好型行为,即在有氧条件下也将大量葡萄糖转化为乳酸和丙酮酸。它们将这些产物输出到周围空间,癌细胞再将其回收用作自身能量工厂的燃料,从而节省葡萄糖用于生长。成纤维细胞还合成并交换谷氨酰胺、脯氨酸和天冬氨酸等氨基酸,这些物质既支持肿瘤的结构又帮助其在营养应激下生长。与此同时,成纤维细胞消耗关键营养并释放乳酸,挤压了依赖葡萄糖的效应性T细胞,并推动巨噬细胞与T细胞走向更具耐受性、较少攻击性的状态。
陷入代谢陷阱的免疫细胞
肿瘤内的免疫系统受燃料可得性影响之深不亚于抗原。需要快速糖代谢以驱动攻击的细胞毒性T细胞和自然杀伤细胞,发现自己处在被剥夺葡萄糖并被乳酸、脂质及其他抑制性代谢物淹没的环境中。它们的动力系统停滞,线粒体受损,表面抑制性“刹车”增加。与此同时,调节性T细胞和与肿瘤相关的巨噬细胞适应这种严酷环境。它们偏好脂肪氧化和氧化代谢,使其在他人失败之处得以繁荣。在成纤维细胞和脂肪细胞的支持下,这些细胞强化了一种耐受性、类似伤口愈合的状态,保护肿瘤并削弱免疫检查点抑制剂和其他免疫疗法的疗效。
将代谢转化为治疗靶点
综述强调了一套不断扩展的实验性药物工具箱,旨在扰动这一支持网络,而不是单纯毒杀分裂的细胞。一些方法旨在阻断脂肪细胞释放脂质或阻止癌细胞对脂质的摄取与燃烧。另一些则针对成纤维细胞驱动的通路,这些通路产生乳酸、重塑基质或招募抑制性髓系细胞。通过降低乳酸水平、阻断特定燃料转运蛋白或重编程细胞内的脂质感知开关,这些策略旨在恢复耗尽的T细胞和自然杀伤细胞对葡萄糖的获取和线粒体健康。最终目标不仅是饿死肿瘤,还是“再教育”其邻里,使免疫细胞重新识别、到达并有效攻击癌细胞。
引用: Kim, T.H., Lim, S.H., Lee, H. et al. Metabolic crosstalk among cancer-associated fibroblasts, adipocytes and immune cells as an immunosuppressive tumor microenvironment driver. Exp Mol Med 58, 366–381 (2026). https://doi.org/10.1038/s12276-026-01650-1
关键词: 肿瘤微环境, 癌症代谢, 与癌相关的成纤维细胞, 与癌相关的脂肪细胞, 肿瘤免疫抑制