Clear Sky Science · zh
外泌体复合体组分 Exoc5 缺失加剧肾脏纤维化进展
为什么肾脏瘢痕很重要
慢性肾脏病影响全球数亿人,其进展的主要原因之一是纤维化——工作性肾组织被缓慢替换为瘢痕组织。本研究考察了一个较少为人知的细胞“机械”,外泌体复合体及其组成部分 Exoc5,试图回答一个实用问题:这种蛋白是在肾脏受损后帮助其整洁修复,还是推动其走向瘢痕和衰竭?
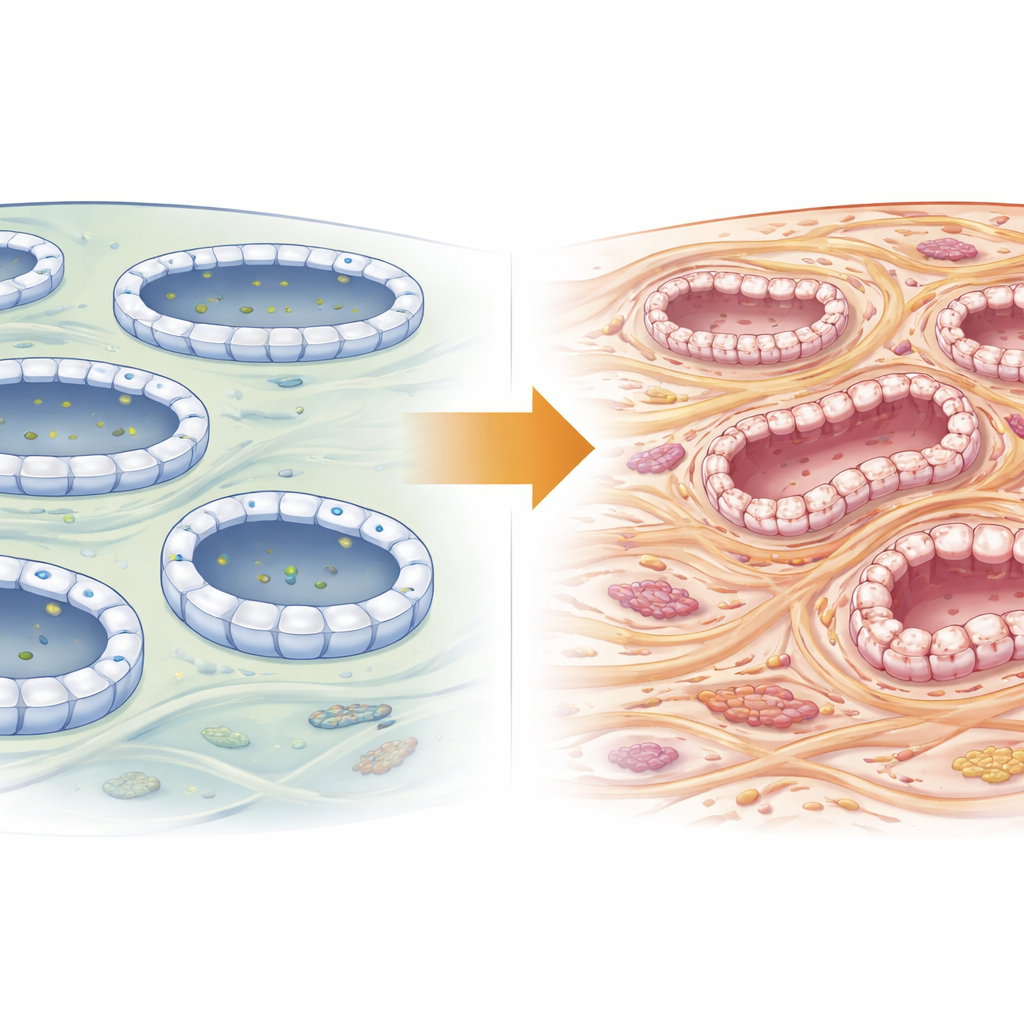
肾小管细胞中的细胞级运输枢纽
每个肾小管细胞都是一个繁忙的物流中心,不断将装有货物的小泡运送到细胞表面的精确位置。这种运输由外泌体复合体组织——一个由八个部分组成的对接复合体。Exoc5 位于该机器的核心,连接来自细胞内的货物与外膜上的对接位点。早期研究表明破坏 Exoc5 会损害多种器官,并且它有助于肾小管细胞维持紧密、有序的结构。由于结构破坏是纤维化的标志,作者怀疑 Exoc5 可能在受损肾脏是恢复还是瘢痕化的抉择中发挥作用。
在小鼠肾脏中检验 Exoc5 的作用
研究人员构建了仅在近曲小管细胞中删除 Exoc5 的小鼠模型——这些段负责大部分肾脏的滤过和重吸收。出人意料的是,这些小鼠在日常条件下生长正常,肾脏结构、运输蛋白定位和功能也无异常。为了模拟常导致瘢痕化的强烈局部损伤,团队对一侧输尿管进行结扎,这是一个标准处理,会在一周内导致受累肾脏的压力积聚、炎症和纤维化。在正常小鼠和缺失 Exoc5 的小鼠中,阻塞均降低了 Exoc5 水平,但敲除动物出现了更严重的小管萎缩、胶原沉积及炎症相关细胞的浸润。
从有序的小管到游走的细胞
健康的小管细胞紧密相连,具有明确的上下极性。在纤维化过程中,它们常经历“上皮—间质转化”(EMT),从固定的片状状态转变为更加可移动、产生纤维的状态。作者发现,在阻塞后,缺失 Exoc5 的肾脏表现出关键 EMT 驱动因子的更强激活以及更高水平的迁移性、产纤维细胞典型蛋白,同时失去维持小管细胞极性的连接蛋白也更为显著。他们还观察到 Pax2(一种在肾小管成熟后通常关闭的发育调控因子)重新出现,在 Exoc5 缺失的小管中尤为明显,尤其出现在那些无法成功分裂的受压细胞中,提示 Exoc5 的缺失使细胞更容易进入一种半修复的、去分化的状态,易于形成瘢痕。
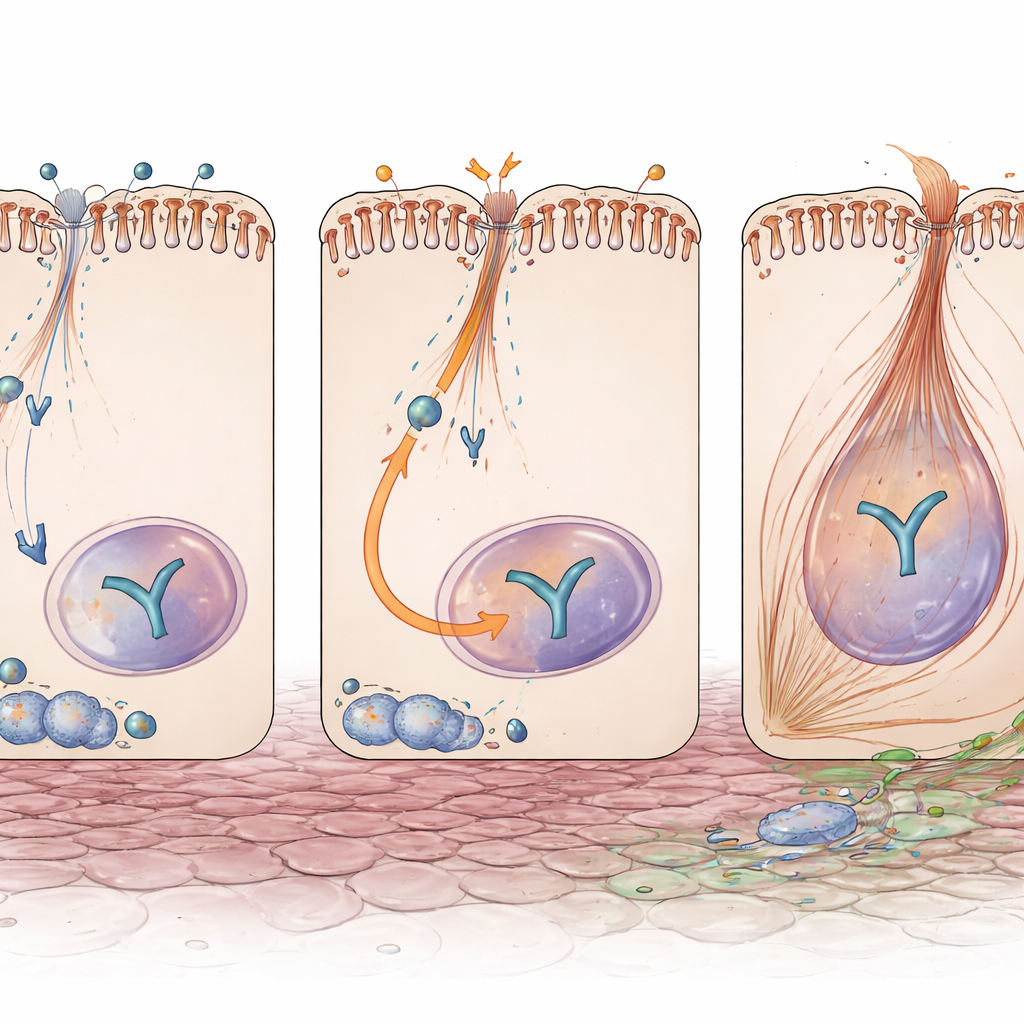
将损伤与瘢痕信号相连的开关
另一个在纤维化中处于核心地位的因子是 YAP,一种对信号作出反应的蛋白,会进入细胞核激活与生长和基质生成相关的基因。即使在未受伤情况下,缺失 Exoc5 的小管中也检测到更高的 YAP 蛋白水平。阻塞后,这些肾脏中 YAP 的激活更强、在细胞核中的富集更明显,其下游产物——已知驱动纤维化重塑的分子——也升高。重要的是,这种变化并非来自 YAP 基因表达的增加,暗示 Exoc5 正常情况下在蛋白或运输水平上对 YAP 有抑制作用。在培养的人肾小管细胞中,使用 RNA 干扰降低 EXOC5 会提升 YAP 和 Pax2,并使细胞对促纤维化信号 TGF-β 的反应更强,表现出更明显的类似 EMT 的变化以及更多细胞获得肌成纤维细胞典型的收缩性纤维。
这对未来治疗意味着什么
综合来看,这些发现将 Exoc5 描绘为一名沉默的守护者:在压力下,它帮助小管细胞维持有序的身份,并抑制诸如 YAP 和 Pax2 之类的促瘢痕信号。当 Exoc5 水平下降——无论是通过基因丧失还是损伤——小管细胞更容易丧失极性、滑入一种类似发育的状态,从而促进纤维化进程。由于在健康条件下在近曲小管中删除 Exoc5 并未损害肾脏,但在受伤后明显加重瘢痕化,这项工作将 Exoc5 及其信号伙伴指向了作为延缓或逆转肾脏纤维化、阻止其进展至肾衰竭的潜在治疗靶点。
引用: Lim, H.J., Han, Y.K., Noh, M.R. et al. Deficiency of exocyst complex component Exoc5 exacerbates the progression of kidney fibrosis. Exp Mol Med 58, 681–695 (2026). https://doi.org/10.1038/s12276-026-01649-8
关键词: 肾脏纤维化, Exoc5, 上皮—间质转化, YAP 信号, 慢性肾脏病