Clear Sky Science · zh
补充L-天冬氨酸通过抑制血小板—肝细胞相互作用介导的线粒体断裂(经ATP–P2X7–NEK7–DRP1轴)纠正小鼠MASLD和MASH
这项肝脏研究为何重要
许多人体内肝脏储存着额外脂肪却浑然不知。这一隐匿性问题现在被称为代谢功能障碍相关性脂肪肝(MASLD),可进展为严重炎症、瘢痕甚至肝癌。本文总结的研究探讨了一种简单的天然氨基酸L-天冬氨酸是否能在小鼠中保护肝脏,并揭示了肝损伤中的一个意外元凶:过度活化的血小板损伤肝细胞的“动力工厂”——线粒体。
现代生活中常见的肝脏问题
MASLD与肥胖和2型糖尿病密切相关,可能很快影响全球超过三分之一的人口。在MASLD中,肝细胞被脂肪充盈、处于应激并开始死亡,从而触发炎症和瘢痕形成。健康的线粒体通常燃烧脂肪和糖以产生能量,但在该病中它们受损并断裂,导致肝脏燃脂减少、脂肪积累增加。尽管问题规模巨大,目前仅有一种药物获批且仅对部分患者有效,研究者因此在寻找能恢复肝脏能量机制的安全、可负担的治疗方法。
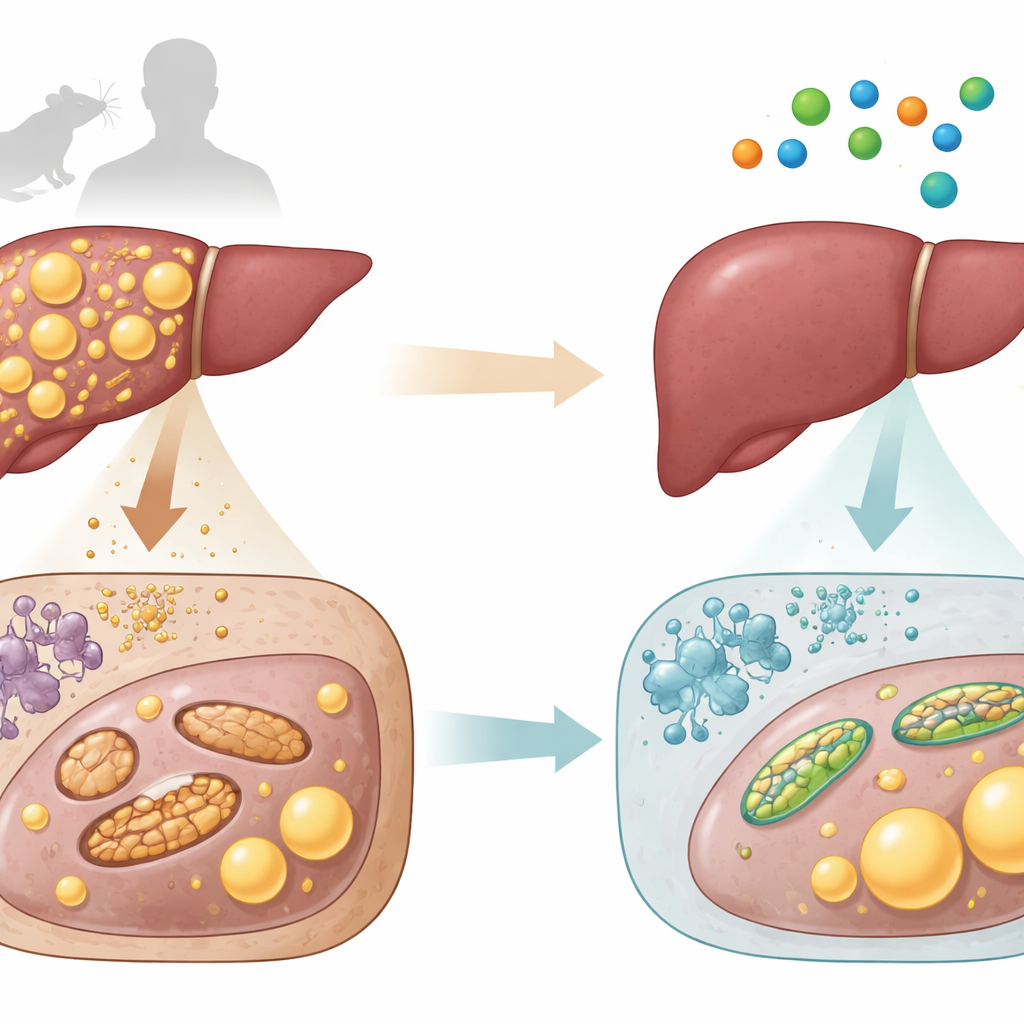
一种简单氨基酸的潜在助力
L-天冬氨酸是构成蛋白质的小分子,同时参与体内能量循环,并已在临床上作为肝脏支持剂使用。研究者首先测定了小鼠和人类的血液与肝组织中L-天冬氨酸的含量。他们发现,肝脏更肥、受损更严重的动物和人,肝组织中的L-天冬氨酸水平一致较低。在两种物种中,L-天冬氨酸越少,脂肪含量越高,肝损伤信号越强。该模式提示L-天冬氨酸下降可能与肝脏健康恶化并行。
在小鼠中逆转脂肪肝与炎症
研究团队接着探问补充L-天冬氨酸是否真的能修复疾病。他们给小鼠饲喂高脂高胆固醇饮食或一种诱发严重肝脏炎症和瘢痕的特殊饮食,模拟人类的MASLD及其晚期MASH。当这些小鼠接受与临床可比剂量的L-天冬氨酸注射时,肝脏变得更轻、更少油腻,血液中的肝酶下降,显微镜检查显示脂滴减少、炎症减轻、瘢痕减少。这些益处在早期脂肪肝和晚期炎性疾病中均有体现,并在相同模型中与已知参考药物效果相当。
保护细胞的“动力工厂”
在肝脏细胞内观察时,病变小鼠的线粒体数量减少,许多线粒体肿大、受损或碎成微小断片。L-天冬氨酸治疗恢复了更健康的延长型线粒体网络。它增强了关键产能酶复合体的活性,提高了线粒体的耗氧量和ATP产出,并增加了线粒体“清理”和更新的标志物。整只动物的测量显示耗氧量和能量消耗增加,表明小鼠总体在燃烧更多燃料,而不仅仅是因为进食减少。
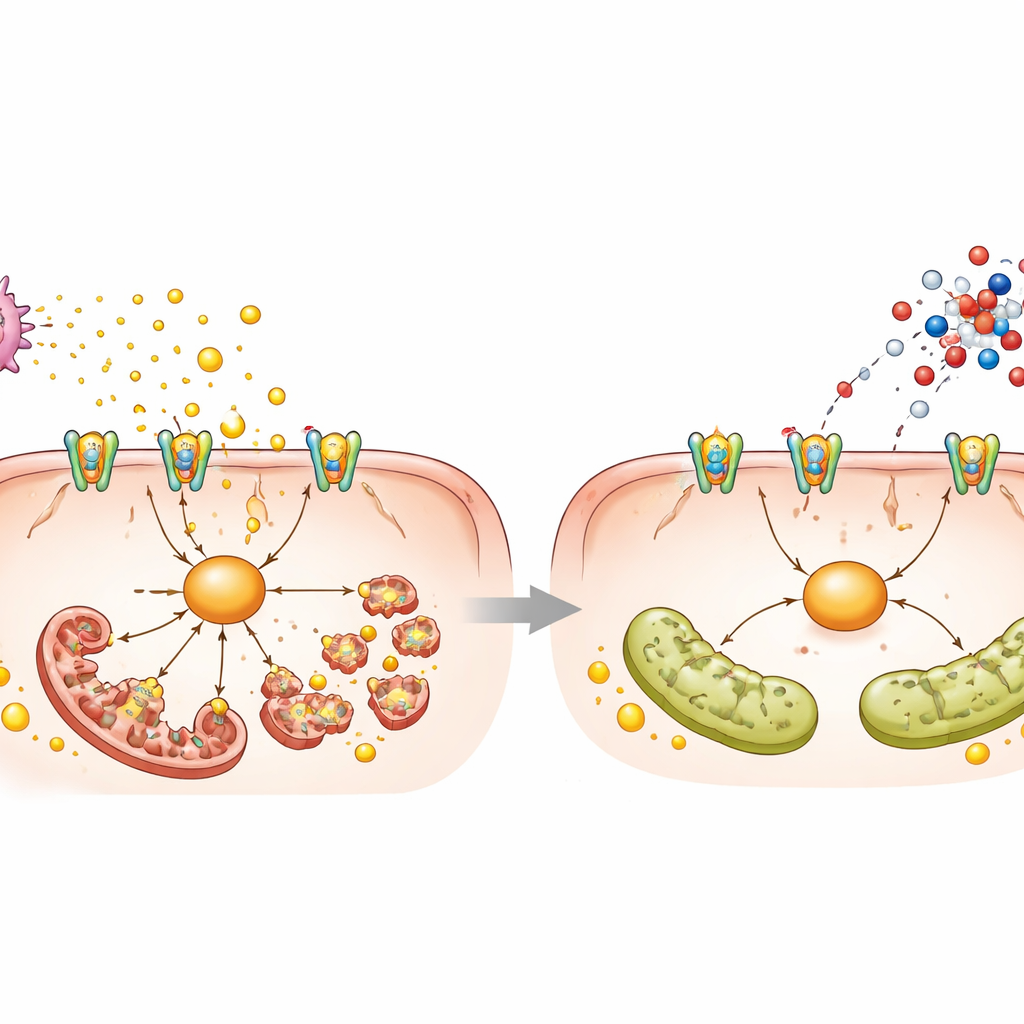
血小板、有毒信号与分子链路
为了解L-天冬氨酸如何发挥这些作用,研究者在单次给药后结合基因表达和代谢物分析。一条意外信号浮现:与血小板激活和信使分子cGMP相关的通路。在脂肪肝中,血液和肝脏中的血小板数量增多且被激活,它们释放额外的ATP——一种正常的能量分子,但当被释放到细胞外时会变得有害。该ATP激活了肝细胞上的P2X7受体,进而开启了NEK7蛋白和裂变蛋白DRP1,驱动线粒体断裂并促进脂肪堆积与细胞死亡。L-天冬氨酸提高了血小板内cGMP水平,抑制了其激活和聚集,减少ATP释放并抑制了肝细胞内的P2X7–NEK7–DRP1链。直接用阿司匹林阻断血小板、抑制P2X7或敲低NEK7可模拟L-天冬氨酸的许多保护作用,支持血小板—肝脏串话是损伤核心的观点。
这对患者可能意味着什么
综上,这些发现表明在脂肪肝疾病中,过度活化的血小板向肝脏释放大量ATP,引发一系列分子级连锁反应,摧毁线粒体并加重脂肪积累和损伤。在小鼠中,补充L-天冬氨酸打破了这一循环:它使血小板更平静、限制ATP释放、维持线粒体形态与功能,并逆转了单纯脂肪肝和炎性纤维化疾病。由于L-天冬氨酸成本低且已作为肝脏支持剂使用,该研究将其作为在人体MASLD和MASH中值得测试的有前景候选物,同时也将血小板驱动的线粒体损伤指出为未来治疗的新靶点。
引用: Cao, WJ., Su, R., Fu, HL. et al. Supplementation of L-aspartate corrects MASLD and MASH in mice by inhibiting platelet–hepatocyte interaction-mediated mitochondrial fragmentation via the ATP–P2X7–NEK7–DRP1 axis. Exp Mol Med 58, 533–547 (2026). https://doi.org/10.1038/s12276-026-01648-9
关键词: 脂肪性肝病, 血小板, 线粒体, L-天冬氨酸, 代谢性肝病