Clear Sky Science · zh
与小胶质细胞相关的多发性硬化进展:在人体体外模型中识别靶点与治疗干预
为何大脑免疫细胞在多发性硬化中重要
多发性硬化(MS)常被描述为身体免疫系统攻击大脑和脊髓的疾病。许多现有药物能有效减少急性发作(复发),但无法阻止许多患者多年间缓慢、无声的病情恶化。本文综述说明常驻于大脑的小型免疫细胞——小胶质细胞——如何可能驱动这种长期衰退,以及人类体外生长的大脑模型如何帮助科学家发现能够真正减缓或阻止进展的治疗方法。
持续损伤的隐秘引擎
传统上,MS 被分为复发型和进行性两类,但现有证据显示,进展几乎在所有患者体内很早就已开始,即便他们表面上仍只表现为复发。复发由来自血液的免疫细胞进入中枢神经系统所驱动,而进展似乎由被困在大脑和脊髓内部的炎症维持。在这一封闭环境中,小胶质细胞参与多种有害过程:持续炎症、白质与灰质神经纤维上绝缘性髓鞘的丧失、有害活性氧化物的积累以及修复失败。最终结果是神经元及其连接的逐步丧失。小胶质细胞在正常情况下通过清除碎片并支持神经细胞来维持大脑健康,但在 MS 中它们常转向更具攻击性的状态并丧失部分保护功能,使其成为推动进展的主要嫌疑者。
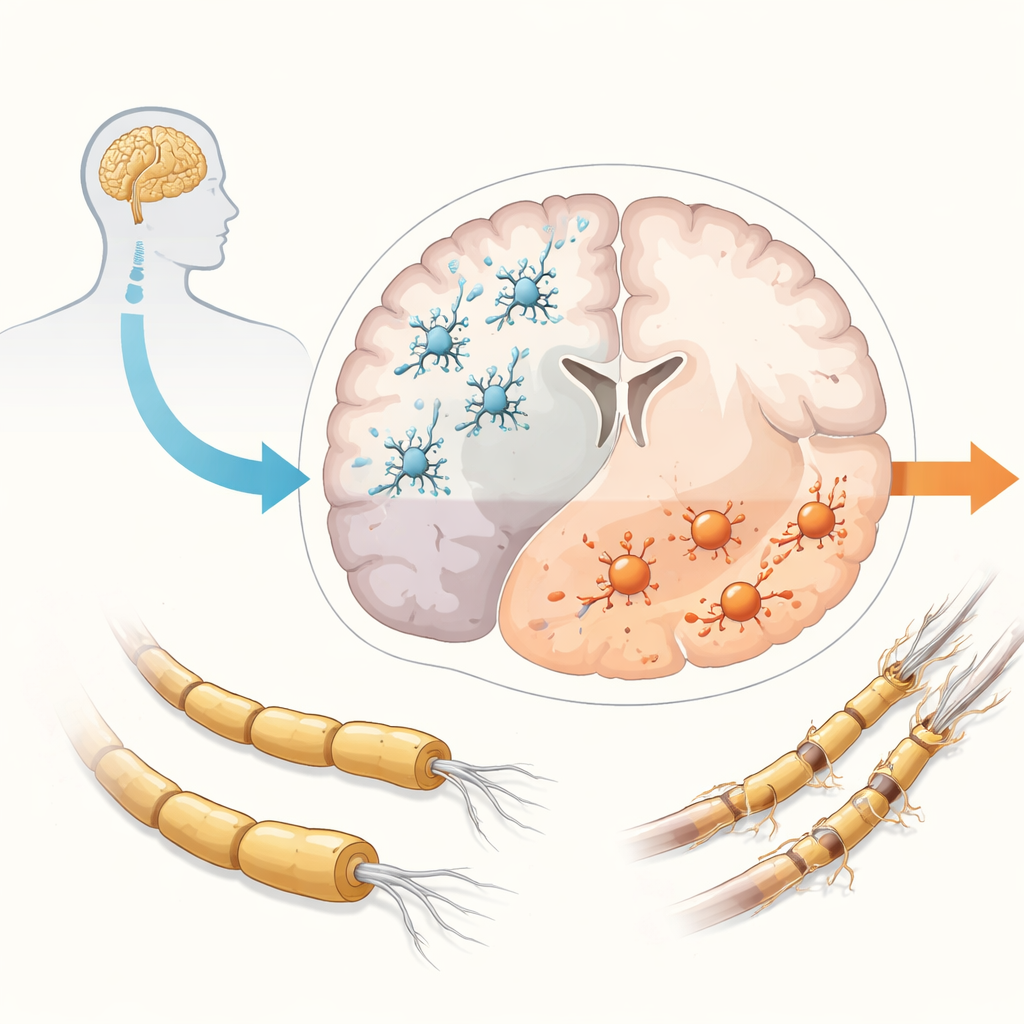
传统动物模型的局限
几十年来,小鼠及其他动物的研究对开发减少复发的药物至关重要,但这些模型在开发能阻止进展的治疗方面基本失败。原因之一在于动物模型只能部分模拟人类 MS,不能完全再现患者大脑中那种复杂且长期存在的炎症。啮齿类动物的小胶质细胞在重要基因和反应上也与人类有差异。因此,在动物中看似有效的治疗往往在人类身上无效。缺乏能真实反映进行性 MS 的动物模型,促使研究者建立新的以人为本的实验室系统,以便更直接地研究小胶质细胞和其他脑细胞。
在培养皿中构建人类大脑模型
科学家现在使用多层次的实验室模型来研究人类小胶质细胞。直接从啮齿类或人类脑组织获得的原代细胞保留许多天然特征,但难以获取、在离开原生环境后迅速变化且不易放大规模。为克服这些障碍,研究者转向诱导多能干(iPS)细胞——将成体细胞重编程为灵活的类干细胞状态。这些 iPS 细胞可被引导分化为小胶质细胞、神经元或其他脑细胞。在简单的二维培养中,iPS 衍生的小胶质细胞能呈现许多关键特征并可大量生产,从而支持精细实验和药物筛选。它们甚至可以从个体 MS 患者体细胞生成,揭示内在差异,例如基因活性改变以及对压力和碎片清除反应的变化。
加入更真实的大脑“邻里”
由于小胶质细胞的行为受周围环境强烈影响,研究者已超越单层细胞培养,转向更逼真的构建方式。在二维共培养中,小胶质细胞与神经元及支持细胞共同生长,有助于它们呈现更自然的形态与行为,并使科学家能够研究细胞类型间的相互影响。三维球体和类器官——微小的自组织脑样组织——更进一步,提供一个柔软、拥挤的环境,更接近真实的脑组织。当小胶质细胞嵌入这些结构中时,它们显示复杂分支形态、对损伤作出反应、与类似血脑屏障的层相互作用,并对来自 MS 患者脑脊液的炎性信号产生反应。这类模型被用于研究慢性炎症如何在小胶质细胞和星形胶质细胞中触发一种“疲惫但发炎”的状态(即细胞衰老),以及小胶质细胞脂质处理的改变如何可能损害髓鞘修复。同时,将人源 iPS 衍生的小胶质细胞或类器官移植入小鼠大脑,允许这些细胞在活体网络中进一步成熟,并在已建立的类 MS 疾病模型中进行测试。
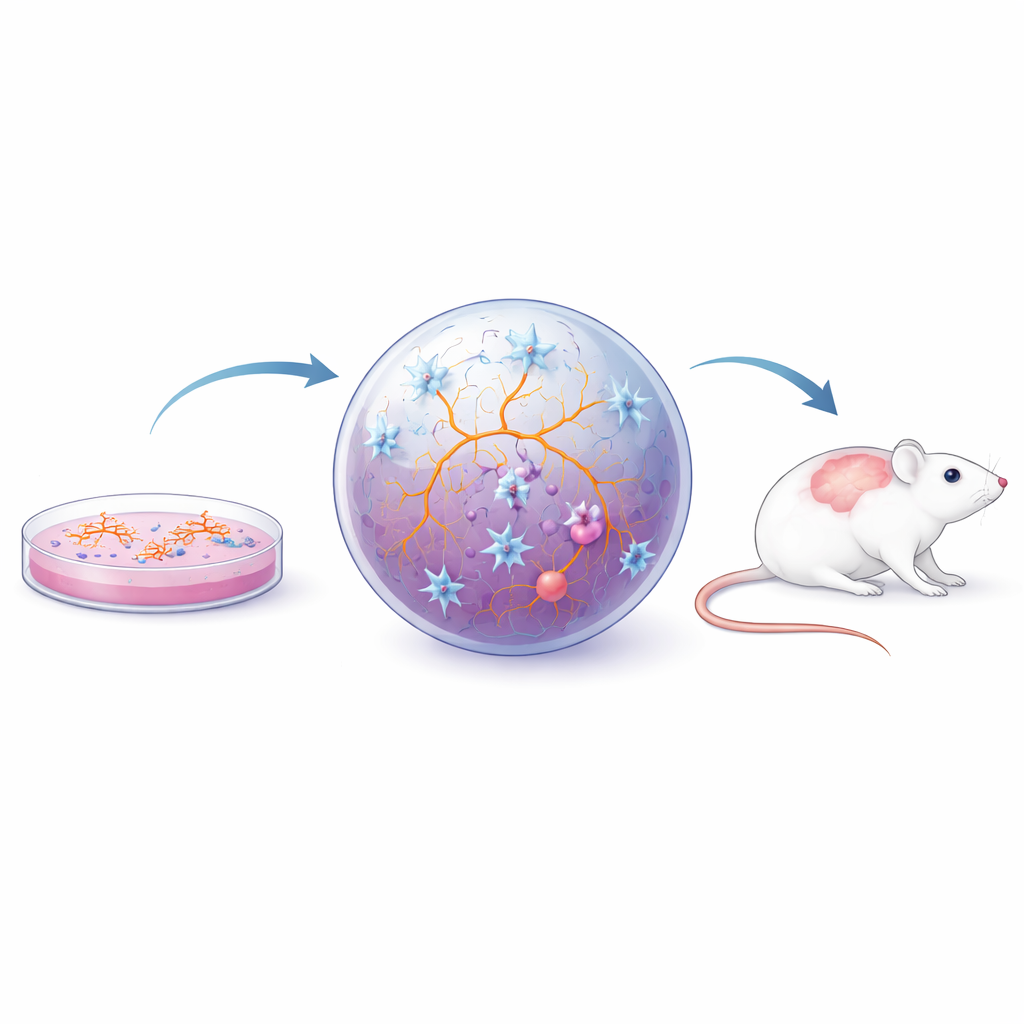
从实验室模型走向未来治疗
总体而言,这些以人为基础的体外和嵌合模型构成了一套工具箱,可用于剖析小胶质细胞如何促进 MS 进展,并测试旨在抑制有害小胶质细胞活性同时恢复其保护功能的新疗法。尽管没有任何模型能完全再现人脑,但每种模型都捕捉到了不同的关键环节,合在一起弥补了简单细胞培养与不完美动物模型之间的鸿沟。通过整合这些系统的见解,研究者希望识别精确的药物靶点——例如控制炎症、类衰老变化和小胶质细胞脂质代谢的通路——从而最终转化为能减缓或阻止进行性 MS 所致逐步残疾的治疗方法。
引用: Blenkle, A., Geladaris, A. & Weber, M.S. Microglia-associated progression of multiple sclerosis: target identification and therapeutic engagement in human in vitro models. Exp Mol Med 58, 357–365 (2026). https://doi.org/10.1038/s12276-026-01647-w
关键词: 多发性硬化 进展, 小胶质细胞, 诱导多能干细胞, 脑类器官, 神经炎症