Clear Sky Science · zh
ESRP1/circPHGDH/miR-149/RAP1B 正反馈回路促进前列腺癌细胞的恶性行为和糖酵解
这项研究为何与男性健康相关
前列腺癌是男性中最常见的癌症之一,许多肿瘤最终会变得更具侵袭性并对治疗产生耐药性。本研究揭示了前列腺癌细胞内一个隐藏的控制回路,该回路帮助肿瘤更快生长、更易转移,并重编程其利用糖作为能量的方式。通过描绘这一分子环路,研究人员指出了潜在的薄弱环节,可能成为放慢疾病进程或增强现有疗法效果的新靶点。
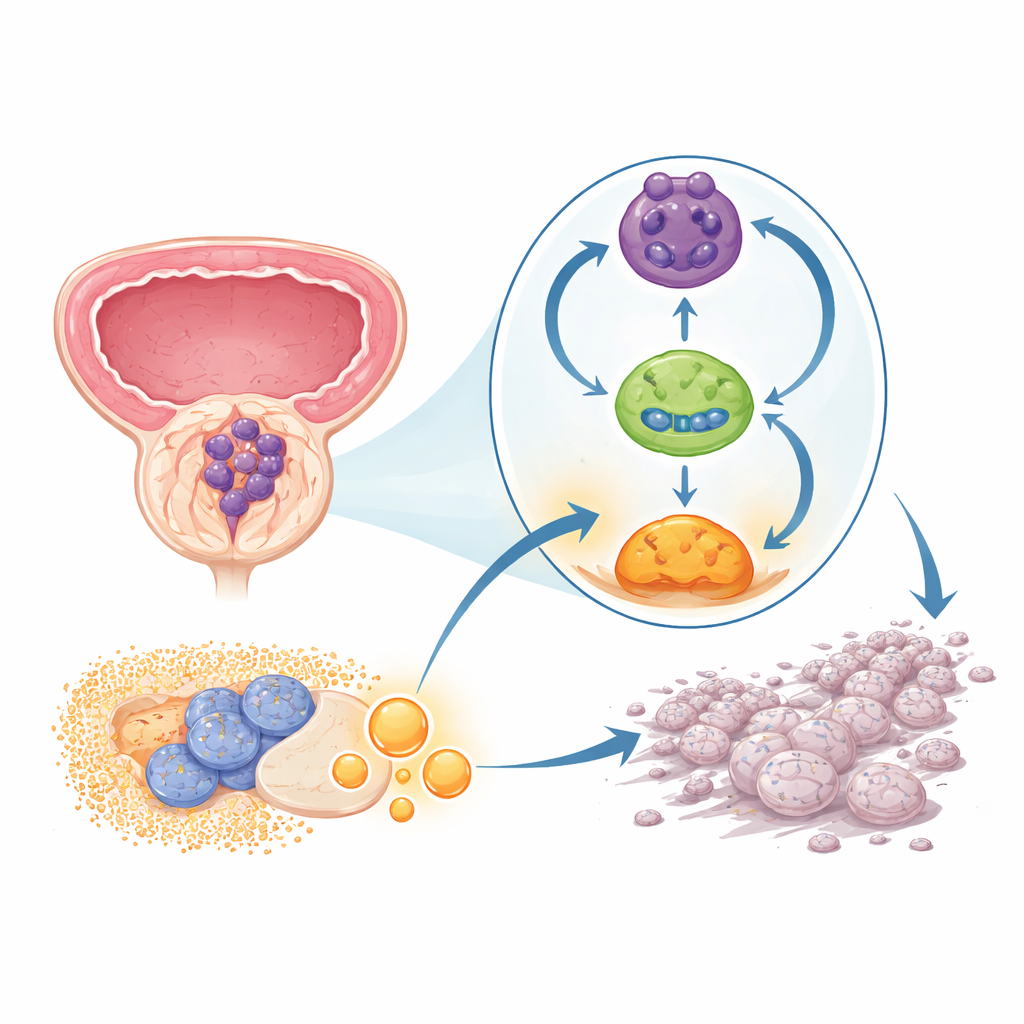
维持癌症活性的隐藏回路
研究组关注一种新近受到重视的遗传物质类型——环状 RNA。与常见的线性 RNA 不同,这类分子形成闭合环状,且非常稳定。在前列腺肿瘤样本和细胞系中,研究人员发现一种名为 circPHGDH 的环状 RNA 水平持续高于邻近的非癌组织。肿瘤中该 RNA 含量较高的患者往往伴随肿瘤体积更大、局部生长更晚期以及远处转移,提示 circPHGDH 可能促成疾病更危险的表型。
癌细胞如何改变其行为
为弄清 circPHGDH 的功能,科学家在体外培养的前列腺癌细胞中调节了该分子的水平。降低 circPHGDH 时,细胞形成的克隆减少,迁移和侵袭能力下降,并显示出更多“上皮型”特征,这种状态不易扩散。与此同时,细胞从许多肿瘤常见的嗜糖代谢方式转向较多依赖有氧能量生成:对糖酵解的依赖降低。有针对性地提高 circPHGDH 则使这些促进肿瘤的性状朝相反方向变化。
小 RNA 与生长信号传导
研究随后追踪 circPHGDH 如何发挥作用。在细胞液相中,circPHGDH 像一个“海绵”吸附一种称为 miR-149 的小型调控 RNA,阻止它抑制其常见靶点。一个关键靶点是 RAP1B,一种参与主要生长与生存通路的信号蛋白,已知在前列腺癌中很重要。当 circPHGDH 抑制了 miR-149 时,RAP1B 水平上升并激活下游信号,促进细胞分裂、迁移和以糖酵解为主的代谢。恢复 miR-149 或直接降低 RAP1B 能逆转许多有害效应,这在细胞培养和携带人体前列腺肿瘤的小鼠模型中均得到证实。
喂养火焰的代谢废物
故事的另一个层面涉及 circPHGDH 的产生机制。其生成依赖于一种称为 ESRP1 的剪接蛋白,ESRP1 决定原始 RNA 如何切割和重连。研究人员证明 ESRP1 与 circPHGDH 区域周围的特定位点结合,并偏好产生环状形式而非标准线性形式。关键的是,他们发现糖酵解的终产物乳酸可在 ESRP1 的单个位点上发生化学修饰,使该蛋白更稳定。由于 circPHGDH 本身促使细胞更多依赖糖酵解并产生更多乳酸,这就形成了一个自我增强的循环:ESRP1 提高 circPHGDH,circPHGDH 提升 RAP1B 与糖酵解,糖酵解产生乳酸,而乳酸反过来稳定 ESRP1。
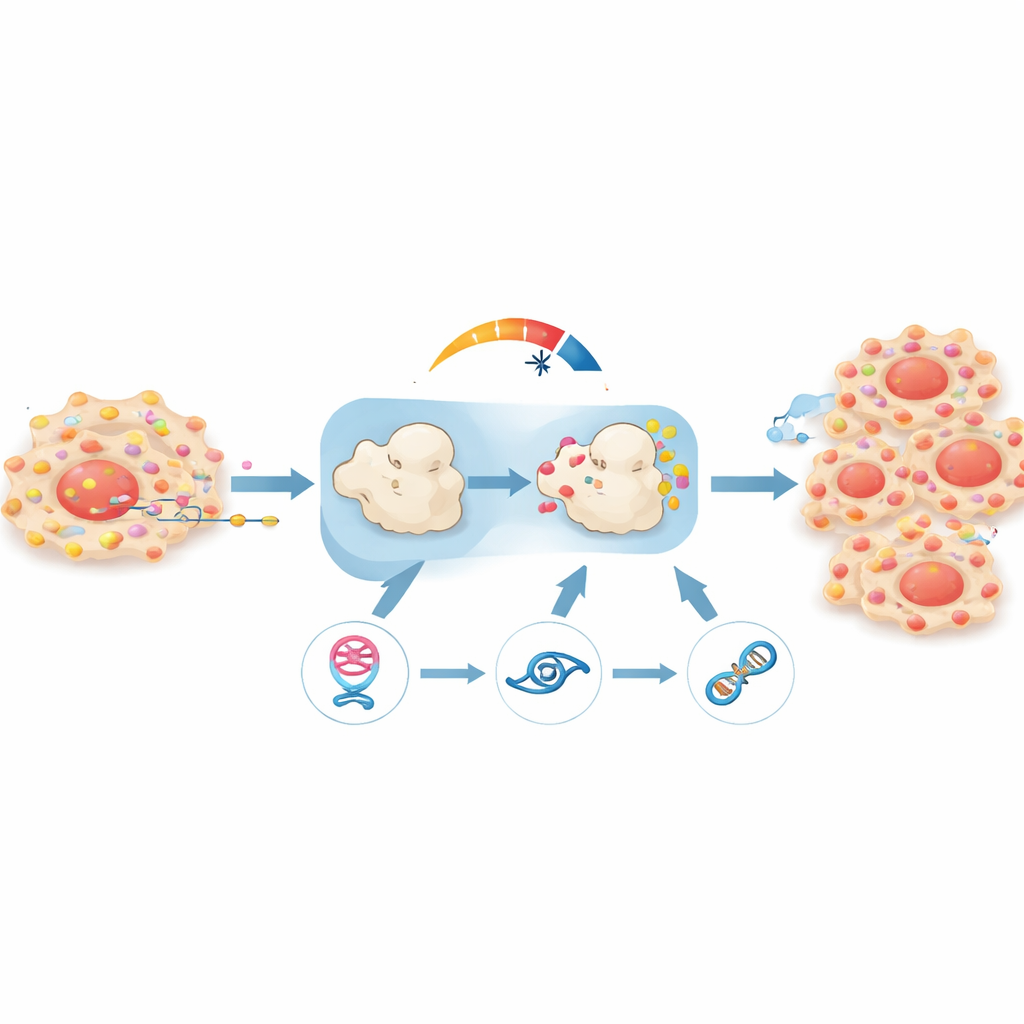
来自动物模型的证据
为验证这一回路在生物体内是否确实重要,研究组将人前列腺癌细胞移植入小鼠体内。被沉默 circPHGDH 的肿瘤生长更慢、重量更轻,且全身成像和组织分析显示转移迹象减少。细胞增殖标志物降低,显微镜下肿瘤组织结构也显得不那么侵袭性。当研究者在这些相同肿瘤中阻断 miR-149 或强制恢复 RAP1B 时,大部分生长与转移表型回归,确认了 circPHGDH–miR-149–RAP1B 链是驱动疾病行为的核心因素。
对未来治疗的意义
综上,这些发现揭示了一个正反馈回路:一种剪接蛋白、一个环状 RNA、一种小型调控 RNA 和一个信号蛋白协同作用,推动前列腺癌细胞走向快速生长、侵袭和嗜糖代谢。对于非专业读者,关键信息是癌细胞可以将其遗传和代谢控制接线成自我增强的电路,从而维持疾病进展。打破这一回路——通过干扰 circPHGDH、恢复 miR-149、阻断 RAP1B 或干预乳酸依赖的 ESRP1 修饰——为未来旨在减缓或阻止侵袭性前列腺癌的药物提供了若干有前景的途径。
引用: Wang, X., Yu, L., Qian, X. et al. A ESRP1/circPHGDH/miR-149/RAP1B positive feedback loop promotes the malignant behaviors and glycolysis of prostate cancer cell. Exp Mol Med 58, 622–635 (2026). https://doi.org/10.1038/s12276-026-01646-x
关键词: 前列腺癌, 环状 RNA, 肿瘤代谢, 微小 RNA, 信号通路