Clear Sky Science · zh
PAK4 与代谢性疾病:营养信号的调控及治疗学意义
为何细胞开关对日常健康至关重要
肥胖、2 型糖尿病和脂肪肝常被归咎于热量摄入,但在细胞内部,分子开关决定我们是燃烧还是储存能量。本文综述聚焦于其中一种开关——一种名为 PAK4 的蛋白,阐明它如何响应不断变化的营养与激素信号,重塑脂肪、肝脏与肌肉的代谢。理解这一隐蔽的控制系统,或能打开新治疗策略的大门,这类策略可同时应对多种代谢疾病,而非逐一处理症状。 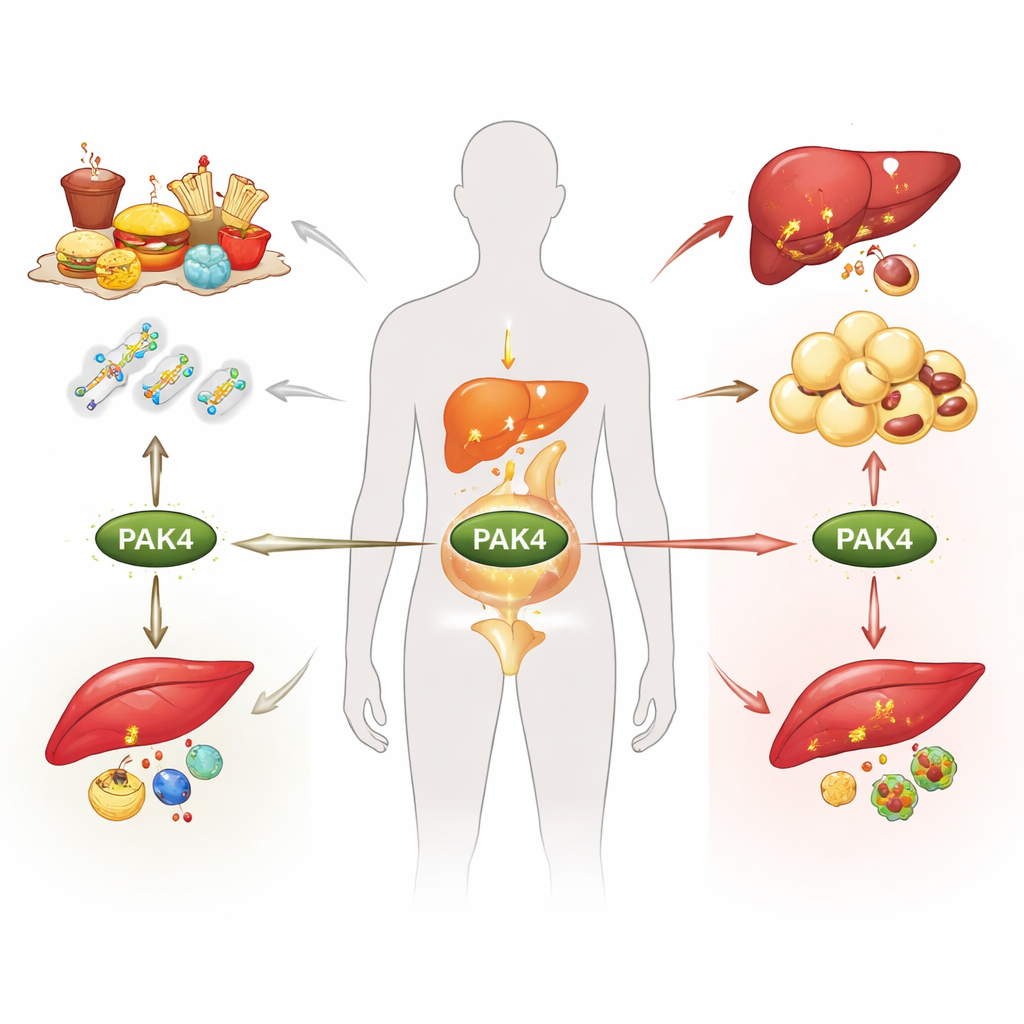
藏在细胞里的主控开关
PAK4 属于一类将细胞内小分子“信使”传递的酶。在健康状态下,PAK4 在主要代谢器官中保持低表达。当能量平衡被打破,例如在肥胖或 2 型糖尿病时,其在脂肪组织、肝脏和骨骼肌中的水平会升高。PAK4 的活性受多重机制控制:上游信号改变其构象,蛋白翻译后又可被添加或去除各种化学标记。这些包括可激活或标记其降解的磷酸化修饰,以及影响其稳定性或活性的其它标记。禁食、进食、激素和压力都会影响这些修饰,因此 PAK4 实际上“感知”机体的营养状态,并将信息传递给关键代谢通路。
PAK4 如何使脂肪细胞偏向储存
在脂肪细胞中,PAK4 起到抑制脂肪分解的刹车作用。通常在禁食或应激激素升高时,另一种酶 PKA 会触发对储存于小脂滴中的脂肪的受控分解。综述描述了 PAK4 如何通过将抑制性磷酸化直接添加到激素敏感性脂肪酶和一种参与脂肪分子运输的脂肪酸结合蛋白上来对抗这一过程。这些改变削弱了释放储存脂肪的机制。PAK4 还通过帮助细胞周期蛋白推动前体细胞向成熟储脂细胞分化,从而在早期支持新脂肪细胞的形成。在动物模型中,去除或抑制 PAK4 会使脂肪细胞燃烧更多燃料,表现出增加能量消耗的“褐化”特征,并使动物免受饮食诱导的体重增加影响。 
PAK4 在脂肪肝与肌肉糖代谢中的作用
在肝脏中,PAK4 同样偏向于促进储存而非燃烧。在禁食或生酮饮食期间,PAK4 水平下降,使肝细胞能够增强脂肪分解和酮体生成,这些产物为其它组织提供能量,甚至可能减缓肿瘤生长。当 PAK4 丰富时,它会对一个核内共抑制子蛋白进行磷酸化修饰,使其抑制 PPARα——这一脂肪氧化与酮体生成的主调控因子。其结果是更多脂肪滞留在肝脏中,血液中的保护性酮体减少。在骨骼肌中,PAK4 干扰 AMPK(一个促进糖摄取和线粒体活性的核心能量感受器)。PAK4 通过以阻断其激活的方式修饰 AMPK,减少肌细胞表面的葡萄糖转运蛋白数量,从而助长胰岛素抵抗。在小鼠的肌肉特异性 PAK4 缺失模型中,这些效应被逆转,即使在肥胖条件下也能改善血糖控制。
压力、防护与与其它细胞开关的关联
综述还强调了 PAK4 在日常代谢之外的影响。在器官如肝脏发生血流减少随后的再灌注等情形时,PAK4 通过标记并使 Nrf2(对抗氧化应激的关键保护因子)不稳定化,削弱了抗氧化防御。与此同时,家族中的另一成员 PAK1 常在心肌、骨骼肌和胰腺的胰岛素分泌细胞中发挥更为支持性的作用,帮助维持正常的葡萄糖处理。这种在代谢疾病中有害的 PAK4 信号与通常有益的 PAK1 功能之间的对比,强调了开发高度选择性药物的必要性,以在抑制 PAK4 的同时不干扰对心脏和内分泌健康必不可少的相关蛋白。
将发现转化为治疗
由于 PAK4 在癌症和代谢紊乱中均表现为过度活跃,药物设计者既在研发抑制其活性的低分子化合物,也在开发能将 PAK4 本身标记以促其降解的新型“降解剂”药物。早期阻断 PAK4 的化合物显示出抗肿瘤潜力,但在特异性和体内药代性质方面遇到挑战。更近期更精确靶向 PAK4 的分子在肥胖小鼠中产生了显著结果:体重下降而进食量并未减少,肝脏更健康,肌肉更活跃,血糖控制改善。降解剂通过物理消除 PAK4 更进一步,早期动物研究表明它们可能能保护肌肉免于萎缩并对某些癌症起到防护作用。综合这些发现,抑低 PAK4 活性有望同时缓解肥胖、糖尿病与脂肪肝,使这一曾经鲜为人知的细胞开关成为未来代谢疗法的有前景靶点。
引用: Bang, I.H., Park, BH. & Bae, E.J. PAK4 in metabolic diseases: regulation by nutrient signals and therapeutic implications. Exp Mol Med 58, 416–424 (2026). https://doi.org/10.1038/s12276-026-01645-y
关键词: PAK4, 代谢性疾病, 肥胖, 脂肪肝, 胰岛素抵抗