Clear Sky Science · zh
氧化还原敏感蛋白 HMGB1:细胞内与细胞外的作用
为何这种会变形的蛋白对健康至关重要
在你体内几乎每个细胞中都存在一种名为 HMGB1 的小蛋白,它的行为有点像多功能工具。在平稳状态下,它默默地协助组织 DNA。但当细胞遭受应激或损伤时,HMGB1 可从细胞核移动,进入周围组织,并作为免疫系统的警报信号。本文综述解释了由氧化驱动的微小化学改变如何将 HMGB1 转变为完全不同的生物学“人格”——既能保护组织,也能引发炎症,甚至助长慢性疾病。理解这种分子“情绪环”可能开辟新的途径,在不完全抑制免疫系统的情况下平息过度炎症。
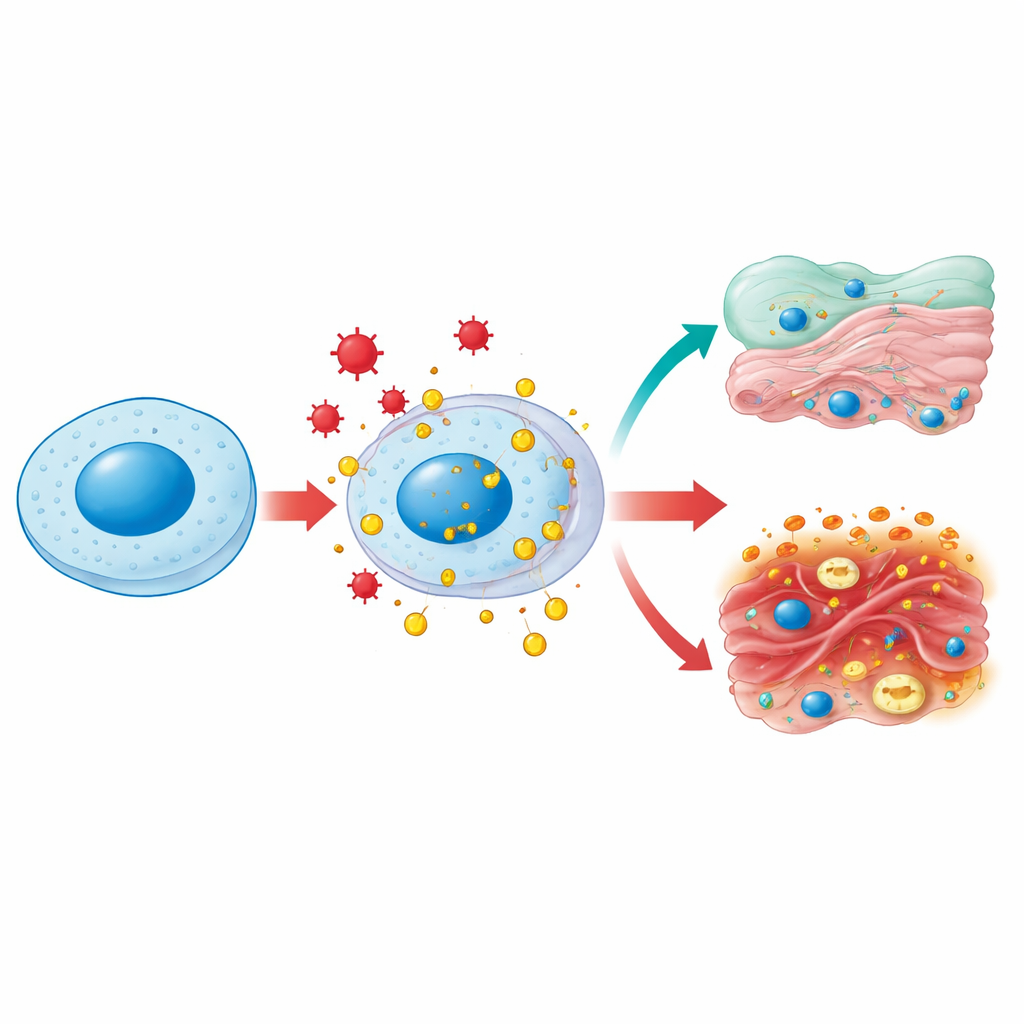
一蛋白,多重场所
HMGB1 通常位于细胞核内,弯曲并放松 DNA 以便基因被复制和修复。在感染、高血糖或毒性损伤等应激下,它可以被化学修饰并被护送到细胞的液相内环境,随后释放到细胞外。在细胞质中,HMGB1 通过促进一种称为自噬的清理过程并防止线粒体过度断裂,帮助维持线粒体这一“细胞动力站”的健康。被释放到细胞外后,HMGB1 成为典型的“危险信号”——免疫细胞将其识别为组织受损的标志并迅速聚集。因而同一分子依其所在位置及化学调谐状态,在细胞内部承担家务角色,在细胞外则充当报警角色。
氧化如何改写其行为
本综述的核心是氧化——由活性氧(ROS)驱动的反应——如何重塑 HMGB1。该蛋白含有三个带硫的氨基酸残基,可充当微小开关。在全还原态时,HMGB1 倾向支持细胞存活并招募修复细胞。轻度氧化可在同一分子内将其中两个位点连接形成“二硫键”构象,这种形式特别善于与细胞表面的免疫受体(如 Toll 样受体和 RAGE)结合,从而强烈刺激炎症介质的产生。更强的氧化应激会将分子推进更高氧化态,使其无法有效结合 DNA 或受体;这种“烧坏”型变体在免疫学上变得沉默,并与炎症的消退阶段以及不引发免疫攻击的细胞死亡程序相关联。
从细胞死亡信号到疾病推动者
HMGB1 与多种细胞死亡方式紧密交织。在剧烈的细胞死亡形式如坏死、程序性坏死(necroptosis)、铁死亡(ferroptosis)和焦亡(pyroptosis)期间,HMGB1 会泄漏或被主动转运出细胞,并携带反映周围氧化环境的氧化还原特征。在坏死早期,它往往处于还原形式,而持续的应激会把它推向更氧化的状态。释放到细胞外后,还原型 HMGB1 可促进某些癌细胞的保护性自噬,帮助其在化疗下存活;而富含二硫键和二聚体的形式则放大炎症级联和补体激活,可能加重组织损伤。HMGB1 还可反向促进某些死亡通路——例如与细菌脂质协同触发程序性坏死,或在中风后推动脑支持细胞的铁依赖性死亡。由此,HMGB1 既标示又调节组织中的生死平衡。
与炎症、自身免疫和癌症的关联
由于其行为对氧化非常敏感,不同 HMGB1 变体在各种疾病中呈现出不同模式。富含二硫键的 HMGB1 与慢性炎症密切相关:它出现在类风湿关节炎的炎性关节、纤维化肝、肺损伤、手术后的缺血再灌注损伤以及脓毒症中——在脓毒症患者中其血液水平与病情严重程度和死亡风险相关。相比之下,还原型 HMGB1 常与细胞迁移和组织重塑相关,如心脏成纤维细胞或单核细胞在趋化因子 CXCL12 的引导下的迁移。过度氧化且免疫上沉默的 HMGB1 则富集于晚期凋亡等情境,在这些情况下机体希望清除濒死细胞而不引发攻击。在肿瘤中,二硫键型支持抑制性、利于肿瘤生长的免疫环境,而阻断 HMGB1 可缩小肿瘤并提高检查点免疫疗法的效果。
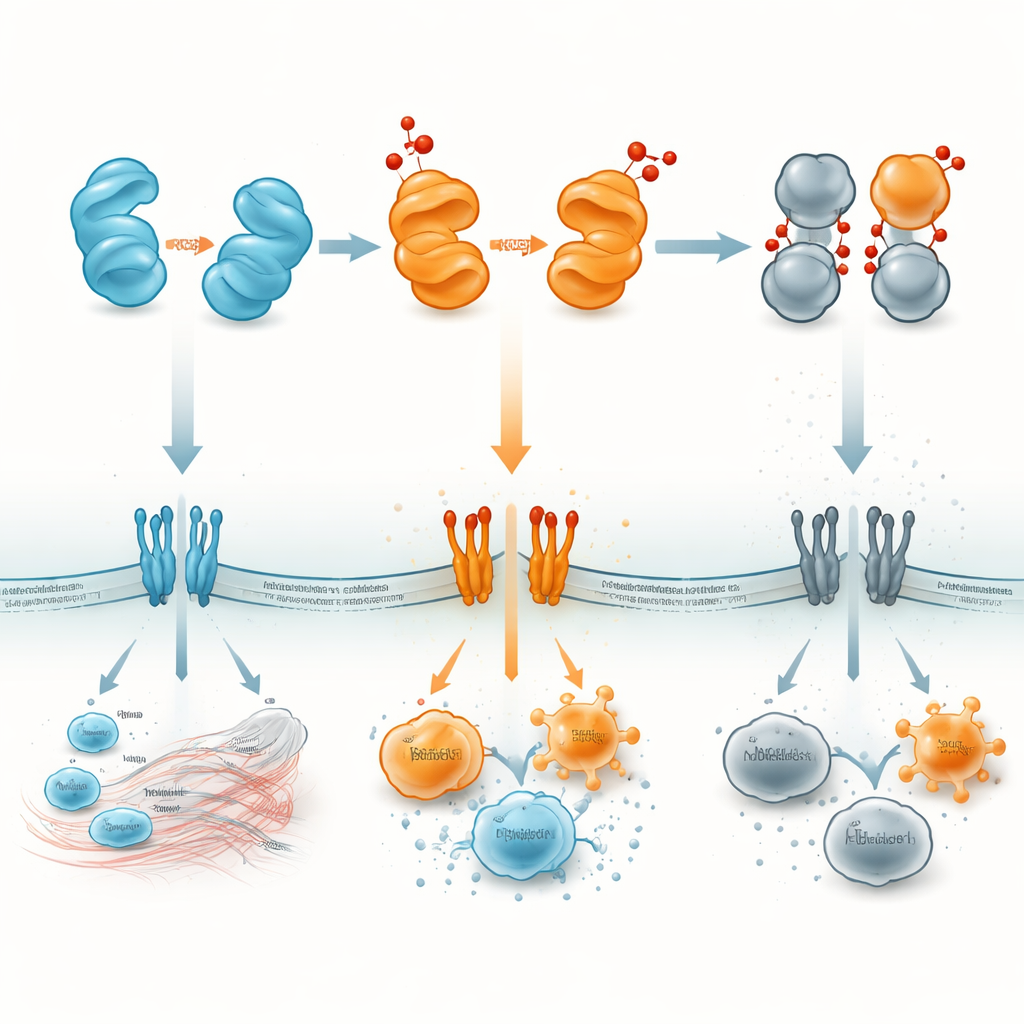
将分子警报转化为治疗靶点
对外行人而言,HMGB1 可被视为一个小型蛋白质警报器,其响度和信息随着化学状态而改变。还原型 HMGB1 倾向召集修复队伍;二硫键和二聚体形式会发出强烈警报,助长有害炎症;而完全氧化的形式则几乎沉默,帮助炎症消退。通过绘制各版本出现的时间与地点——在细胞核内、细胞质中、血液中或特定器官内——研究者希望设计出能阻断有害形式或稳定有益形式的药物。这类策略可能使临床医生在治疗脓毒症、自身免疫、中风、肺损伤或癌症时,不仅靶向 HMGB1 本身,还能调控控制该蛋白如何向免疫系统“发声”的氧化还原“调光开关”。
引用: Kwak, M.S., Jung, S.F., Park, I.H. et al. The redox-sensitive protein HMGB1: intracellular and extracellular roles. Exp Mol Med 58, 345–356 (2026). https://doi.org/10.1038/s12276-026-01640-3
关键词: HMGB1, 炎症, 氧化应激, 细胞死亡, 自身免疫性疾病