Clear Sky Science · zh
通过T细胞受体的机械传导:共识、争议与未来展望
免疫细胞如何“感知”其周围世界
我们的免疫系统不仅能侦测化学信号,还能感知物理力。这篇综述探讨了T细胞——寻找病毒和癌细胞的白细胞——如何可能利用表面受体上的微小推拉来决定是否发动攻击。在分子尺度上理解这种“触觉”可能会重塑我们对疫苗、癌症免疫疗法和自身免疫疾病的看法。
T细胞受体的特殊职责
故事的核心是T细胞受体,这是位于T细胞表面的分子机器,用于检查其他细胞展示的蛋白片段。当找到合适的片段时,T细胞可以迅速激活、增殖并消灭受感染或癌变的靶细胞。该受体必须满足一系列苛刻要求:对极少量的外来片段做出反应、在大量无害的自身片段中保持忽略、在T细胞巡逻全身时迅速工作,并且在每个人体内应对数百万种不同的受体变体。细胞内经典的信号通路——涉及蛋白激酶、支架蛋白和转录因子——已被较为清晰地描绘。但仍然不解的是最初的一步:表面结合一个片段这一简单动作如何把受体从静默状态切换为活化状态。
关于第一个火花的不同观点
研究者提出了若干模型来解释T细胞受体如何首先被激活。一种观点认为,当受体被聚集到小簇中时,局部浓度提高,使信号反应更有效率,从而启动信号传导。另一种观点强调构象变化:结合可能会扭曲或放松受体复合体的某些部位,使细胞内被埋藏的片段暴露出来,从而让酶对其进行修饰。第三种模型强调细胞接触区的拥挤效应:短的受体—配体对会在紧密区域内堆积,物理性地排斥通常关闭信号的体积较大的酶,从而倾向于激活。每种模型都有实验支持并能解释部分现象,但单一模型都无法完全说明受体极高的敏感性及其区分高度相似蛋白片段的能力。
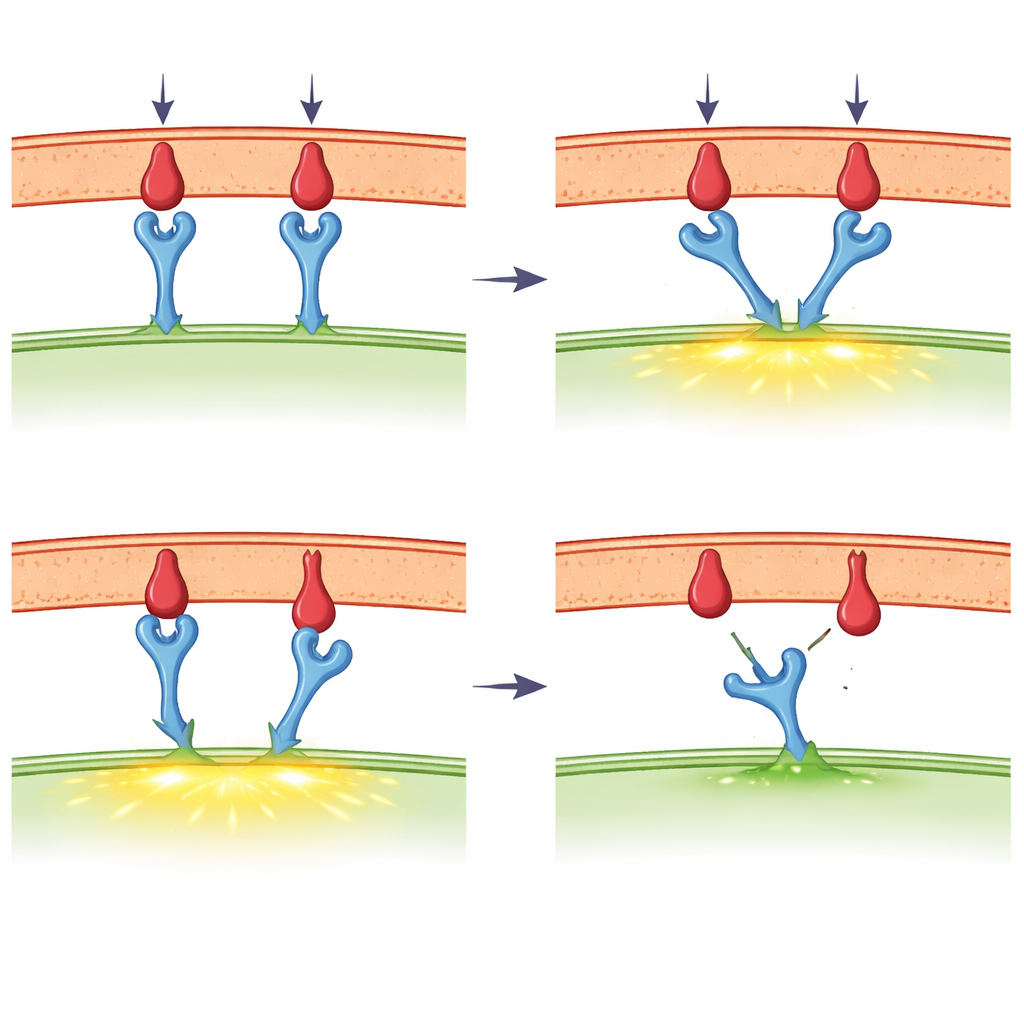
当触觉与力进入视野
该综述的一个重要焦点是新兴观点:T细胞受体表现为机械传感器——对力做出响应的装置。借助超高灵敏度的仪器,科学家们对单个受体—配体键施加了比苹果重量小万亿倍的力。他们发现,对于强效的外来片段,适度的拉力实际上可以延长键的寿命,这种行为被称为“抓取”(catch)响应。而较弱或自身的片段则表现为“滑脱”(slip)行为:在受力时更快解离。T细胞自身通过其由肌动蛋白丝和马达蛋白组成的细胞内骨架产生此类力,尤其集中在称为免疫突触的紧密接触区。新的分子张力探针显示,在T细胞早期激活期间确实存在与抓取行为相符的力范围,尽管不同的实验方法有时报告的数值不同,并因此引发了热烈讨论。
随时间区分自身与非自身
文章还重新审视了T细胞如何将噪声多、短暂的接触事件转化为可靠决策。长期以来的一个想法是动力学校对(kinetic proofreading),该理论认为信号通过一系列需要时间的步骤推进;只有能使受体持续结合足够久的片段,才能使级联达到不可逆的激活点。作者讨论了机械效应如何锐化这一时间过滤:拉力延长了有生产性的键的寿命并缩短了无效键的寿命,从而拉大了强刺激与弱刺激之间的差距。他们还考虑到T细胞可能整合多次短暂接触而非依赖单次长接触,以及信号网络内的反馈如何储存近期相遇的一种分子“记忆”。这些修正有助于解释T细胞在复杂组织环境中如何兼顾速度与准确性。
免疫受体之间的共同原则
尽管T细胞受体在其功能要求上显得异常严格,但许多设计原则在其他免疫受体中也能观察到。B细胞受体和先天免疫细胞上的抗体受体具有类似的信号模式,且常在紧密接触区运行,在这些区域拥挤、聚集和细胞骨架作用都很重要。对力的类似抓取响应已在若干此类受体—配体对中被报告。这提示感知机械线索可能是免疫系统用来检测靶标是否牢固固定、是否正确呈递以及是否值得响应的一般策略。
这对健康与治疗意味着什么
对普通读者来说,结论是T细胞不仅仅“嗅”到外来分子的存在——它们还会测试这些分子在被拉扯时的感觉。通过结合化学、物理与细胞生物学,这篇综述认为免疫受体将结合差异与力的细微差别转化为关乎细胞生死的决策。更深入理解这些机械生物学规则,可能会指导更优的T细胞疗法设计、更精确的疫苗以及通过改变受体的机械交互而非仅改变受体配体结合来调节免疫反应的新疗法。
引用: Travaglino, S., Jeon, Y., Kim, Y. et al. Mechanotransduction through T cell receptors: consensus, controversies and future outlooks. Exp Mol Med 58, 319–335 (2026). https://doi.org/10.1038/s12276-026-01639-w
关键词: T细胞受体, 机械传导, 抓取键(catch bonds), 免疫突触, 动力学校对