Clear Sky Science · zh
UBE2M:联结蛋白Neddylation与结直肠腺癌细胞周期调控的桥梁
这项研究为何对肠癌重要
结直肠癌是全球最常见且致死率高的癌症之一,主要原因在于肿瘤细胞学会无节制地分裂。该研究揭示了一个先前未被发现的控制开关,帮助结直肠癌细胞越过细胞分裂的关键检查点。通过阐明这一开关在分子层面的工作机制——并证明已有的一种抗真菌药物可干扰该过程——这项工作指出了一条可能减缓或阻止肿瘤生长的新途径。
肿瘤细胞内的隐秘调控层
细胞分裂并非随意进行;它遵循有序的周期,周期中设有检查点以确认复制DNA并分裂为两份是否安全。癌细胞常常篡改这些检查点。作者将注意力集中在一种称为neddylation的化学标记过程上,这一过程在蛋白质合成后会对其进行微妙修饰。早期研究提示neddylation在多种癌症中更为活跃,但其如何关联结直肠癌细胞的分裂周期尚不清楚。研究团队利用来自人类肿瘤的大型单细胞数据集以及来自1800多名患者的总体基因表达数据,发现neddylation活性在处于G2/M期——细胞分裂前的最后一道关口——的恶性肠细胞中特别高。
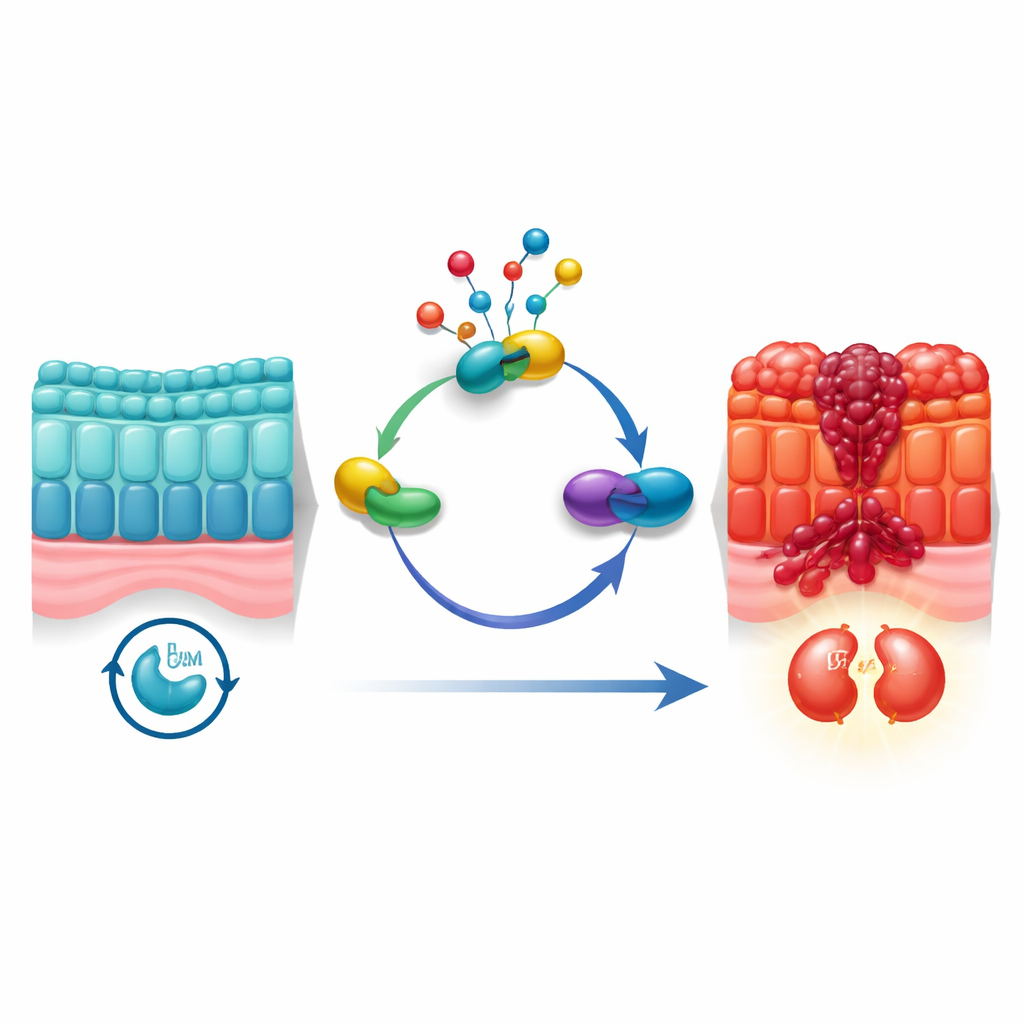
聚焦分子“桥梁”蛋白
为弄清哪些分子将neddylation与细胞分裂连接起来,研究者使用网络式的计算分析筛选数千个基因。一种蛋白脱颖而出:UBE2M,这是一种帮助将小型NEDD8标签附着到其他蛋白上的酶。数据中,UBE2M不仅与neddylation和细胞周期通路强相关,而且在结直肠肿瘤组织中的表达明显高于邻近正常组织。肿瘤中UBE2M含量较高的患者通常预后更差,提示它可能是驱动因子而非路人。当团队在癌细胞系和小鼠肿瘤模型中降低UBE2M表达时,肿瘤生长减慢、细胞分裂减少、程序性细胞死亡增加。相反,强制使细胞过表达UBE2M则加速了生长和细胞周期进程。
保护促生长关键蛋白的接力机制
进一步深入研究后,科学家们探究了UBE2M如何帮助细胞分裂。他们发现UBE2M并非单独行动,而是触发了一条涉及另外两个蛋白USP39和PABPC1的接力链。通常情况下,PABPC1会被一连串的泛素标签标记,送往细胞的蛋白质回收机器进行降解。团队证明,UBE2M通过NEDD8修饰USP39。这种修饰增强了USP39去除PABPC1上泛素链的能力,从而将PABPC1从降解中拯救出来并使其更稳定。PABPC1含量增加后,细胞在翻译特定信使RNA为蛋白质方面更高效,其中就包括编码CCNB1的mRNA——CCNB1是一种作为G2/M检查点“油门”的细胞周期蛋白。本质上,UBE2M通过稳定PABPC1进而提高CCNB1的生成,推动细胞更容易进入分裂。
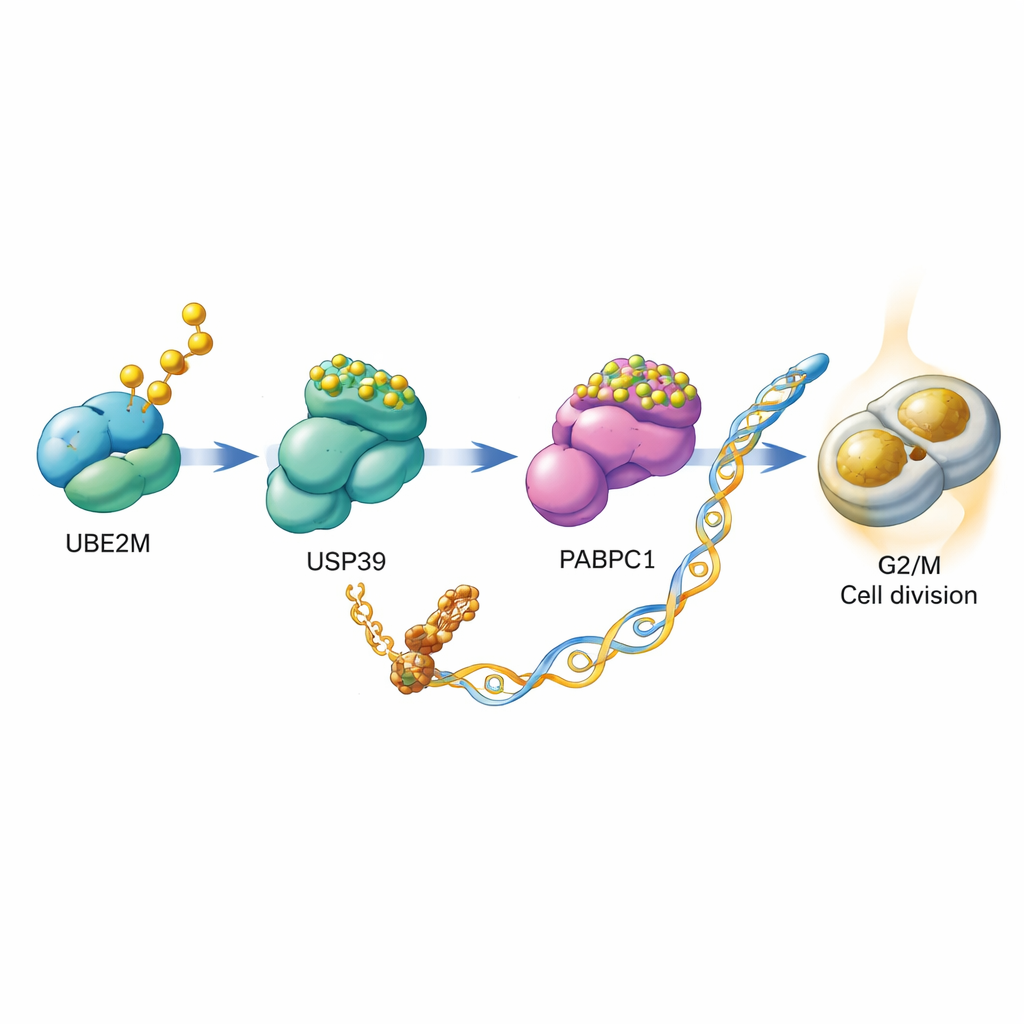
从分子机制到药物机会
发现UBE2M–USP39–PABPC1–CCNB1这一链条后,研究者看到了结直肠癌细胞的一个新脆弱点。作者转向米卡芬净(micafungin),这是一种已用于治疗真菌感染的药物,最近被鉴定为能抑制UBE2M的neddylation活性。在体外培养的肠癌细胞中,米卡芬净削弱了USP39的neddylation,增加了PABPC1的降解并降低了CCNB1蛋白水平。结果是细胞分裂变慢,更多细胞在G2/M检查点停滞,凋亡增加。在植入结直肠癌细胞的小鼠中,天天给药的米卡芬净显著缩小了肿瘤体积,相较于未治疗组效果明显,而无需直接去除UBE2M本身。
从长远看这对患者意味着什么
这项工作清晰地描绘了单一酶UBE2M如何将一种微妙的蛋白标记系统与肠癌细胞分裂决策连接起来。通过经由USP39稳定翻译因子PABPC1,UBE2M间接提高了强效细胞周期驱动因子CCNB1的水平,使肿瘤增速加快。尽管仍需更多研究与临床验证,但这些发现表明,通过阻断这一接力——例如借助像米卡芬净这样的药物再利用——可能为减缓结直肠癌进展并改善患者结局提供一种新的靶向策略。
引用: Wang, Z., Wang, Y., Chen, Y. et al. UBE2M as a bridge spanning neddylation and cell cycle regulation in colorectal adenocarcinoma. Exp Mol Med 58, 501–518 (2026). https://doi.org/10.1038/s12276-026-01636-z
关键词: 结直肠癌, 细胞周期, Neddylation, UBE2M, 靶向治疗