Clear Sky Science · zh
药物诱导的胃肠毒性与屏障完整性:临床相关的人体肠上皮模型中由细胞骨架介导的损伤
为何肠道副作用很重要
许多用于抗癌、抗炎或治疗其他疾病的药物可能无意中损害肠道黏膜。当这一肠道“内皮肤”受损时,患者可能出现腹泻、疼痛、恶心和营养吸收不良,有时严重到必须停止或降低救命疗法的剂量。然而,现有的实验室检测在药物进入临床前常常无法发现这些问题。本研究引入了一个更接近真实的人体肠道的体外模型,并展示了它如何更早识别损伤肠道的药物以及揭示这些药物削弱机体天然屏障的机制。
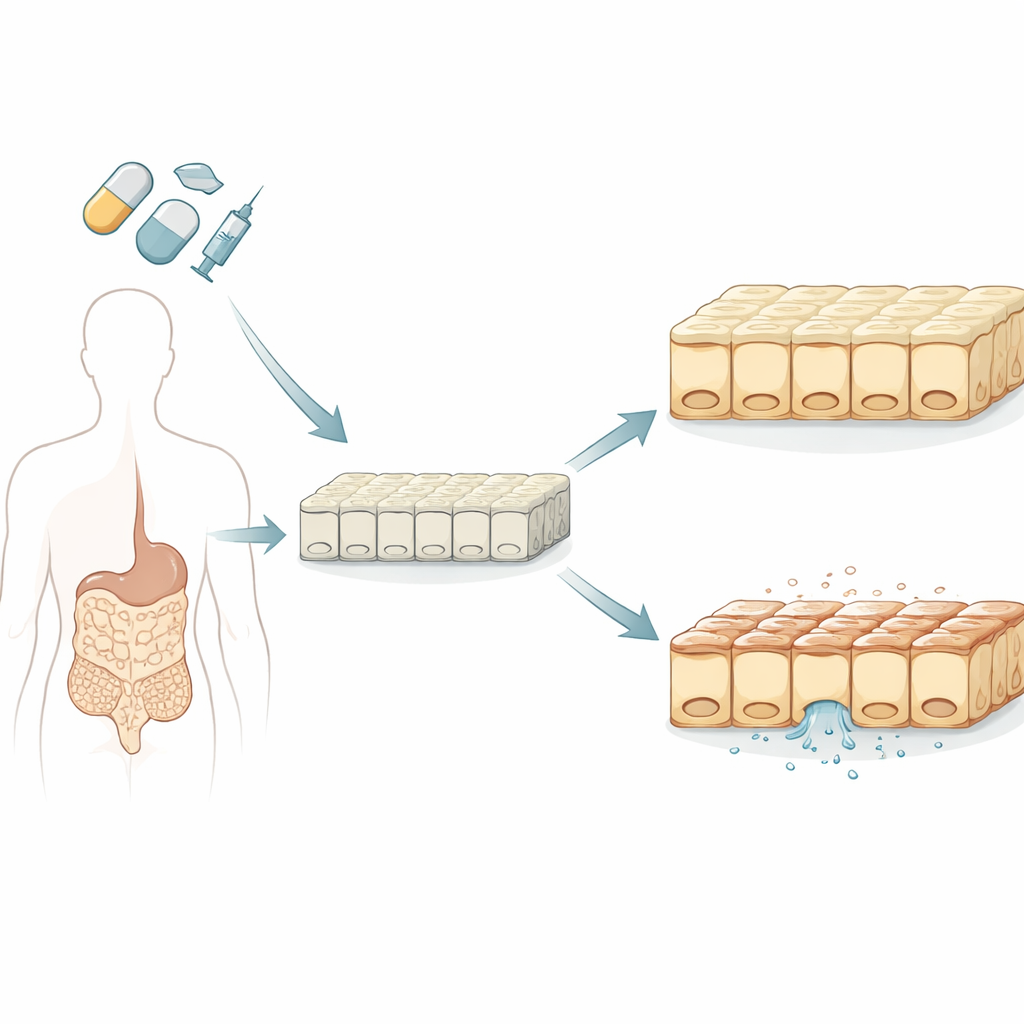
构建更好的微型肠道
研究人员首先利用干细胞在体外培养出人类肠上皮单层,干细胞具有分化为多种组织类型的能力。与长期用于药物测试的传统来源于肿瘤的细胞系不同,这些干细胞来源的细胞形成了更接近真实小肠的混合群体,包括分泌黏液和产生激素的细胞。团队确认这些实验室培养的肠道上皮在渗透性、上下极性以及影响药物通过和代谢的关键运输和代谢功能方面表现出逼真的特征。
测量屏障的电学致密性
为评估肠道安全性,研究组将重点放在跨上皮电阻(TEER)上,这是一种无创的读数,用以反映相邻细胞间的封闭程度。高TEER表示屏障致密且具有保护性;TEER下降则表明肠道与血流之间的壁变得泄漏。科学家将TEER与一种衡量细胞存活的标准测试(比如测量ATP等能量分子)进行比较。他们让新的肠道模型与旧的癌细胞模型分别暴露于17种已知在引发胃肠副作用频率上存在差异的药物,包括常见的化疗药、靶向抗癌小分子以及像布洛芬和其他抗炎药之类的止痛药。
在细胞死亡前发现隐性损伤
在这组药物中,干细胞来源的肠上皮的TEER测量结果优于传统的ATP测试和旧的癌细胞屏障模型。若干化疗药物在ATP水平上变化不大,表明细胞仍然存活,但它们导致TEER显著下降并在活死染色图像中显示出明显损伤。这意味着屏障在细胞完全死亡之前就可能失效,这是经典存活性测试无法察觉的早期预警。当团队将体外结果与临床记录中各药物引起胃肠症状的频率进行比较时,新的TEER测定几乎识别出所有高风险药物并对低风险药物给出正确的无问题提示,表现出很高的准确性。
药物如何破坏内部支架
为查明细胞内部出了什么问题,科学家在用两种靶向微管的化疗药处理后分析了基因表达活动。研究发现与细胞骨架、细胞间粘附和细胞外基质——帮助细胞锚定其周围环境的网状结构——相关的基因普遍下调。额外实验显示活性氧(ROS)随剂量增加而上升,活性氧是可损伤细胞结构的不稳定含氧分子。这些变化共同指向一系列事件:某些药物扰乱了肠上皮细胞的内部框架和细胞间连接,松动了屏障并使物质可通过细胞间隙渗漏。
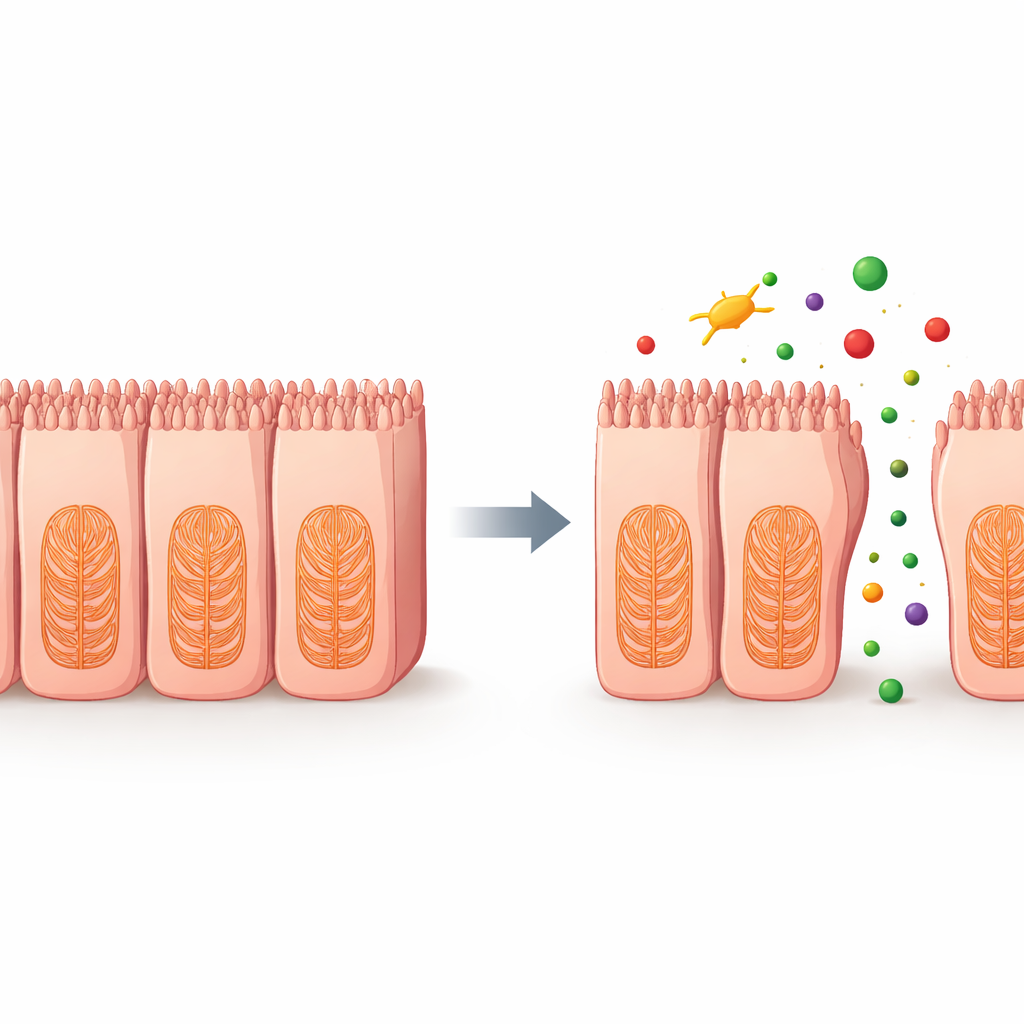
对患者有何意义
这项工作表明,基于干细胞的人体肠上皮模型结合对屏障致密性的简单电学测量,可以比长期使用的实验室方法更可靠地预测哪些药物可能引起肠道损伤。通过及早检测屏障弱化并将其与对细胞支架的潜在损伤相联系,该平台可帮助药物开发者在化合物进入临床前弃用或重新设计有风险的候选药物。长期来看,这类更逼真的“微型肠道”测试或能减少患者不适或危险的胃肠副作用,同时使医生能够更安全地使用强效疗法。
引用: Yu, W.D., Lee, S., Cho, HS. et al. Drug-induced gastrointestinal toxicity and barrier integrity: cytoskeleton-mediated impairment in a clinically relevant human intestinal epithelium model. Exp Mol Med 58, 487–500 (2026). https://doi.org/10.1038/s12276-025-01635-6
关键词: 胃肠毒性, 肠道屏障, 干细胞模型, 药物安全性, 化疗副作用