Clear Sky Science · zh
干扰素调节因子5通过NLRP3和表达Ly6C的细胞参与肺气肿的发病机制
这项肺部研究为何重要
慢性阻塞性肺疾病(COPD)和肺气肿夺走了数百万人的呼吸,即便他们早已戒烟。现有药物可以帮助打开气道,但很少能平息那种持续燃烧、不断侵蚀肺组织的隐匿性炎症。本研究揭示了造成这种损伤的一个分子“主谋”,提示了一种新的保护薄弱气囊并减缓肺功能下降的策略。
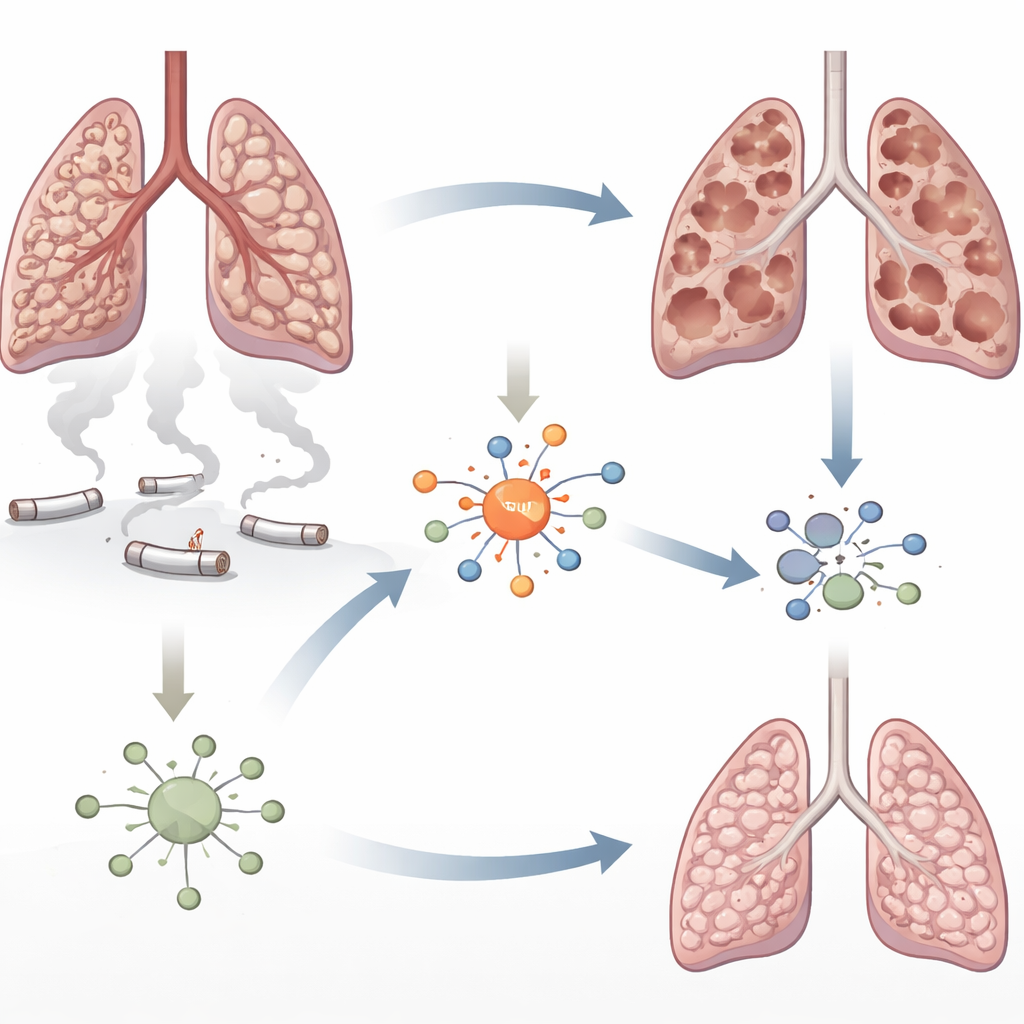
近距离观察烟草损伤的肺
肺气肿的特征是负责气体交换的微小气囊逐渐瓦解。香烟烟雾携带的有害颗粒浸袭肺组织,损伤细胞并招募大量免疫细胞。作者关注一种称为干扰素调节因子5(IRF5)的蛋白,它在自身免疫疾病中被认为能驱动炎症,但在COPD中未被充分研究。早期研究提示,暴露于烟雾的肺中IRF5水平会上升。本研究旨在弄清IRF5是随炎症被动上调,还是实际上促成了肺组织的破坏。
在小鼠中关闭关键开关
为了探查IRF5的作用,团队构建了完全缺失该基因的小鼠。他们将正常小鼠和缺失IRF5的小鼠分别暴露于数周的香烟烟雾,并比较其肺部状况。在正常小鼠中,烟雾导致明显的肺气肿表现:相邻气囊间的隔膜丧失,留下大而过度扩张的空腔。相比之下,缺乏IRF5的小鼠在结构损伤方面基本受到保护,尽管烟雾仍然将免疫细胞吸引到气腔并升高多种炎性分子水平。这表明IRF5是烟雾暴露与实际撕裂肺结构之间的关键联系。
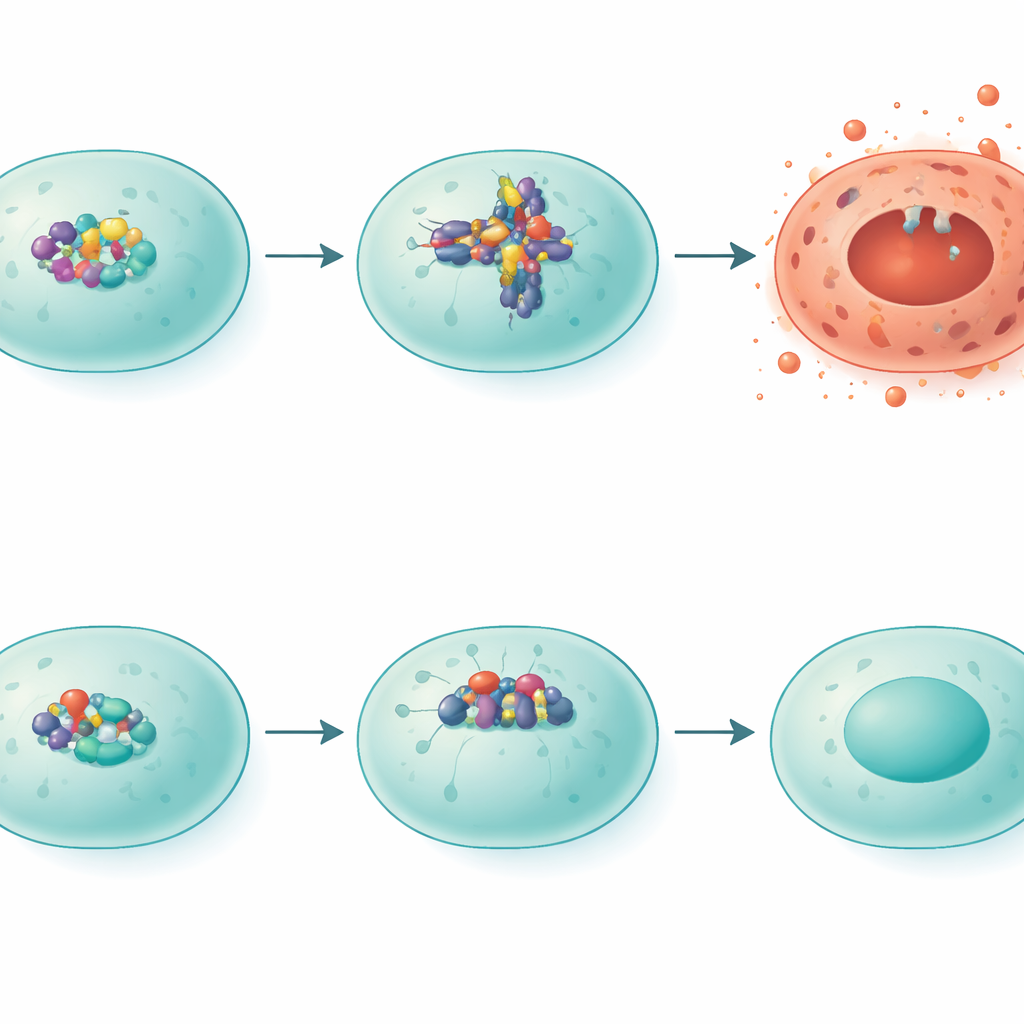
IRF5如何推动细胞走向剧烈死亡
研究者随后聚焦于一种名为焦亡(pyroptosis)的暴力细胞死亡形式,这种死亡会在细胞膜上炸出孔洞,将炎性内容物泄入周围组织。由NLRP3组成的蛋白复合体位于该过程的核心。在暴露于烟雾的正常小鼠中,NLRP3水平上升,另一种蛋白gasdermin D的剪切模式显示出类焦亡状态。在缺失IRF5的小鼠中,NLRP3水平明显较低,gasdermin D被切割成与较少破坏性结果相关的替代形式。当团队在体外将IRF5人为上调于与肺相关的细胞中时,NLRP3水平随之上升,证实了IRF5作为转录开关,启动这一有害通路的作用。
具有保护作用的免疫细胞登场
IRF5还改变了肺内免疫细胞的构成。在缺乏IRF5的小鼠中,一类在表面分子Ly6C上高度标记的血源性细胞显著增加。这些Ly6C高表达的细胞包括单核细胞和T细胞,在烟雾暴露后数量增多。当科学家从缺失IRF5的小鼠中分离出Ly6C高细胞并将其输注到普通烟雾暴露的小鼠体内时,接受者的气囊破坏减少,肺中NLRP3水平也降低。额外实验显示,IRF5直接抑制Ly6C基因的活性,提示在IRF5存在时,这类可能具有保护作用的细胞的产生或维持会减少。
人体肺部验证了这一信号
为检验这些发现是否与人相关,作者检查了因肺癌接受手术的患者肺组织样本。他们比较了气体交换功能良好的人与存在明显肺气肿者的组织。来自肺气肿组的肺组织中IRF5蛋白水平显著较高。尽管这项研究规模不足以把IRF5与症状严重度或急性加重直接关联,但该模式与小鼠结果一致:病变肺中IRF5更多,而较健康的肺中较少。
这对未来治疗意味着什么
综合来看,这项工作将IRF5描绘为烟雾驱动肺损伤的核心协调者。它增强了以NLRP3为中心的细胞死亡机制,并将免疫细胞谱系引向较少Ly6C高表达的群体,而后者似乎有助于维持气囊结构。对患者而言,含义很直接:一种能抑制IRF5活性的药物理论上可能减少最具破坏性的炎症形式,而不至于完全关闭免疫系统。尽管目前尚无用于COPD的此类疗法,本研究提供了清晰的分子靶点和一种在生物学上可行的治疗路径,目标不仅是打开狭窄的气道——还可能真正保护肺的脆弱支架。
引用: Heo, SH., Park, S.Y., Kim, N.H. et al. Interferon regulatory factor 5 involves the pathogenesis of emphysema through NLRP3 and Ly6C expressing cells. Exp Mol Med 58, 425–435 (2026). https://doi.org/10.1038/s12276-025-01632-9
关键词: 肺气肿, 慢性阻塞性肺病, 炎症, 肺免疫, 细胞死亡