Clear Sky Science · tr
Orak hücre hemoglobininin fibrilleşmesinin dörtlü yapısal kökeni: bir moleküler dinamikler çalışması
Bu kan öyküsü neden önemli
Orak hücre hastalığı, tek bir kan proteinindeki çok küçük bir değişiklikle başlar, ancak bu değişiklik kırmızı kan hücrelerini yeniden şekillendirip damarları tıkayabilir ve yaşam boyu süren ağrıya yol açabilir. Bu çalışma, o tek değişikliğin hemoglobin proteininin hücre içinde sert lifler halinde nasıl dizildiğini fizik temelli, ayrıntılı bir bakışla inceliyor. Gelişmiş bilgisayar simülasyonlarını kullanarak yazarlar atomik ayrıntıları tüm hücre düzeyindeki sorunlarla ilişkilendiriyor ve gelecekteki ilaçların hemoglobinin kan akışını tıkamasını nasıl önleyebileceğine dair yeni ipuçları sunuyor.
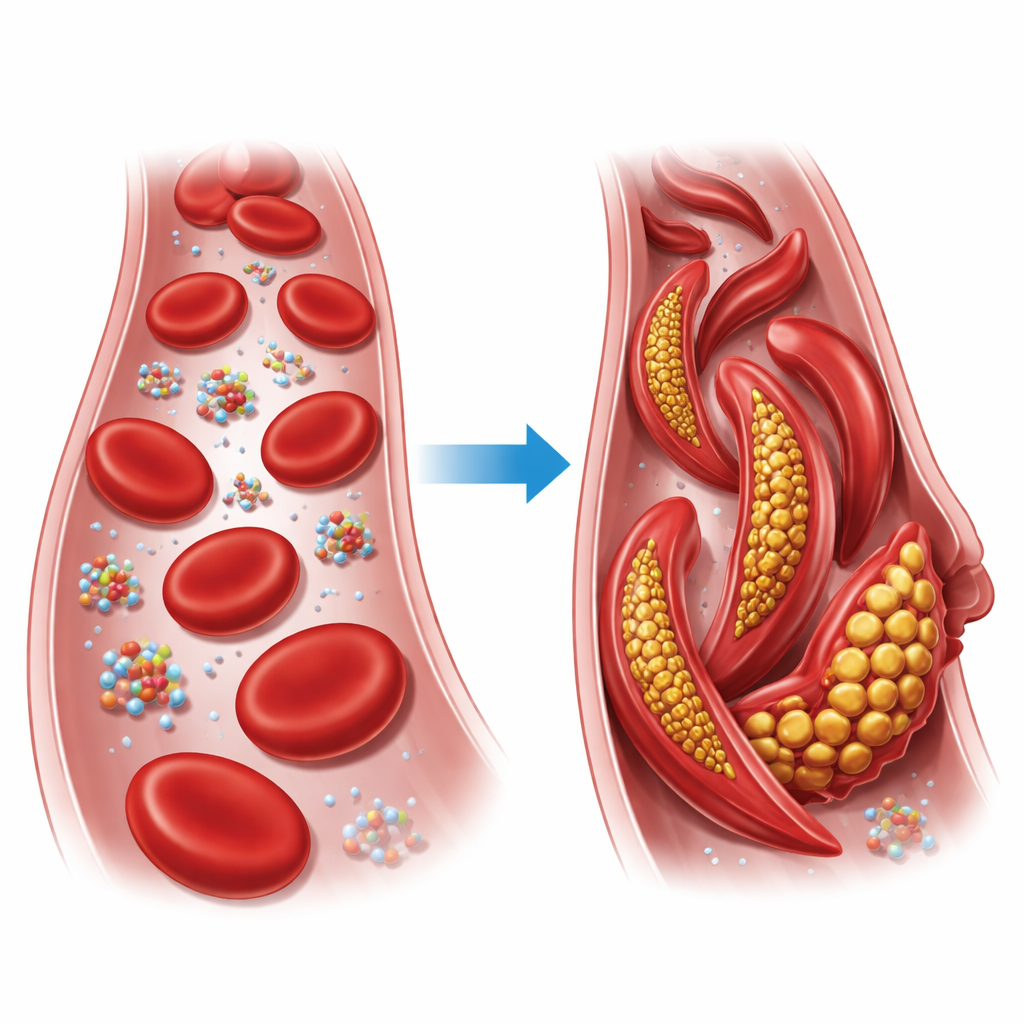
Küçük bir değişim, büyük sonuçlar
Hemoglobin, kırmızı kan hücrelerimizi oksijenle taşıyan proteindir. Her hemoglobin ünitesi dört zincirden oluşur ve bunlar gevşek (R) durumu ile gergin (T) durumu olarak bilinen iki ana genel halde düzenlenebilir. Orak hücre hastalığında, bu zincirlerden birindeki tek bir yapı taşı değişir: yük taşıyan bir glutamat, beta zincirinin 6. pozisyonunda yağlı bir valin ile yer değiştirir. Düşük oksijen koşullarında bu değişmiş versiyon —orak hemoglobin— uzun lifler halinde birbirine bağlanır ve normalde yuvarlak olan kırmızı kan hücrelerini sert, orak benzeri şekillere dönüştürerek küçük damarları tıkayabilir ve dokuları oksijen kıtlığına sokabilir.
Hemoglobinin kayıp şekillerini izlemek
Yazarlar, tam hemoglobin ünitelerinin bir lif içinde nasıl döndüğünü ve bir araya geldiğini inceliyor. Bu büyük ölçekli şekil değişikliğini, proteinin iki yarısının birbirine göre nasıl döndüğünü ölçen tek bir açıyla takip ediyorlar. Moleküler dinamik simülasyonları—atomların su ve tuz ortamında zaman içinde nasıl hareket ettiğini hesaplayan sanal deneyler—kullanarak bu açıyı geniş bir aralıkta nazikçe zorlayıp her şeklin ne kadarlık enerji maliyeti olduğunu hesaplıyorlar. Vücut sıcaklığında hem normal hem de orak hemoglobinin birçok böyle şekli keşfedebildiğini görüyorlar. Orak hemoglobin hafifçe tercih edilen bir açı gösteriyor, ancak bu şekil tercihleri tek başına neden yalnızca orak formunun kararlı lifler oluşturduğunu açıklamak için yeterli değil.
Orak lifleri neden yapışır, normal olanlar neden parçalanır
Lif oluşumunun özüne inmek için çalışma, komşu hemoglobin ünitelerinin lif boyunca ve lifler arası nasıl çekim kurduğunu ölçüyor. Ekip, birçok farklı genel şekil için birlikleri bir arada tutan net çekim olan kohezyon enerjisini hesaplıyor. Orak hemoglobin için bu kohezyon enerjisi test ettikleri tüm şekil aralığında negatif (yani çekici) kalıyor; dolayısıyla lifler kararlı kalıyor ve kolayca ayrışmıyor. Buna karşılık normal hemoglobin için bazı şekillerde kohezyon enerjisi pozitif çıkıyor ve bu açılarda lifler kararsız olup kendiliğinden parçalanmaya yatkın oluyor. Kritik fark, mutasyona uğramış valin yan gruplarının komşu proteinlerin içine nasıl sokulduğu: orak hemoglobinde bu yağlı bölgeler hem yanal hem de lif ekseni boyunca sağlam temaslar kurarak doğrudan lif büyümesini destekliyor.
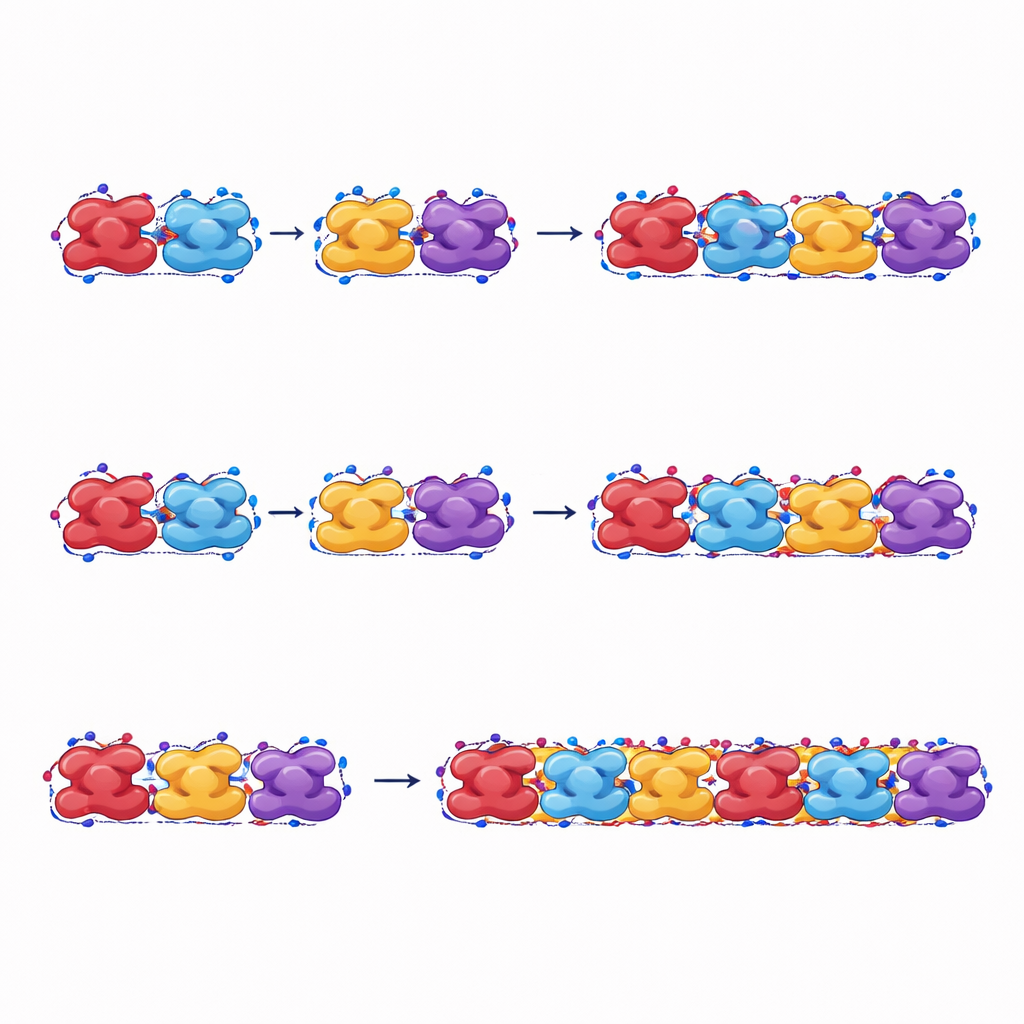
Bu lifler nasıl yük taşır ve nasıl kırılır
Yazarlar, mekanik stresi taklit etmek için simüle ettikleri lifleri aynı zamanda geriyor. Uzunluk doğrultusunda çekildiğinde, orak hemoglobinden yapılan lifler normal hemoglobinden yapılanlara göre daha yüksek kuvvet ve şekil değişimine dayanıyor ve kırılmadan önce daha fazla enerji dağıtıyor. Liflerin ilk ortaya çıktığı form olmasa da orak liflerin gevşek formu bile, şekil açısından plastik değişiklikler yoluyla bağı koruyarak bir kez oluşmuş lifin bütünlüğünü sürdürmeye yardım edebiliyor. Buna karşılık normal hemoglobin lifleri komşu üniteler arasında daha kolay ayrılıyor ve kırılmadan önce daha az enerji absorbe ediyor; bu da onların stres altında daha az kararlı olduğunu doğruluyor.
Gelecekteki tedaviler ve yeni malzemeler için ipuçları
Toparlanacak olursa, simülasyonlar tek bir amino asit değişikliğinin hemoglobin ünitelerinin nasıl bir araya geldiğini yeniden şekillendirdiğini; özellikle gergin durumda, bütünsel düzeni liflerin güçlü çekimini destekleyen açılara bükerek hemoglobinin uzun, sert lifler oluşturmasını sağladığını gösteriyor. Bu geometri ve yapışkanlığın birleşimi orak hemoglobinin termal harekete ve mekanik çekime karşı dirençli lifler oluşturmasına izin veriyor; bu da nihayetinde kırmızı kan hücrelerini deforme edip kan akışını engelliyor. Genel protein düzeninin lif kararlılığını kontrol eden belirli özelliklere işaret ederek, çalışma etkili anti-orak ilaçlarının hemoglobini liflerin energetik olarak elverişsiz ve mekanik olarak kırılgan olduğu şekillere yönlendirerek işe yarayabileceğini —yani ölümcül bir moleküler tıkanıklığı serbest akışlı bir kan akışına geri çevirebileceğini— öne sürüyor.
Atıf: Jiang, M., Qin, Z. The quaternary structure origin of the fibrillation of sickle hemoglobin: a molecular dynamics study. npj Soft Matter 2, 7 (2026). https://doi.org/10.1038/s44431-026-00019-8
Anahtar kelimeler: orak hücre hastalığı, hemoglobin lifleri, protein agregrasyonu, moleküler dinamikler, kan bozuklukları