Clear Sky Science · tr
Hesaplamalı ve deneysel boşluğu köprüleme: öğrenme modellerinin karşılaştırılmasına dayalı Alzheimer tedavilerini önceliklendirmek için büyük dil modelinden yararlanma
Aileler ve hastalar için neden önemli
Alzheimer hastalığı insanlardan hafızayı, bağımsızlığı ve yaşam kalitesini alır; ancak gerçekten etkili tedaviler hâlâ nadirdir. Bu çalışma, mevcut ilaçları kullanarak yeni tedaviler bulmayı hızlandırmanın bir yolunu araştırıyor: güçlü bilgisayar modellerini, günlük sohbet botlarında kullanılan türde bir yapay zeka olan büyük bir dil modeliyle (LLM) birleştirerek büyük miktarda tıbbi veri ve araştırma makalesini tarıyor. Amaç, uzun aday ilaç listesini, bilim insanlarının ve doktorların gerçekten hastalarda test edebileceği küçük, gerçekçi bir kümeye daraltmaktır.
Mevcut ilaçları yeni bir amaç için yeniden kullanmak
Yepyeni bir ilaç geliştirmek on yıldan uzun sürebilir ve milyarlarca dolara mal olabilir; başarı garantisi yoktur. Alternatif olarak ‘‘ilaç yeniden kullanımı’’ mevcut onaylı ilaçların Parkinson veya depresyon gibi diğer koşullar için değil de yeni amaçlarla kullanılma olasılığını araştırır. Bu ilaçların güvenlik profilleri bilindiği için Alzheimer için klinik denemelere daha hızlı geçme olanağı sunarlar. Ancak biyolojik veritabanlarını ve tıp literatürünü tarayan modern bilgisayar yöntemleri artık araştırmacıların elle gerçekçi şekilde değerlendirebileceğinden çok daha fazla aday üretiyor ve bu da süreçte yeni bir darboğaz yaratıyor.
Birden çok akıllı modeli bir araya getirmek
Araştırma ekibi bu sorunu, üç farklı gelişmiş bilgisayar modelinden başlayan bir Alzheimer İlaç Yeniden Kullanım çerçevesi oluşturmak suretiyle ele aldı. Her model, hastalıklar, ilaçlar, genler ve diğer tıbbi kavramları birbirine bağlayan büyük bir biyomedikal “harita” olan bilgi grafiğini inceliyor ve Alzheimer’a yardımcı olabilecek ilaçları öneriyordu. Her model desenleri farklı gördüğü için listeler tam olarak örtüşmüyordu. Yazarlar her modelin ilk 30 önerisini alınan toplam 90 aday ilacı içeren tek bir havuzda birleştirdiler; ardından büyük dil modelini otomatik ama temkinli bir değerlendirici rolünde kullanarak her ilaç için yayımlanmış çalışmaları okuttu ve kanıtın Alzheimer için yardımcı, nötr veya zararlı görünüp görünmediğini değerlendirmesini sağladılar.
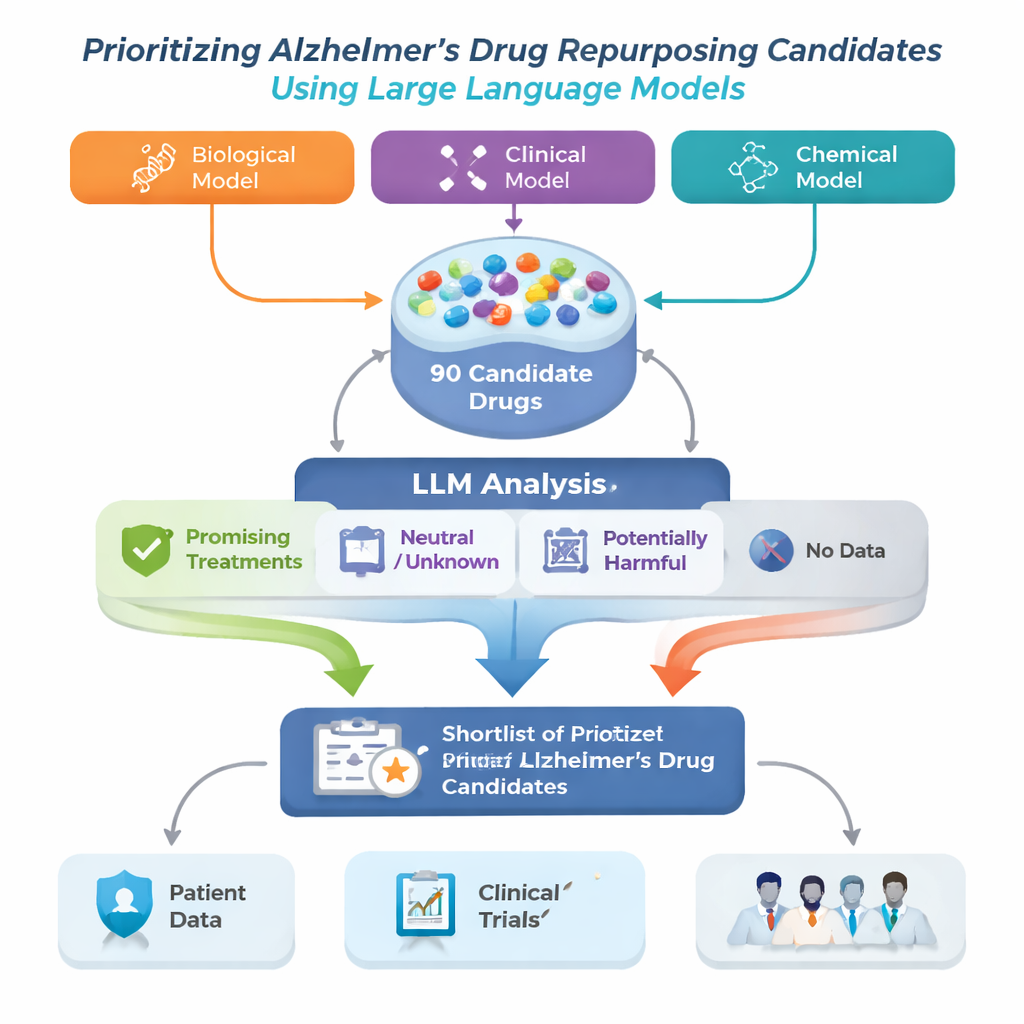
Yapay zekâ tıp literatürünü nasıl okuyor
Her aday ilaç için sistem PubMed’den en fazla 200 bilimsel özet ve ayrıca bir ilaç veritabanından ayrıntılı ilaç açıklamaları çekti. LLM’den değerlendirmesini yalnızca kendisine gösterilen metne dayandırması ve her özeti Alzheimer tedavisi açısından olumlu, nötr veya olumsuz olarak etiketlemesi istendi. Bu etiketler daha sonra basit puanlara dönüştürüldü: olumlu, nötr veya olumsuz olan özetlerin payı. İki kural seti kullanılarak—biri açık olumlu kanıt gerektiren daha katı, diğeri faydaya dair herhangi bir ipucunu işaretleyen daha hoşgörülü—çerçeve ilaçları dört gruba ayırdı: umut vadeden tedaviler, potansiyel olarak zararlı olanlar, belirsiz veya nötr olanlar ve Alzheimer ile ilgili hiçbir makalesi olmayan ilaçlar. Son grup, az incelenmiş olmasına karşın özellikle yenilikçi fırsatlar barındırabilir.
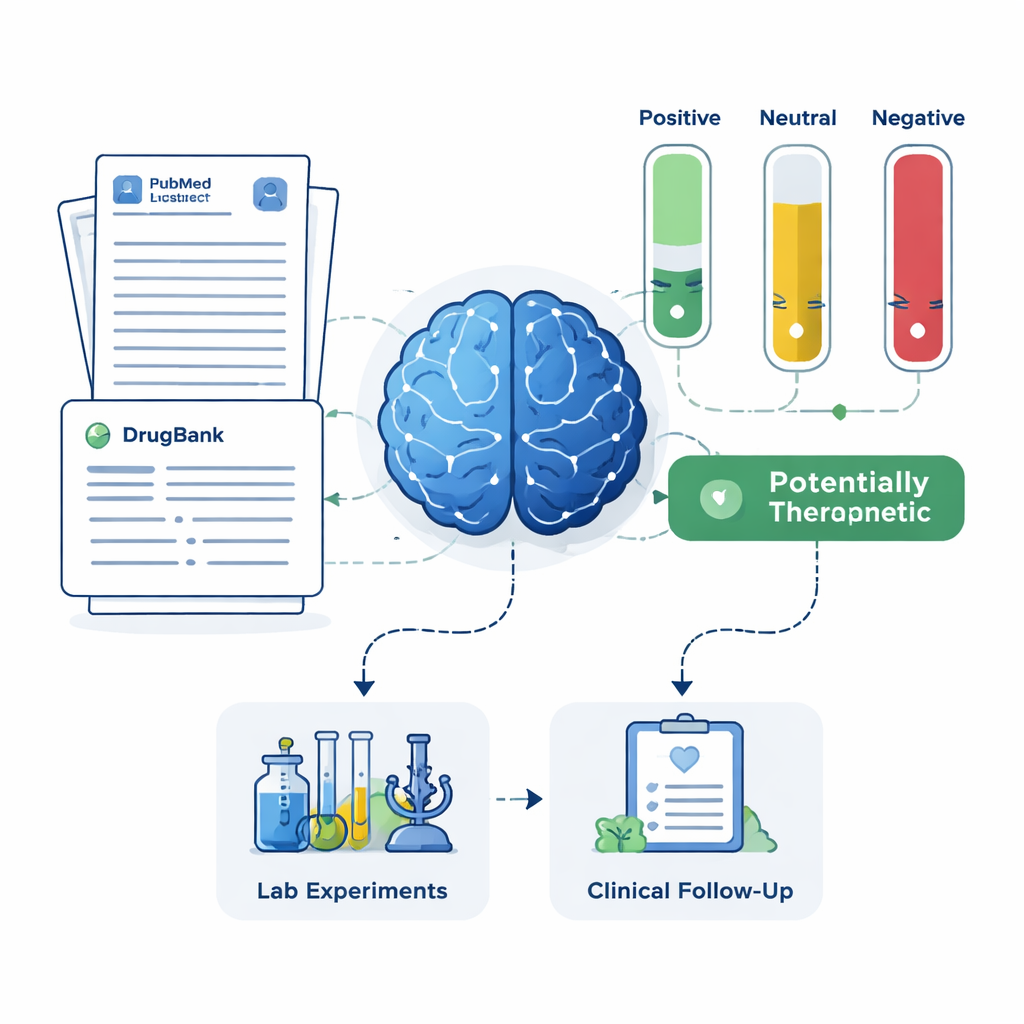
Gerçek hastalar ve klinik denemelerle karşılaştırma
Yapay zekânın kısa listesinin gerçek dünyada anlamlı olup olmadığını görmek için ekip sonuçlarını iki bağımsız kaynakla karşılaştırdı: büyük bir Alzheimer hasta sicili ve kayıtlı klinik denemelerin kayıtları. Çerçeve, hasta verilerinde güçlü koruyucu sinyaller ve geniş deneme geçmişine sahip mevcut bir Alzheimer ilacı olan memantin’i yüksek öncelikli bir aday olarak başarılı şekilde geri getirdi. Ayrıca magnezyum, minosiklin, pimavanserin, testosteron ve doksisiklin gibi değişen düzeylerde destekleyici araştırmalar olan ancak uzman klinisyenlerce umut verici bulunan ilaçları da vurguladı. Aynı zamanda, literatürün olası zararı veya fayda eksikliğini gösterdiği ilaçları tespit ederek bunların önceliklerinin düşürülmesini veya tedavi yerine yan etki araştırmaları için incelenmesini önerdi.
Bilgisayar tahminlerinden pratik sonraki adımlara
Günlük ifadeyle, bu çerçeve binlerce makaleyi okuyan, büyük tıbbi veritabanlarındaki desenleri çapraz denetleyen ve insan uzmanlara odaklanmaları için çok daha kısa, daha iyi düzenlenmiş bir Alzheimer ilaç adayları listesi sunan ultra hızlı, dikkatli bir araştırma asistanı gibi davranır. Çalışma, fikir üretmek için grafik tabanlı modelleri ve kanıtı değerlendirmek için bir dil modelini birleştirerek araştırmacıların iyi desteklenen ilaçları ve test için ilgi çekici yeni seçenekleri daha hızlı bulabileceğini gösteriyor. Bu yaklaşım tek başına Alzheimer’ı tedavi etmese de, bilgisayar tarafından üretilen fikirleri laboratuvar deneyleri ve klinik denemelerin zorlu çalışmasıyla bağlamanın güçlü yeni bir yolunu sunuyor ve potansiyel olarak daha etkili tedavilere giden yolu hızlandırabilir.
Atıf: Li, M., Niu, S., Xu, Y. et al. Bridging the computational-experimental gap: leveraging large language model to prioritize Alzheimer’s therapeutics based on comparison of learning models. npj Health Syst. 3, 20 (2026). https://doi.org/10.1038/s44401-026-00074-3
Anahtar kelimeler: Alzheimer hastalığı, ilaç yeniden kullanımı, yapay zeka, büyük dil modelleri, bilgi grafikleri