Clear Sky Science · tr
Tümör mikroçevresindeki mekânsal olarak değişen ilişkileri modellemek için graflarda fonksiyonel kenarları kodlamak
Kanserin mahalle haritasını çıkarmak neden önemli
Kanser tek başına büyümez. Tümör hücreleri bağışıklık hücreleri, destek hücreleri, kan damarları ve kimyasal sinyallerle dolu, mekânsal olarak sıkışık bir mahallede yaşar. Bu komşuların nasıl düzenlendiği ve birbirlerini ne kadar güçlü etkilediği, kanserin yayılıp yayılmayacağını, tedaviye yanıt verip vermeyeceğini ya da kontrol altında kalıp kalmayacağını belirleyebilir. Bu makale, mikroskopik görüntüler ve tümörlerin moleküler haritalarını ağlara dönüştüren yeni bir yapay zeka çerçevesi SPIFEE’yi tanıtıyor; bu sayede araştırmacılar hangi hücre ve yol etkileşimlerinin hastalık türü ve hasta sonucu ile en çok ilişki kurduğunu saptayabiliyor.
Dokuyu bir ağ haritasına dönüştürmek
Modern kanser çalışmalarında bir tümörün mikroskop altındaki görüntüsünden çok daha fazlası ölçülebiliyor. Bazı yöntemler tek hücrede onlarca proteini vurgularken, diğerleri doku yapısının ayrıntılı renkli kesitlerini sağlar ve yeni araçlar tümör diliminin binlerce noktasında hangi genlerin aktif olduğunu kaydeder. SPIFEE bunların tümünü aynı mahallenin farklı görünümleri olarak ele alır. Her örneği bir grafik olarak temsil eder: düğümler tümör mikroçevresindeki hücre tipleri, görsel doku desenleri veya moleküler yollar gibi anahtar varlıkları gösterirken, kenarlar bu varlıkların mekânda nasıl etkileşime girdiğini yakalar. Kritik olarak, SPIFEE bir etkileşimi “mesafe” gibi tek bir sayıya indirgemez. Bunun yerine her kenar, iki varlığın belirli mesafe aralıklarında ne kadar karıştığını veya birbirini ittiğini tanımlayan küçük bir eğri saklar ve böylece daha zengin mekânsal ayrıntıyı korur.
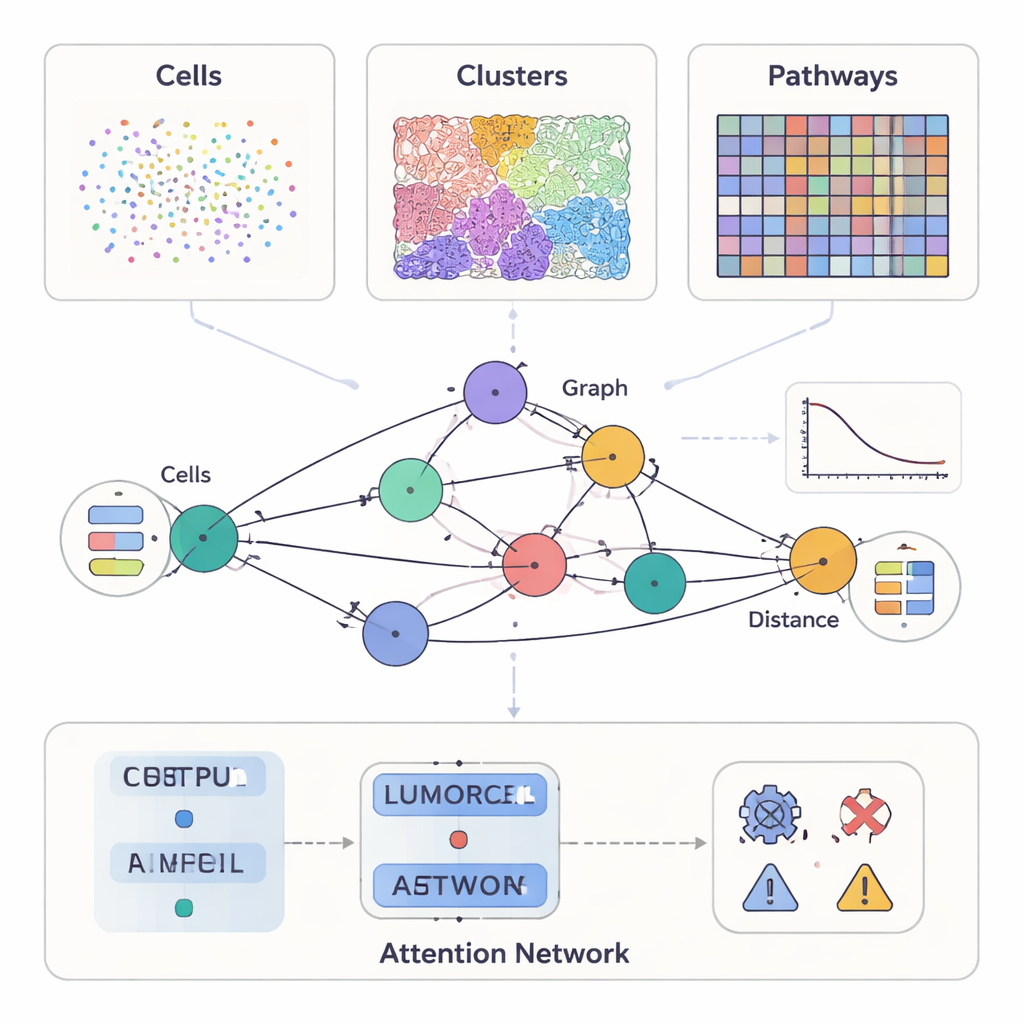
Çeşitli kanser verilerine esnek bir mercek
Yazarlar SPIFEE’yi farklı teknoloji ve ölçeklerdeki birkaç büyük, bağımsız kanser veri setinde test ettiler. Çoklu immunofloresans ile etiketlenmiş pankreas örneklerinde grafikte her düğüm bir hücre tipini temsil ediyordu ve düğüm özellikleri bu hücrelerin nasıl iletişim kurma eğiliminde olduğunu özetleyen tek hücre RNA dizilemesinden geliyordu. Rutin hematoksilin-eozin ile boyanmış akciğer kanseri kesitlerinde düğümler, kendi kendine denetimli bir öğrenme sistemi tarafından otomatik olarak keşfedilen yinelenen görsel doku desenlerini temsil etti. Üçüncü bir durumda, standart akciğer kanseri kesitleri derin öğrenme aracıyla sanal mekânsal transkriptomik haritalara dönüştürüldü ve SPIFEE düğümleri hipoksi, östrojen veya JAK–STAT sinyalleşmesi gibi moleküler yolları; özellikler ise gen aktivitesinden türetilen değerleri temsil ediyordu. Tüm bu ayarlarda aynı çerçeve farklı düğüm türlerini alıp yine karşılaştırılabilir mekânsal grafikleri oluşturabildi.
Sağkalım sonuçlarını ayıran etkileşimleri bulmak
SPIFEE bir grafik oluşturduktan sonra, grafiği bir graf dikkat (graph attention) ağına geçirir; bu ağ sadece bir sonucu—örneğin kanser alt tipi, sağkalım riski veya hastalık ile kanser dışı iltihap arasındaki farkı—tahmin etmeyi öğrenmekle kalmaz, aynı zamanda hangi kenarların o tahmin için en önemli olduğunu vurgular. Pankreas dokusunda SPIFEE, kronik pankreatiti pankreas duktal adenokarsinomadan önceki graf tabanlı yöntemlerden daha yüksek doğrulukla ayırt etti. Model tutarlı şekilde epiteliyal (tümör-benzeri) hücrelerle düzenleyici T hücreleri, antijen sunan hücreler ve yardımcı T hücrelerini içeren etkileşimlere odaklandı; bu da kanserde iltihaba kıyasla daha belirgin bir immünsüpresif çevreye işaret ediyor. Akciğer adenokarsinomu kesitlerinde SPIFEE, etkileşimleri daha iyi veya daha kötü sağkalımla ilişkili olan belirli stromal–tümör desenlerini belirledi; bu da tümör ile destekleyici doku arasındaki “sınır bölgelerinin” standart analizlerin kaçırabileceği önemli prognostik ipuçları taşıdığını öneriyor.
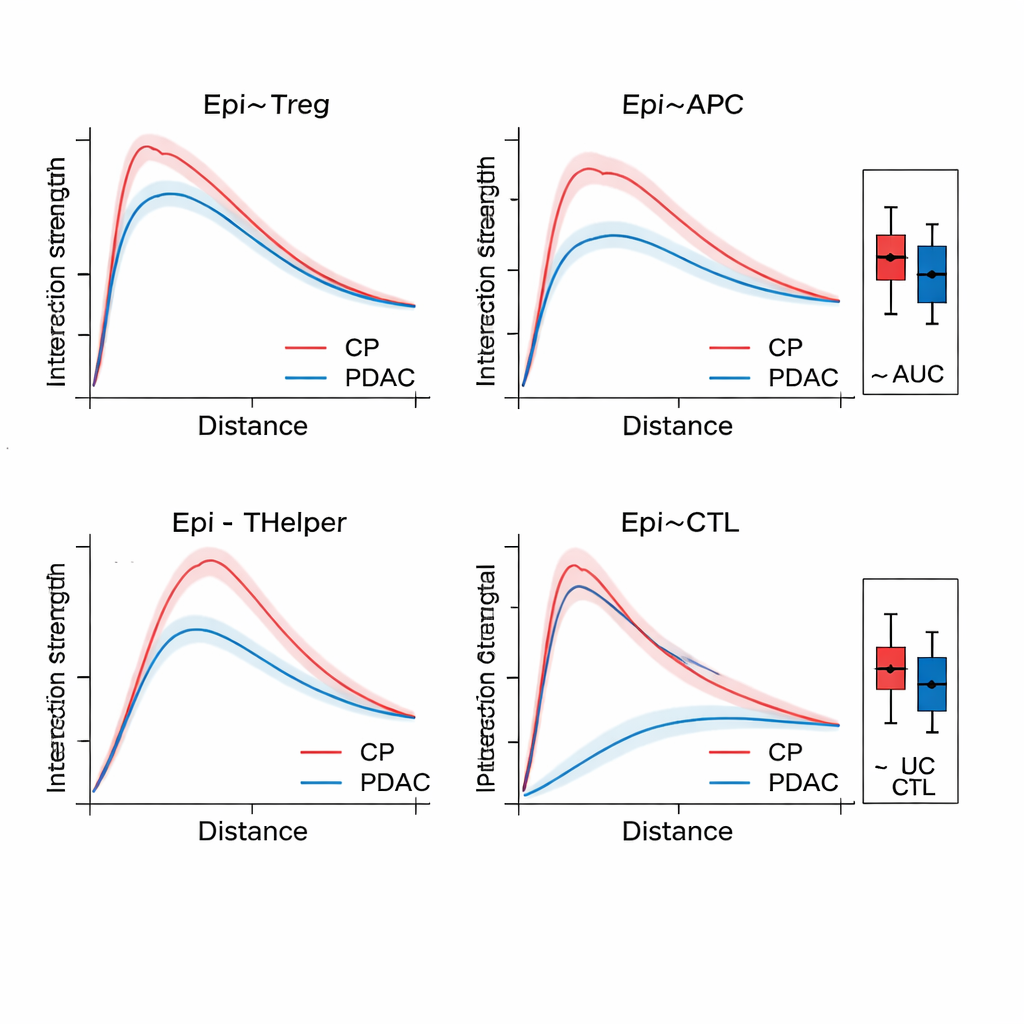
Rutin kesitlerden moleküler karşılıklı konuşmaları okumak
Belki de en çarpıcı olanı, SPIFEE’nin sıradan patoloji görüntüleri gen-aktivite tahmin haritalarına çevrildiğinde anlamlı yol etkileşimlerini çıkarabilmesiydi. Yolları düğümler ve bunların mekânsal birlikte-ortaya-gelişini fonksiyonel kenarlar olarak ele alarak, yöntem hipoksi ile EGFR veya JAK–STAT ile PI3K gibi çiftleri ön plana çıkardı—akciğer kanserinde immün kaçış ve ilaç direncini zaten bilinen kombinasyonlar. Ayrıca akciğer adenokarsinomunda östrojenle ilişkili yolları, skuamöz tümörlerde ise belirli immün ve stres yollarını önceliklendirdi; bu bulgular toplu RNA dizileme ve bağımsız gerçek mekânsal transkriptomik veri setindeki desenlerle uyumluydu. Bu, moleküler ölçümler yaklaşık olsa bile rutin kesitlerdeki mekânsal kalıpların, önemli yolların tümör içinde nasıl etkileştiğine dair geri kazanılabilir sinyaller taşıdığını gösteriyor.
Geleceğin kanser bakımına ne anlama geliyor
Uzman olmayan biri için ana mesaj şudur: SPIFEE, tümör hücrelerinin “sosyal yaşamını” görüntülerden ve moleküler haritalardan doğrudan okumaya olanak veren yeni bir yol sunuyor. İlişkilerin mesafe ile nasıl değiştiğini tek puanlara indirgemek yerine kodlayarak ve hangi etkileşimlerin en önemli olduğunu sıralamak için dikkat tabanlı sinir ağları kullanarak, bu çerçeve kanser tiplerini ayıran ve sağkalımı tahmin eden hücre, doku deseni ve yol kombinasyonlarını ortaya çıkarabiliyor. Bu bulguların biyolojik ve klinik doğrulamaya ihtiyacı olmakla birlikte, SPIFEE gibi yaklaşımlar rutin tümör örneklerinin sadece statik anlık görüntüler değil, tanı, risk sınıflandırması ve nihayetinde kişiselleştirilmiş tedavi seçimlerini yönlendirmeye yardımcı olabilecek etkileşim sıcak noktalarının dinamik haritalarını sağlayabileceği bir geleceğe işaret ediyor.
Atıf: Tsang, A.P., Krishnan, S.N., Kulkarni, R. et al. Encoding functional edges in graphs to model spatially varying relationships in the tumor microenvironment. npj Artif. Intell. 2, 27 (2026). https://doi.org/10.1038/s44387-026-00075-5
Anahtar kelimeler: tümör mikroçevresi, mekânsal transkriptomik, graf sinir ağları, kanser patolojisi, hücre-hücre etkileşimleri