Clear Sky Science · tr
İnteraksiyon-kısıtlı 3B molekül üretimi: bir difüzyon modeli kullanılarak yapıya dayalı farmakofor modellemesini mümkün kılmak
Neden daha iyi ilaç tasarlamak bu kadar zor?
Modern ilaç keşfi sıklıkla küçük bir molekülü bir proteine kilit için anahtar sokuyormuş gibi yerleştirmeye bağlıdır. Ancak anahtar sadece uyum sağlamakla kalmamalı: ilacın güçlü ve özgül şekilde bağlanabilmesi için zayıf elektriksel çekimler ve sudan kaçınan yüzeyler gibi doğru küçük çekimlerin de oluşması gerekir. Kimyasal evren astronomik ölçüde büyüktür ve günümüz veri tabanlarının çok ötesindedir; bu yüzden araştırmacılar, bu hayati temas desenlerini koruyarak sıfırdan yeni anahtarlar icat etmenin daha akıllı yollarını arıyorlar.
Bilgisayara gerçekten önemli olanı öğretmek
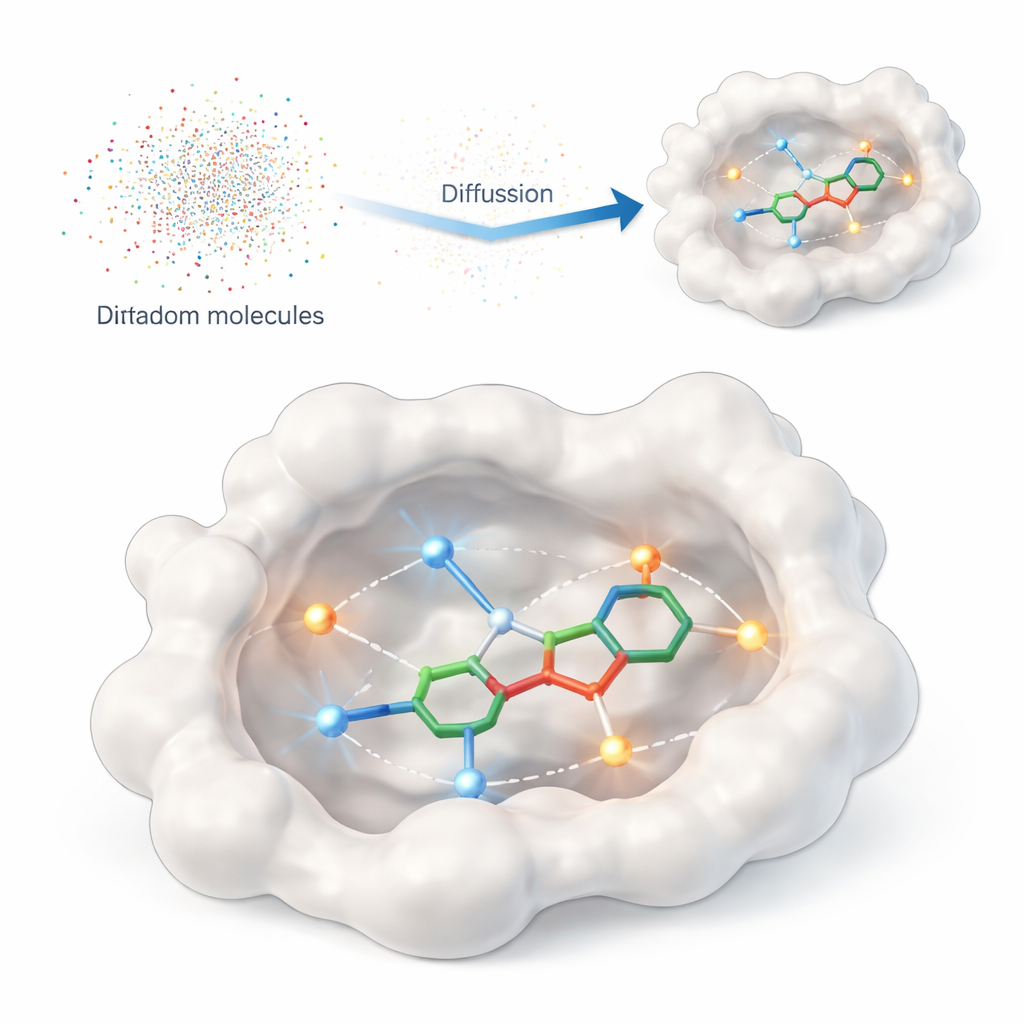
Bu çalışma, bir proteinin bağlanma cebinin içinde doğrudan üç boyutlu ilaç benzeri moleküller üreten DiffPharma adlı hesaplamalı bir çerçeveyi tanıtıyor. Algoritmadan mevcut bileşiklerin devasa kataloglarında arama yapması istenmek yerine, DiffPharma atom atom yeni moleküller oluşturuyor ve bunları proteinin nasıl etkileşmesi gerektiğiyle yönlendiriyor. Yöntem, rastgele gürültüden başlayıp kademeli olarak bunu yapılandırılmış bir nesneye —bu durumda proteinin cebine yerleşmiş bir 3B molekül— "gürültü giderme" şeklinde dönüştüren modern bir üretken model sınıfı olan difüzyon modelleri üzerine kuruludur.
Proteinin tokalaşmasını kodlamak
Modele proteinin yüzeyinde neyin önemli olduğunu anlatmak için yazarlar, anahtar temasları proteinin ve bir referans molekülün yolları boyunca serpiştirilmiş küçük "etkileşim parçacıkları" olarak temsil ediyor. İki yaygın etkileşim türü vurgulanıyor: belirli atomlar arasında yönlü mıknatıslar gibi davranan hidrojen bağları ve suyun uzağında kümelenen yağlı bölgeler şeklinde ortaya çıkan hidrofobik temaslar. Ayrı sinir ağları her etkileşim türünün geometrisini ve kimyasını, ayrıca bağlanma cebinin genel şeklini öğreniyor; ardından özel bir füzyon mimarisi bu bakış açılarını tek, tutarlı bir resimde birleştirerek molekül üretimini yönlendiriyor.
Gerçek bağlanma desenlerini ne kadar iyi taklit ediyor?
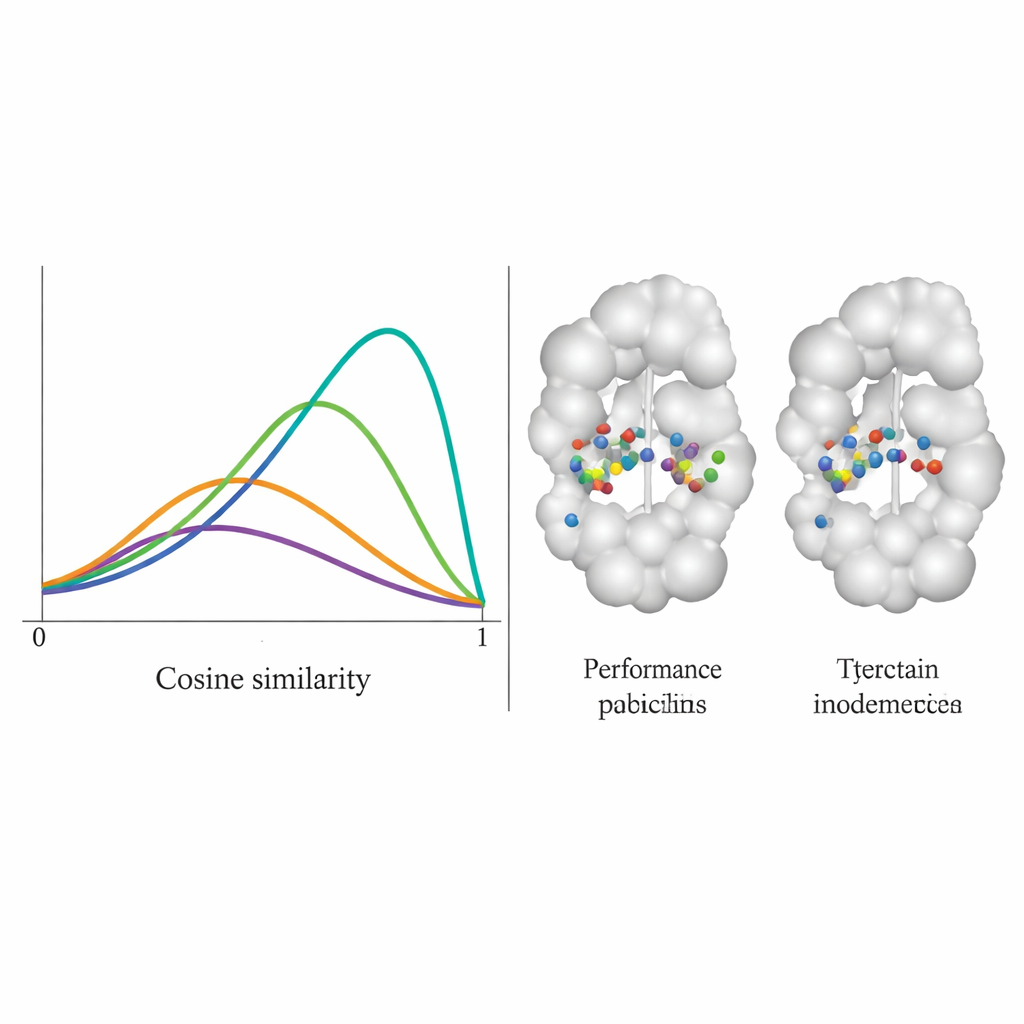
Ekip, DiffPharma’yı 100 farklı protein–molekül çiftinde test etti ve yeni moleküllerin orijinal temas desenlerini kalça kalça ne kadar sadakatle yeniden ürettiğini sordu. Bunu 0 ile 1 arasında değişen, 1’in mükemmel uyum anlamına geldiği kosinüs benzerliği puanı ile ölçtüler. DiffPharma’nın dağılımı yaklaşık 0.9 civarında doruk yaptı; bu da ortalamada aynı protein kalıntılarının referans yapılardakiyle aynı türde anahtar etkileşimleri oluşturduğu anlamına geliyor — altı rakip yönteme kıyasla önemli ölçüde daha iyi. Önemli olarak, model bunu yaparken çeşitli moleküler şekiller üretmeye devam etti ve üretilen bileşikler gerçek, kararlı moleküllere tipik bağ uzunlukları, açılar ve genel 3B geometri korudu.
Teoriden pratik ilaç adaylarına
Benchmark’ların ötesinde yazarlar, DiffPharma’nın gerçek hedefler için mantıklı ilaç adayları tasarlayıp tasarlayamayacağını sordular. İyi çalışılmış iki enzim —AKT kinaz ve antibiyotik direnciyle bağlantılı bir β‑laktamaz— için yöntem, bilinen ligantların temel etkileşim desenlerini koruyan ancak çoğu zaman farklı kimyasal iskeletler kullanan moleküller üretti; bu, ilaç kimyasında arzu edilen bir "iskelet atlama" biçimidir. SARS‑CoV‑2 ana proteazı üzerine daha zorlayıcı bir vaka çalışmasında, DiffPharma belirli etkileşim seçimleri kullanılarak yönlendirildi ve ardından moleküler dinamik simülasyonlar ve bağlanma enerjisi tahminleri ile incelendi. Daha katı etkileşim kısıtları altında üretilen moleküller daha stabil kompleksler oluşturdu ve bazen bilinen bir referans inhibitörden daha elverişli öngörülen bağlanma enerjileri gösterdi. Kayda değer biçimde, sistem eğitim sırasında hiç görünmemiş olmasına rağmen protein yapısı ve etkileşim talimatlarından yalnızca referans bileşiği yeniden keşfetti.
Gelecekteki ilaçlar için bunun anlamı
Uzman olmayan biri için DiffPharma, proteinin cebinin şekli ve istenen "tokalaşma" desenleri verildiğinde uygun kimyasal anahtarlar öneren akıllı, 3B farkındalıklı bir taslak aracı olarak düşünülebilir. Henüz bir ilacın ihtiyaç duyduğu tüm özellikleri —çözünebilirlik veya metabolizma gibi— optimize etmiyor olsa da yöntem, proteinin yüzeyindeki hayati temas haritasını güvenilir şekilde koruyor ve mevcut katalogların ötesinde kimyasal uzayın yeni bölgelerini keşfediyor. Bu etkileşim‑yönlendirmeli yaklaşım, hastalıkla ilişkili proteinlerin yapısal verilerinden deneysel ilaç geliştirme için çeşitli, gerçekçi başlangıç noktalarına daha hızlı geçişte araştırmacılara yardımcı olabilir.
Atıf: Sako, M., Yasuo, N. & Sekijima, M. Interaction-constrained 3D molecular generation using a diffusion model enables structure-based pharmacophore modeling for drug design. npj Drug Discov. 3, 8 (2026). https://doi.org/10.1038/s44386-026-00040-x
Anahtar kelimeler: yapıya dayalı ilaç tasarımı, moleküler üretken modeller, farmakofor modelleme, protein–ligand etkileşimleri, SARS-CoV-2 ana proteazı