Clear Sky Science · tr
Yapay zekâ yönlendirmeli rekabetçi doklama ile sanal tarama ve bileşik etkinliği tahmini
Yeni İlaçlar İçin Daha Akıllı Aramalar
Yeni ilaçlar bulmak, milyonlarca molekülden oluşan bir samanlıkta iğne aramaya benzer. Bu çalışma, yapay zekâdaki son ilerlemelerin, hangi moleküllerin hastalıkla ilişkili bir proteine yapışma olasılığının yüksek olduğunu ve gerçekten ilaç olarak işe yarayabileceğini tahmin ederek bu aramayı nasıl daha hızlı ve ucuz hale getirebileceğini gösteriyor. Yazarlar, laboratuvarda bir kimyasalı birer birer test etmek yerine, AI modellerini moleküller arasında sanal yarışmalar yürütmek ve kazananların öne çıkmasını sağlamak için kullanıyorlar.
Yapay Zekâ Moleküler Kilit-Uyumu Nasıl Öğrenir
Birçok modern ilaç, bir anahtarın kilide girmesi gibi proteinlerin üzerindeki küçük ceplere oturarak işe yarar. Geleneksel olarak bilgisayar programları, atomlar arasındaki kuvvetleri tahmin eden fiziksel denklemler kullanarak bu uyumu kestirmeye çalıştı. Son birkaç yılda ise AlphaFold3 ve Boltz gibi difüzyon tabanlı birlikte-katlanan modellere sahip yeni AI sistemleri, çok sayıda bilinen protein–molekül yapısından öğrenerek gelişti. Bu sistemler artık deneysel bir yapı olmasa bile bir proteinin ve potansiyel bir ilacın üç boyutta nasıl birlikte katlanabileceğini “hayal edebiliyor”. Yazarların ele aldığı temel soru, bu AI araçlarının sadece makul görüntüler çizmekten daha fazlasını yapıp yapamayacağı — iyi ilaçları kötü olanlardan ayırt edip edemeyecekleri.
Gerçek Bağlayıcılar ve Taklitçiler
Ekip önce iyi incelenmiş 16 proteini ve daha karmaşık bir bakteriyel enzim olan DNA girazı test etti. Her protein için AI modellerinden hem bilinen etkin inhibitörleri hem de ilişkili olmayan “hedef-dışı” molekül setini aynı bağlanma bölgesine yerleştirmelerini istediler. Tek bir tahmine güvenmek yerine, AI’nin her molekülü birçok çalışmada ne kadar tutarlı yerleştirdiğine baktılar. Gerçek inhibitörler aynı konuma ve yönelime tekrar tekrar dönme eğilimindeydi; birbirlerine birkaç trilyonda metre içinde kümeleniyorlardı. Etkisiz moleküller daha geniş dolaşıyor ve sık sık cebin uzağında konumlanıyordu. Bu basit fikir — poz yakınsaması — bir bileşiğin gerçekten hedef proteine uyup uymadığına dair güçlü bir sinyal olduğu ortaya çıktı.
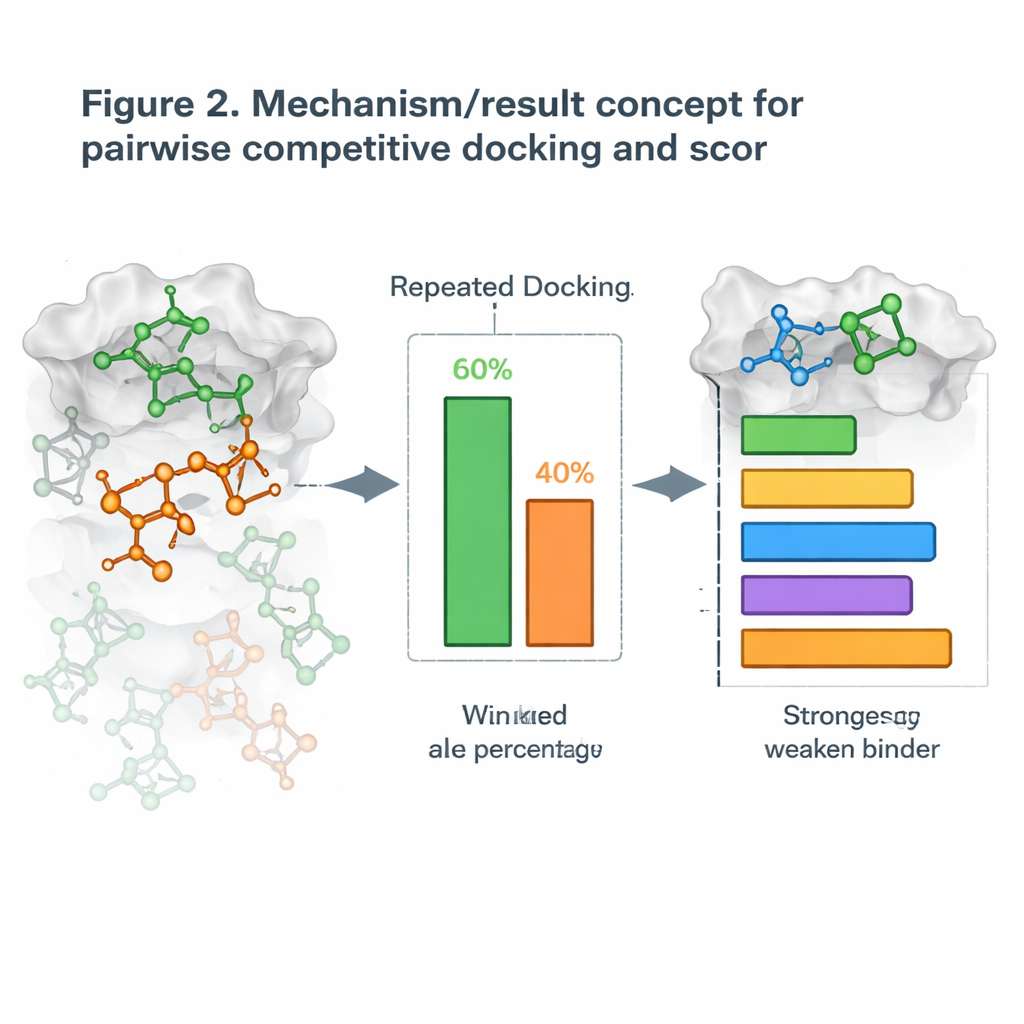
Doklamayı Kafa Kafaya Yarışmaya Çevirmek
Bunun üzerine yazarlar eşleştirmeli rekabetçi doklama adını verdikleri yeni bir strateji tanıttılar. Bir kerede bir molekül doklamak yerine, iki adayı proteinle birlikte doklayıp aynı cep için “rekabet etmelerine” izin veriyorlar. Birçok tekrarlı çalışmadan sonra bölgeyi daha sık işgal eden molekül o eşleşmenin kazananı ilan ediliyor. Tüm olası eşleştirmeleri çalıştırarak bir galibiyet-mağlubiyet tablosu oluşturuyor ve bir turnuva sıralaması gibi her molekül için Rekabetçi Doklama Skoru hesaplıyorlar. Bu skorlar, moleküllerin gerçek dünyadaki hedeflerini ne kadar güçlü bloke ettiklerine dair ölçümlerle karşılaştırıldığında sıralamalar sıklıkla iyi örtüştü; bazı protein sistemlerinde anlaşma neredeyse mükemmele yakındı.
Sanal Taramalardan Daha İyi Antibiyotik Tasarımına
Bakteriler için hayati öneme sahip bir enzim olan DNA girazı ayrıntılı bir test vakası olarak kullanıldı. Bu proteinin, yaygın olarak kullanılan florokinolonlar da dahil olmak üzere farklı antibiyotik sınıflarının hedeflediği birkaç ilaç cebi var. AI modelleri genellikle her ilaç sınıfını doğru cebe yerleştirebildi ve rekabetçi doklama skorları ölçülen potansiyellerini kabaca izledi. Yazarlar daha sonra florokinolon bölgesi için hangilerinin en iyi rekabet ettiğini görmek üzere 3.000’den fazla onaylı ilacı içeren bir sanal taramaya ölçeklendirdiler. İki aşamalı stratejileri — önce “hepsi bir arada” rekabetiyle olası kazananları seçmek, ardından ceptede ne kadar sıkı kümelendiklerine göre filtrelemek — gerçek florokinolonları önemli ölçüde zenginleştirirken daha zayıf adayları eledi. Son olarak, AI destekli bir molekül üreticisi kullanarak yeni florokinolon benzeri yapılar önerdiler ve rekabetçi doklamayı uygulayarak daha iyi tahmini bağlanma ve kabul edilebilir ilaç-benzeri özelliklere sahip bir avuç aday buldular.
Sözler, Sınırlar ve Hastalar İçin Anlamı
Çalışma, modern AI modellerinin yalnızca makul protein–ilaç yapıları çizmekle kalmayıp; rekabetçi bir çerçevede çalıştırıldıklarında bileşikleri genellikle gerçek deneysel verilerle paralel şekilde sıralamalarına yardımcı olabileceğini gösteriyor. Bu laboratuvar çalışmalarının yerini almaz — performans hâlâ belirli proteine güçlü biçimde bağlıdır, bazı cepler yanlış tahmin edilebilir ve AI modelleri çok büyük veya alışılmadık moleküller için başarısız olabilir. Ancak bu modeller ve eğitim verileri geliştikçe, eşleştirmeli rekabetçi doklama gibi yaklaşımlar erken aşama ilaç keşfini çok daha verimli hâle getirebilir. Hastalar için bu, zamanla hedefe yönelik ilaçların, dirençli bakterilere karşı yeni antibiyotiklerin daha hızlı geliştirilmesine dönüşebilir.
Atıf: Mirgaux, M., Barcelli, V., Chua, A.C.Y. et al. AI-guided competitive docking for virtual screening and compound efficacy prediction. npj Drug Discov. 3, 6 (2026). https://doi.org/10.1038/s44386-026-00039-4
Anahtar kelimeler: Yapay zekâ ile ilaç keşfi, sanal tarama, moleküler doklama, protein-ligand bağlanması, antibiyotik tasarımı