Clear Sky Science · tr
Logic-kısıtlı gen-yol heterojen bilgi grafiği aracılığıyla histopatolojik görüntülerden sinyal yolak anormalliklerini çıkarma
Kanser Lamları İçindeki Gizli Hücresel Sinyalleri Görmek
Hekimler kanseri mikroskop altında incelediklerinde çoğunlukla şekil ve renkleri görürler; hücrelerin içindeki karmaşık moleküler “konuşmaları”yı değil. Oysa genler ve yolaklar arasındaki bu görünmez sinyalleşme «konuşmaları» sıklıkla bir tümörün nasıl büyüdüğünü ve tedaviye nasıl yanıt verebileceğini belirler. Bu çalışma, rutin patoloji görüntülerini okuyup hangi hücresel iletişim yollarının—yani yolakların—bozulduğunu çıkaran yeni bir yapay zekâ sistemi tanıtıyor; böylece ek laboratuvar testleri olmadan moleküler davranışa bir pencere açıyor.
Tek Gen İpuçlarından Daha Büyük Resme
Geleneksel yaklaşımlar doku görüntülerinden tekil genlerin durumunu tahmin etmeye çalışır: belirli bir gen mutasyonlu mu, değil mi? Bu faydalı olmakla birlikte, kanser nadiren tek bir hatalı gene bağlıdır. Bunun yerine gen grupları birlikte çalışarak büyüme, hayatta kalma ve bağışıklığı kontrol eden tüm sinyal yolaklarını bozar. Yazarlar, tek genlere odaklanmanın bu işbirlikçi davranışı kaçırdığını ve tümörlerin mikroskop altında neden göründüğünü ve davrandığını açıklamada yetersiz kalabileceğini savunuyor.
Görüntüler, Genler ve Yolaklar Arasında Bir Harita Oluşturmak
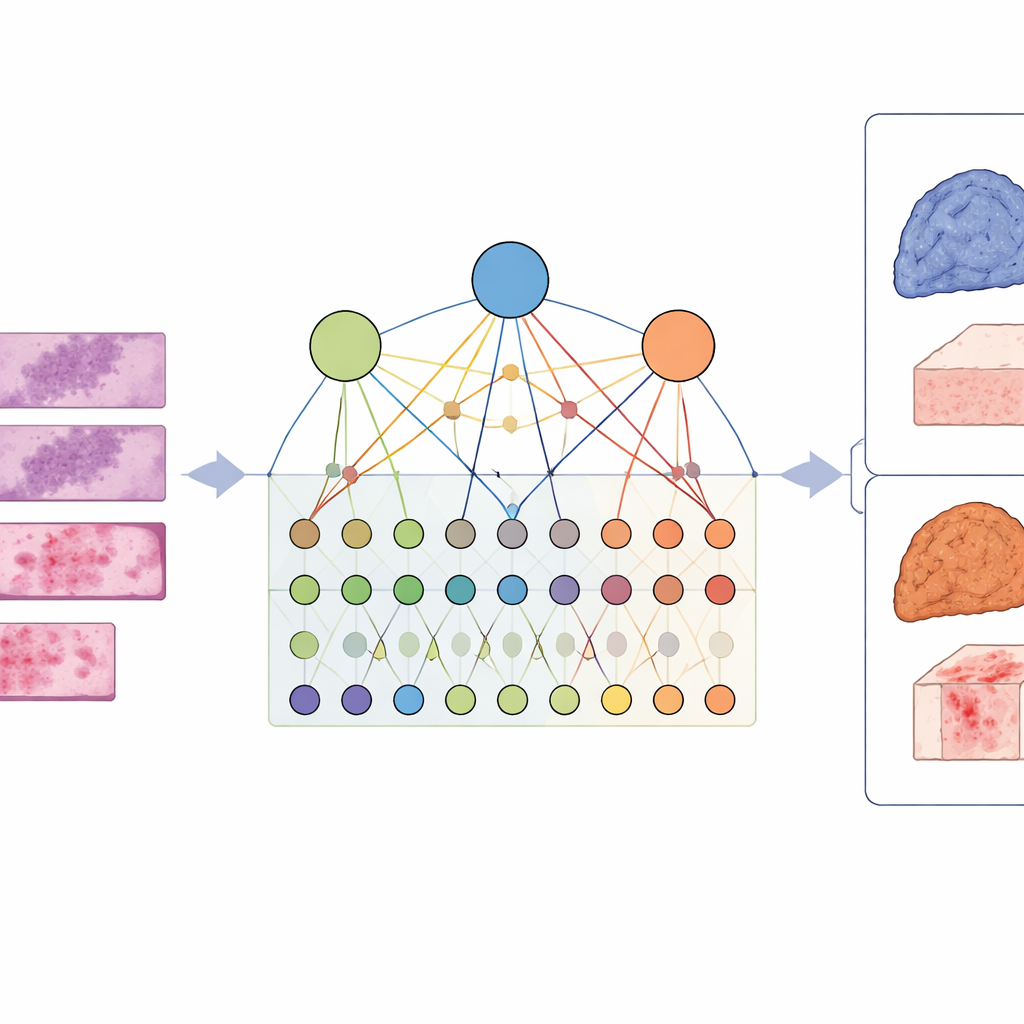
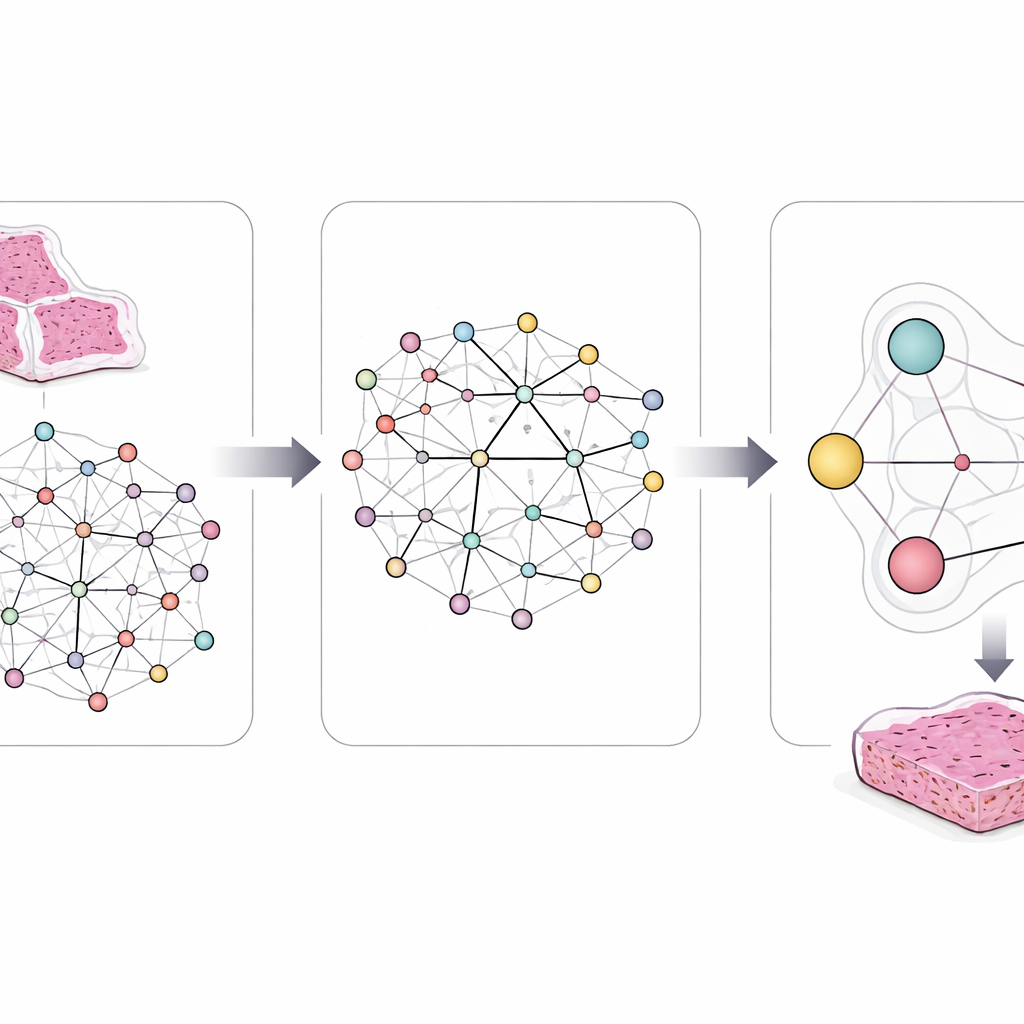
Bu karmaşıklığı yakalamak için araştırmacılar LCG-HGNN adlı, üç bilgi katmanını birbirine bağlayan bir çerçeve tasarladı. Önce akciğer adenokarsinomunun her tam-lama görüntüsünü birçok küçük yama hâline bölüp bu yamaları yakın veya benzer görünen bölgelerin bağlantılı olduğu bir grafik olarak temsil ettiler. İkinci olarak, bilinen biyolojik veritabanlarını kullanarak gen işaretleyicilerini sinyal yolaklarına bağladılar ve hangi genlerin hangi yolaklara ait olduğunu kodlayan ikinci bir grafik oluşturdular. Son olarak, yapay zekâ modeli bu birleşik grafik boyunca bilgi akışına izin vererek görüntü desenlerinin, genlerin ve yolakların birbirini etkilemesini sağladı; bunları ayrı ayrı ele almak yerine etkileşim içinde değerlendirdi.
Sisteme Bilinen Biyolojiyi Öğretmek
Ana yenilik, modelin rehbersiz serbestçe öğrenmesine izin verilmemesi. Yazarlar onlarca yıllık kanser araştırmasından türetilmiş açık, kural benzeri ifadeleri gömüyor. Örneğin bazı mutasyonlar aynı tümörde neredeyse hiç birlikte görülmez ve bazı yolaklar diğerlerinin yukarısında veya aşağısındadır. Bu tür kuralları yapay zekânın iç bağlantılarını ve tahminlerini nazikçe yönlendiren mantıksal kısıtlar olarak kodluyorlar. Model, bilinen biyolojiyle veya hastaların lamları arasındaki benzerliklerle çelişen bir gen ve yolak değişiklikleri kombinasyonu önerirse, bu kurallar onu daha gerçekçi alternatiflere itiyor.
Mevcut Yöntemlere Karşı Doğruluğu Test Etmek
Ekip, sistemlerini genetik verilerle ilişkilendirilmiş 1.600’den fazla akciğer kanseri lamı üzerinde değerlendirdi. Bunu tek genlere odaklanan standart derin öğrenme modelleri ve yolak yapısını göz ardı eden ancak çok sayıda geni aynı anda işleyen daha gelişkin yöntemlerle karşılaştırdılar. Hücre büyüme sinyallerini ve dokunun destek iskeletini içeren önemli yolaklar da dahil olmak üzere birkaç önemli yolda, yeni model gen grubu değişikliklerini ve yolak anormalliklerini daha doğru tahmin etti. Ayrıca görünümü, belirli mutasyonlarla ilişkilendirildiği bilinen gerçek klinik örneklere yakından uyan görüntü yamaları üretti; bu da modelin anlamsız görüntü özellikleri yerine anlamlı mikroskobik desenlere odaklandığını düşündürüyor.
Bu Hastalar İçin Neden Önemli
Uzman olmayan biri için temel sonuç şudur: bu yaklaşım rutin bir patoloji lamını zengin bir moleküler içgörü kaynağına dönüştürüyor. Her olası hedef için ayrı ve sıklıkla maliyetli genetik testler sipariş etmek yerine, doktorlar gelecekte böyle modelleri zaten topladıkları görüntülerden doğrudan bozulmuş yolakları taramak için kullanabilirler. Yöntemin hâlâ daha geniş, gerçek dünya doğrulamasına ihtiyacı var ve henüz genomik testi tamamen ikame etmiyor; ancak mikroskop görüntüsünün tümörün iç devrelerine bakan bir pencereye dönüşebileceği—daha kesin ve biyolojik olarak bilgilendirilmiş kanser bakımını yönlendirmede yardımcı olabileceği—bir geleceğe işaret ediyor.
Atıf: Yu, Y., Shi, W., Chen, X. et al. Inferring signaling pathway abnormalities from histopathological images via logic-constrained gene-pathway heterogeneous knowledge graph. npj Biomed. Innov. 3, 23 (2026). https://doi.org/10.1038/s44385-026-00078-6
Anahtar kelimeler: kanser yolakları, histopatoloji yapay zekâsı, graf sinir ağları, akciğer adenokarsinomu, dijital patoloji