Clear Sky Science · tr
Katı tümörlerin tedavisi için bakteriyel mühendisliği bilgilendirmek amacıyla in vitro ko-kültür modellerinin kullanımı
Kanserde bakterilerin sizin için neden önemli olabileceği
Cerrahi, kemoterapi ve radyoterapi gibi kanser tedavileri hayat kurtarıyor ancak genellikle ağır yan etkilere ve sıklıkla tedavi başarısızlığına yol açabiliyor. İlginç bir yeni fikir, yaşamakta olan bakterileri katı tümörleri içeriden bulup hedef alan hassas araçlar olarak kullanmak. Bu makale, insan hücreleri ve bakterilerin birlikte büyüdüğü laboratuvar test sistemlerinin—hastalara ulaşmadan önce daha güvenli ve daha akıllı bakteriyel tedaviler tasarlamak için—bilim insanları tarafından nasıl kurulduğunu açıklıyor.
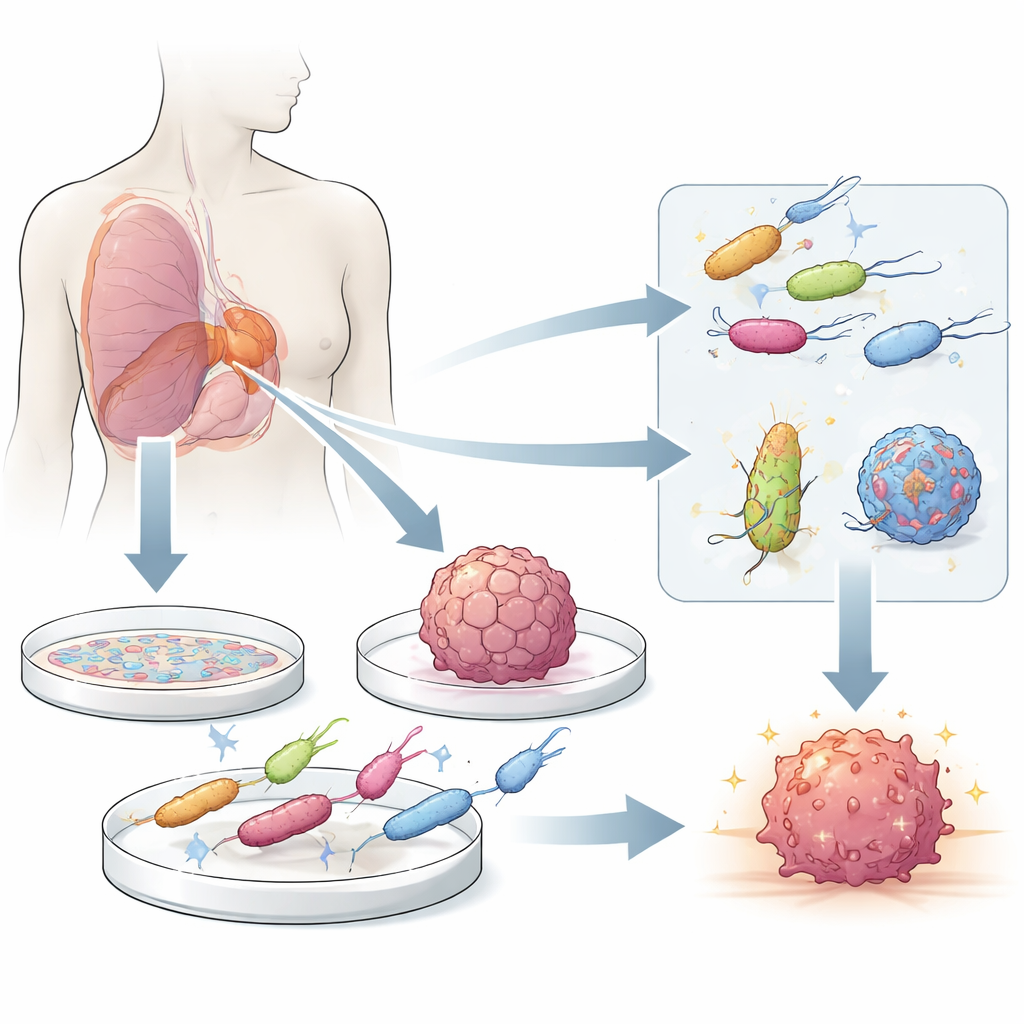
Tümörleri bulan küçük yardımcılar
Belli bakteriler doğal olarak sağlıklı dokuların üzerinde, katı tümörlerin içindeki zorlu, oksijenden yoksun ortamı tercih eder. Sızan tümör kan damarlarından geçerek veya bağışıklık hücreleriyle taşınarak tümöre giren bu mikroplar, tümör çekirdeğindeki ölü ve ölmekte olan hücrelere doğru hareket eder; burada çoğalabilir ve bazen kanser hücresi ölümünü ve yerel bağışıklık saldırılarını tetikleyebilirler. Modern genetik mühendisliği, bu doğal “tümör-homing” suşlarını ilaçlar, bağışıklık uyarıcıları veya diğer yükleri doğrudan ihtiyaç duyulan yere teslim edebilen canlı taşıyıcılara dönüştürüyor; zararlı özelliklerini zayıflatma çabaları ise güvenliği artırıyor.
Gerçeğe yakın laboratuvar mini-tümörleri oluşturmak
Bu yaşayan ilaçları anlamak ve geliştirmek için, bilim insanlarının vücutta olup biteni mümkün olduğunca yakından taklit eden test yataklarına ihtiyacı var. Basit düz hücre katmanları yetiştirmesi kolay ve hızlı tarama için faydalıdır, ancak gerçek tümörlerin karmaşık yapısını ve oksijen gradyanlarını kaçırır. Kanser hücre hattından yapılmış sferoidler ve hasta dokusundan geliştirilen organoidler gibi üç boyutlu modeller, canlı bir dış kabuk, sessiz bir iç bölge ve ölü bir çekirdek gibi anahtar özellikleri daha iyi yeniden üretir. Bakteriler bu mini-tümörlerle doğrudan karıştırıldığında, araştırmacılar onların nasıl işgal ettiğini, nerede biriktiğini ve mühendislik ürünü ilaç devrelerinin hasta tümörüne benzeyen koşullarda ne kadar iyi çalıştığını izleyebilirler.
Sinyalleri incelemek için hücreleri ayırmak
Diğer ko-kültür tasarımları fiziksel temastan daha çok bakteriler ve insan hücreleri arasındaki görünmez kimyasal alışverişe odaklanır. Transwell sistemlerinde gözenekli bir zar iki odacığı böler, böylece küçük moleküller geçerken hücreler yerinde kalır. Bu, örneğin bir bakteri suşunun zararsız bir bileşiği tümör öldürücü bir gaza dönüştürmesini ve bu gazın yakınlardaki kanser hücrelerine difüze olduğunu test etmeyi sağlar. Mikroakışkan çipler—kanallar ve bölmeler içeren küçük cihazlar—gerçekçiliğe başka bir katman ekler. Akış, oksijen düzeyleri ve zamanlamayı kontrol edebilir; mühendislikli bakterilerin büyümesini, senkronize döngülerle patlamasını ve kanser hücrelerini terapötik moleküllerle tekrar tekrar yıkamasını sağlayarak her iki tarafın zaman içindeki yanıtlarını yakından izlemeye olanak tanır.
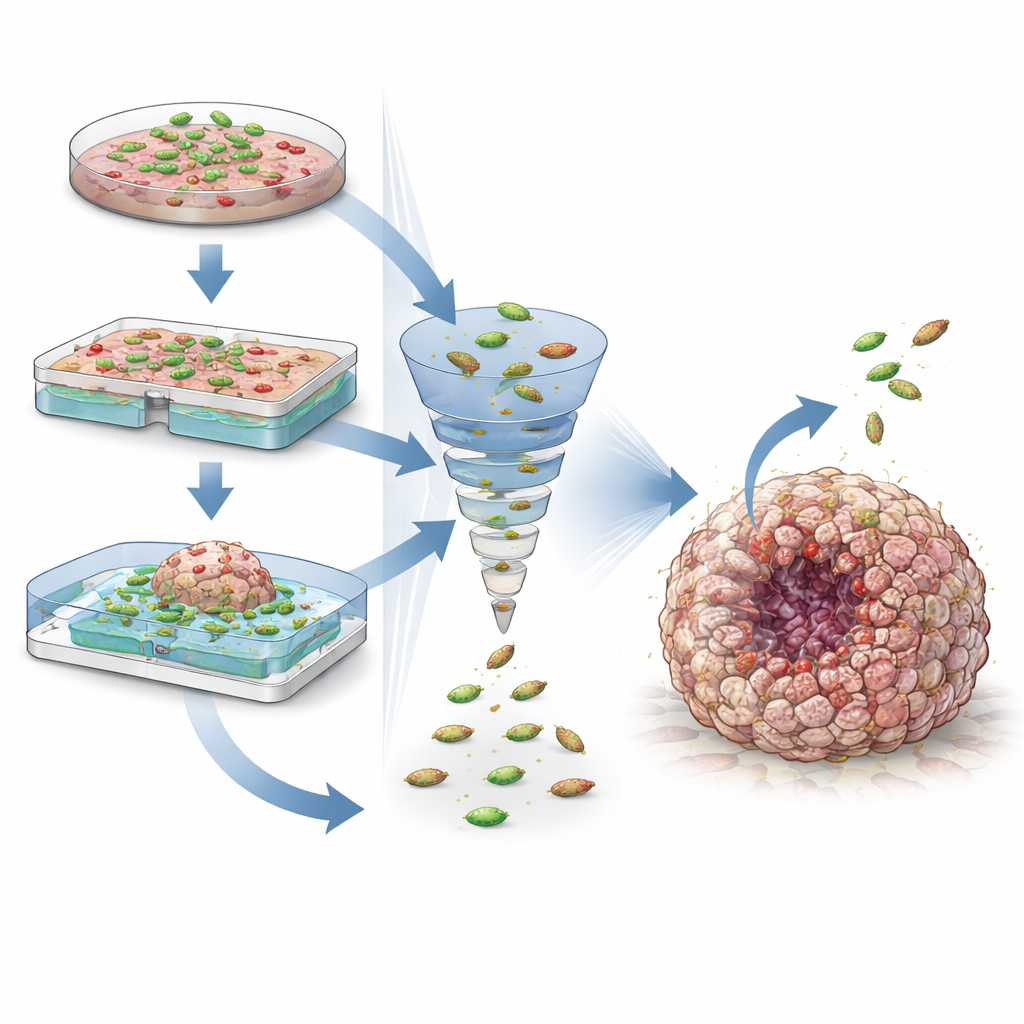
Tümör ekosisteminin içini görmek
Ko-kültür modelleri, bakterilerin daha geniş tümör ekosistemiyle nasıl etkileştiğini incelemek için de kullanılıyor. Bireysel hastalardan türetilen organoidler, orijinal tümörlerinin birçok genetik özelliklerini ve ilaç yanıtlarını koruyabilir; bu da bakteriyel terapilerin kişiselleştirilmiş testine kapı açar. Bu kültürlere bağışıklık hücreleri eklemek, bakterilerin anti-kanser bağışıklığını nasıl güçlendirebileceğini veya bastırabileceğini ve bunların checkpoint inhibitörü ilaçlarla nasıl birleşebileceğini ortaya koyar. Aynı zamanda bu modeller, DNA'ya zarar verip başlangıçta kansere katkıda bulunabilecek bakteriyel toksinler gibi güvenlik endişelerini de işaretler. Kültür koşullarını, oksijen düzeylerini ve canlı görüntülemeden DNA dizilemeye kadar ölçüm yöntemlerini ayarlayarak araştırmacılar bu faydaları ve riskleri sistematik olarak keşfedebilirler.
Laboratuvardan hasta yatağına
Heyecan verici hayvan sonuçlarına rağmen, çok az bakteriyel kanser terapisi insan denemelerinde açık faydalar göstermiştir. Yazarlar, ko-kültür sistemlerinin daha akıllıca kullanılmasının bu boşluğu kapatabileceğini savunuyor. Hasta-ila hasta farklılıklarını, tümör karmaşıklığını ve önceki tedavileri daha iyi yakalayarak bu modeller en umut verici mühendislikli suşları, bunları mevcut ilaçlarla nasıl birleştireceğimizi ve nerede başarısız olabileceklerini belirleyebilir. Ayrıca laboratuvarların dünya çapında sonuçları karşılaştırabilmesi ve düzenleyicilerin güvenlik ile etkinliği daha emin biçimde değerlendirebilmesi için paylaşılan standartlara ihtiyaç olduğunun altını çiziyorlar. Basitçe söylemek gerekirse, bakterilerle yan yana yetiştirilen dikkatle tasarlanmış laboratuvar mini-tümörleri, bu “akıllı böcekleri” rafine etmenin güçlü bir yolunu sunuyor; bu da gelecekteki hastaların hem daha güvenli hem de daha etkili bakteriyel terapiler alma olasılığını artırıyor.
Atıf: Foschini, S., Wright, J.A., Woods, S.L. et al. Use of in vitro co-culture models to inform bacterial engineering for the treatment of solid tumours. npj Biomed. Innov. 3, 21 (2026). https://doi.org/10.1038/s44385-026-00075-9
Anahtar kelimeler: bakteriyel kanser terapisi, tümör organoidleri, ko-kültür modelleri, sentetik biyoloji, tümör mikroçevresi