Clear Sky Science · tr
Kanser immünoterapisi için makrofajların mühendisliği: ortaya çıkan bulgular ve terapötik potansiyel
Vücudun Temizlik Ekibini Kanserle Savaşan Hücrelere Dönüştürmek
Vücudumuz, mikropları ve ölü dokuları yutan gezici “temizlik” hücreleri olan makrofajlarla dolu. Bu derleme, bilim insanlarının bu hücreleri kanserle savaşacak şekilde nasıl yönlendirmeyi öğrendiğini inceliyor. Makrofajlar tümörler içinde bol bulunduğundan—bugünün önde gelen immünoterapilerine dirençli olanlarda bile—onları anlamak ve mühendislik yapmak, zor tedavi edilen kanserli hastalar için yeni seçenekler açabilir.
Tek Bir Hücre Tipinin Çok Yüzü
Makrofajlar tek, sabit bir hücre tipi değildir; şekil değiştiren varlıklardır. Kanda dolaşarak gelebilirler ya da dokularda yerleşik olabilirler ve yerleştikten sonra yerel sinyallere yanıt verirler. Tümörlerde, tümöre bağlı makrofajlar ya kanser hücrelerini öldürmeye yardımcı olabilir ya da kafa karıştırıcı biçimde tümörlerin büyümesine ve yayılmasına destek verebilir. Önceki araştırmalarda bunları iki kutuya—“M1” (saldırı modu) ve “M2” (onarım veya destek modu)—sığdırmaya çalıştılar. Yeni genetik ve mekansal haritalama araçları şimdi çok daha zengin bir durum spektrumu gösteriyor; birden fazla alt grup ve davranış var ve bunlar tümöre ve konuma göre değişiyor. Bir zamanlar kesinlikle “tümör yanlısı” olduğu düşünülen hücreler bile, bazı bağlamlarda T hücrelerini harekete geçirip anti-kanser bağışıklığı destekleyebilir.
Çevrelerini Hissetmek ve Kanser Hücrelerini Yutmak
Makrofajlar sadece kimyasal sinyalleri dinlemez; çevrelerindeki fiziksel dünyayı da hissederler. Bir tümörün yoğun protein ağında sürünürken, hücreler arasından sıkışıp geçerken ve sıvı kuvvetlerine maruz kalırken, Piezo1 gibi özelleşmiş reseptörler aracılığıyla sertlik ve gerilimi algılarlar. Bu mekanik ipuçları, klasik bağışıklık sinyalleriyle birlikte, makrofajları daha iltihaplı ya da daha yatıştırıcı rollere eğebilir. İşlevsel olarak makrofajlar kanser hücrelerini yutup sonra onları parçalayıp fragmanları (antijenleri) T hücrelerine sunarak doğuştan gelen ve edinilmiş bağışıklık arasında köprü kurabilir. Kanser hücreleri, yüzeydeki CD47 gibi bir molekül aracılığıyla makrofajlarda bir frenle bağlanan “beni yeme” sinyalleri göndererek karşı koyar. Bu etkileşimi engelleyen ilaçlar birçok klinik çalışmada yer alıyor; kanser hücresi temizliğini artırıyorlar ama sağlıklı hücrelere zarar vermemek için dikkatli ayarlama gerektiriyorlar.
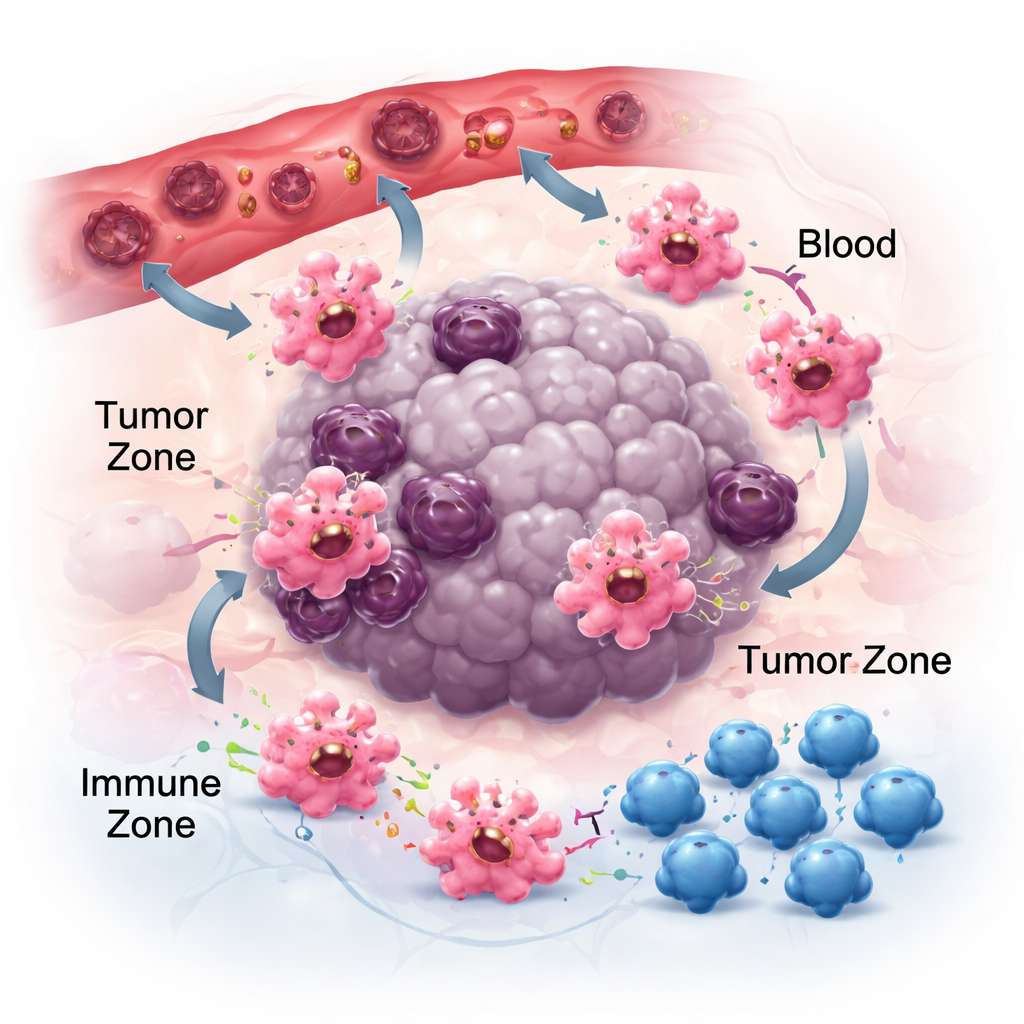
Tümör Mahallesinde Hareket Etmek, Yapışmak ve İletişim Kurmak
Kanserde etkili olmak için makrofajların önce tümörlere ulaşması, sonra da doğru nişlere yerleşmesi gerekir. Kanser ve çevreleyen hücreler tarafından salınan kemokinler ve büyüme faktörleri gibi kimyasal izleri takip ederler. CCR2–CCL2 çiftleri gibi etkileşimler onları tümörlere çeker ve bu sinyalleri engelleyen ilaçlar makrofaj birikimini azaltabilir; yine de tamamen kesmez, bu da CSF-1 ve VEGF gibi diğer çekicilerin varlığına işaret eder. Yerleştikten sonra makrofajların yerel matrise nasıl yapıştığı da davranışlarını şekillendirir. İntegrin adı verilen adezyon reseptörleri sadece yapıştırıcı gibi davranmaz; iltihaplanma sinyallerini güçlendirir ve hücreleri daha tümörle savaşan hallere yönlendirebilir. Aynı zamanda makrofajlar, RNA ve protein taşıyan küçük paketler olan ekstrasellüler veziküller salarlar; bunlar yakın hücrelere mesaj taşır. Tümör tipine bağlı olarak bu veziküller bağışıklığı köreltip yayılmaya yardımcı olabilir ya da anti-tümör yanıtları güçlendirebilir; bu da makrofaj iletişiminin bağlama bağımlı doğasını vurgular.
Genler ve Materyallerle Makrofajları Yeniden Programlamak
Makrofajlar katı tümörlere birçok T hücresinden daha iyi nüfuz ettiğinden, araştırmacılar şimdi onları canlı ilaçlar olarak yeniden tasarlıyor. Genetik bir strateji, kimerik antijen reseptörü (CAR) T hücre terapisinden ödünç alır: sentetik bir reseptör ekleyerek CAR makrofajlar (CAR-M) oluşturmak. Bu tasarım hücreleri tümör belirteçlerini tanır, kanser hücrelerini daha verimli yutar, çevreleyen matrisi sindirir, iltihaplı sinyaller salar ve tümör antijenlerini sunarak T hücrelerini aktive eder. HER2 hedefli CAR-M’lerin erken insan deneyleri güvenlik ve biyolojik aktivite açısından cesaret verici sonuçlar gösterse de güçlü, kalıcı faydaları kanıtlamak için daha fazla çalışma gerekiyor. Paralel olarak, genetik olmayan yaklaşımlar lipitler veya polimerlerden yapılmış partiküller ve “sırt çantaları” kullanır. Makrofajlar ilaç yüklü nanoparçacıkları yutabilir ve Truva atı gibi derin tümörlere taşıyabilir veya yüzeye tutturulmuş yamalar takarak immün güçlendirici sinyalleri yavaşça serbest bırakabilir; bu, içlerini aşırı yüklemeden onların tümörle savaşan bir kimliğini korumalarına yardımcı olur. Makrofaj kaynaklı veziküller de doğal, hücresiz taşıyıcılar olarak test ediliyor.
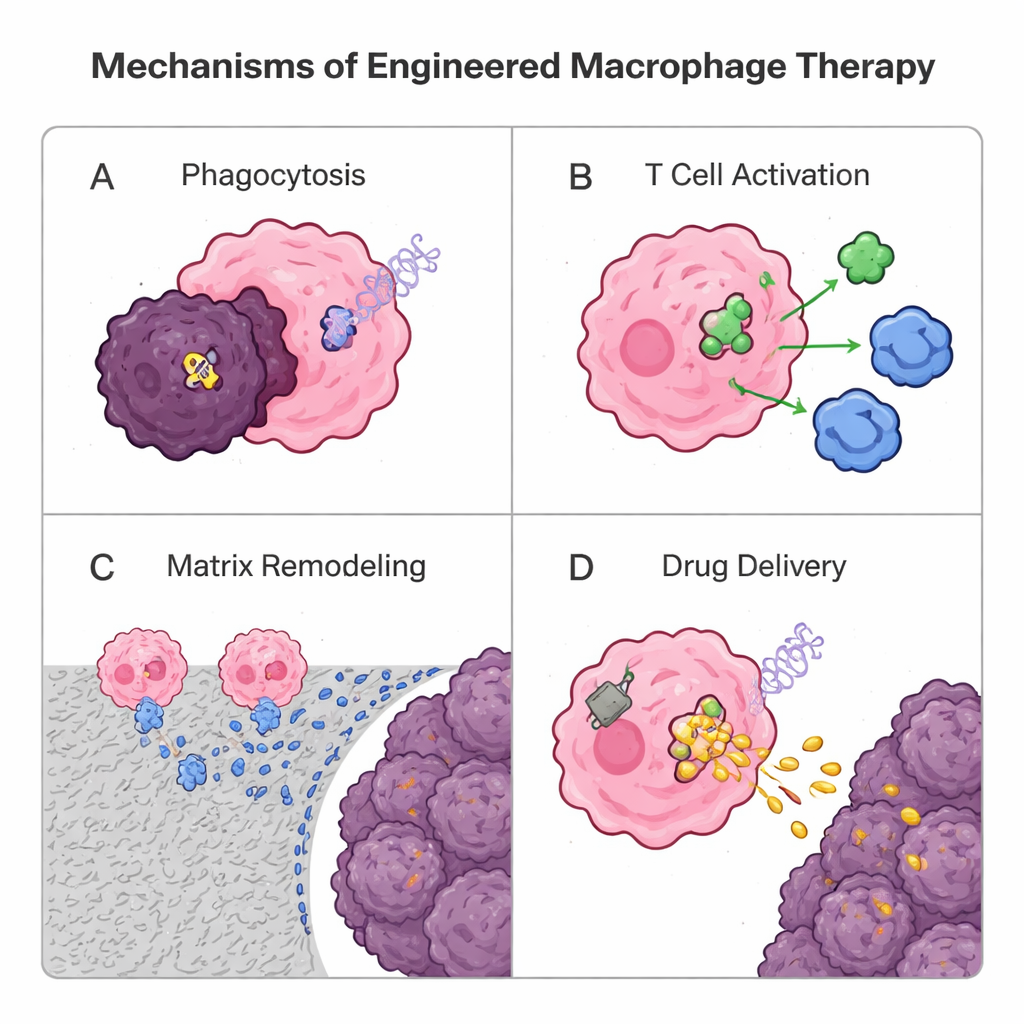
Önümüzdeki Zorluklar ve Umut İçin Nedenler
Vaadlerine rağmen makrofaj terapileri pratik engelleri aşmak zorunda. Hastalardan yeterli tutarlılıkta hücre üretmek zaman alıcı ve maliyetlidir ve infüze edildiklerinde bu hücreler sonsuza dek yaşamaz veya çoğalmazlar. Doğuştan gelen esneklikleri biyolojik olarak faydalı olsa da, karmaşık ve baskılayıcı tümör mikroçevresinde onları anti-tümör modunda tutmayı zorlaştırabilir. Yazarlar, gelişmiş biyomühendislik modellerinin—gerçek doku mekaniğini taklit eden 3B kültürler, organoidler ve organ-on-a-chip sistemlerinin—mühendislenmiş makrofajların hastalardaki davranışını anlamak ve öngörmek için kritik olacağını savunuyorlar. Yine de, katı tümörlere girme, kanser hücrelerini yutma ve T hücrelerini uyandırma konusundaki doğal yetenekleri ile erken güvenlik verileri, özellikle şu anda çoğu immün tedaviye dirençli olan “soğuk” tümörlere karşı, makrofaj tabanlı terapilerin önemli yeni bir silah olabileceğini düşündürüyor.
Atıf: Block, A., Liu, X., Zhang, D. et al. Engineering macrophages for cancer immunotherapy: emerging insights and therapeutic potential. npj Biomed. Innov. 3, 18 (2026). https://doi.org/10.1038/s44385-026-00072-y
Anahtar kelimeler: makrofaj immünoterapisi, tümör mikroçevresi, CAR makrofajlar, fagositoz, nanosunun taşıma ile ilaç verme