Clear Sky Science · tr
Canlı ortamda glikoz düzeylerini sürekli izlemek için mikro-organ temelli bir mikroakışkan biyosensör
Bu neden diyabetliler için önemli
Tip 1 diyabetle yaşayan kişiler için günümüzdeki “yapay pankreas” sistemleri hâlâ sürekli dikkat gerektiriyor—yemeklerin bildirilmesi, alarmların yönetilmesi ve gece hipoglisemi endişesi gibi. Bu çalışma, tek bir enzim ya da bilgisayar denklemi yerine vücudun kendi şeker kontrol mekanizmasının küçük, canlı bir parçasını ödünç alan radikal olarak farklı bir glikoz sensörünü araştırıyor: adacıklar olarak adlandırılan pankreas hücresi kümeleri. Bu mini-organların evrim boyunca optimize ettikleri işi yapmasına izin vererek, araştırmacılar daha akıllı, daha güvenli glikoz izleyicileri inşa etmeyi ve bir gün arka planda daha bağımsız çalışabilecek cihazlar geliştirmeyi hedefliyor.
Canlı bir sensör olarak küçük bir organ
Mevcut biyosensörlerin çoğu, kimyasalları saflaştırılmış moleküller veya tek hücre dizileri kullanarak tespit eder. Bunlar tek bir maddeye tepki verir ve ham sinyali yorumlamaya çalışan yazılıma iletir. Yazarlar bu yaklaşımın güçlü, yerleşik bir “bilgisayarı” göz ardı ettiğini savunuyor: birden fazla sinyali aynı anda doğal olarak algılayıp bunları koordine bir yanıta dönüştüren mikro-organlar, örneğin pankreas adacıkları. Her adacık, sürekli birbirleriyle iletişim halinde olan birkaç hormon üreten hücre tipini içerir. Birlikte glikozun yanı sıra amino asitler, bağırsak ve stres hormonları ile vücudun yakın geçmişteki yüksek/düşük durumlarına da yanıt vererek kan şekerini dar ve güvenli bir aralıkta tutarlar. Yazarlar, bu yerleşik karmaşıklığın basit bir glikoz oksidaz sensöründen daha zengin ve daha güvenilir bilgiler üretecek şekilde kullanılabileceğini öne sürüyor.
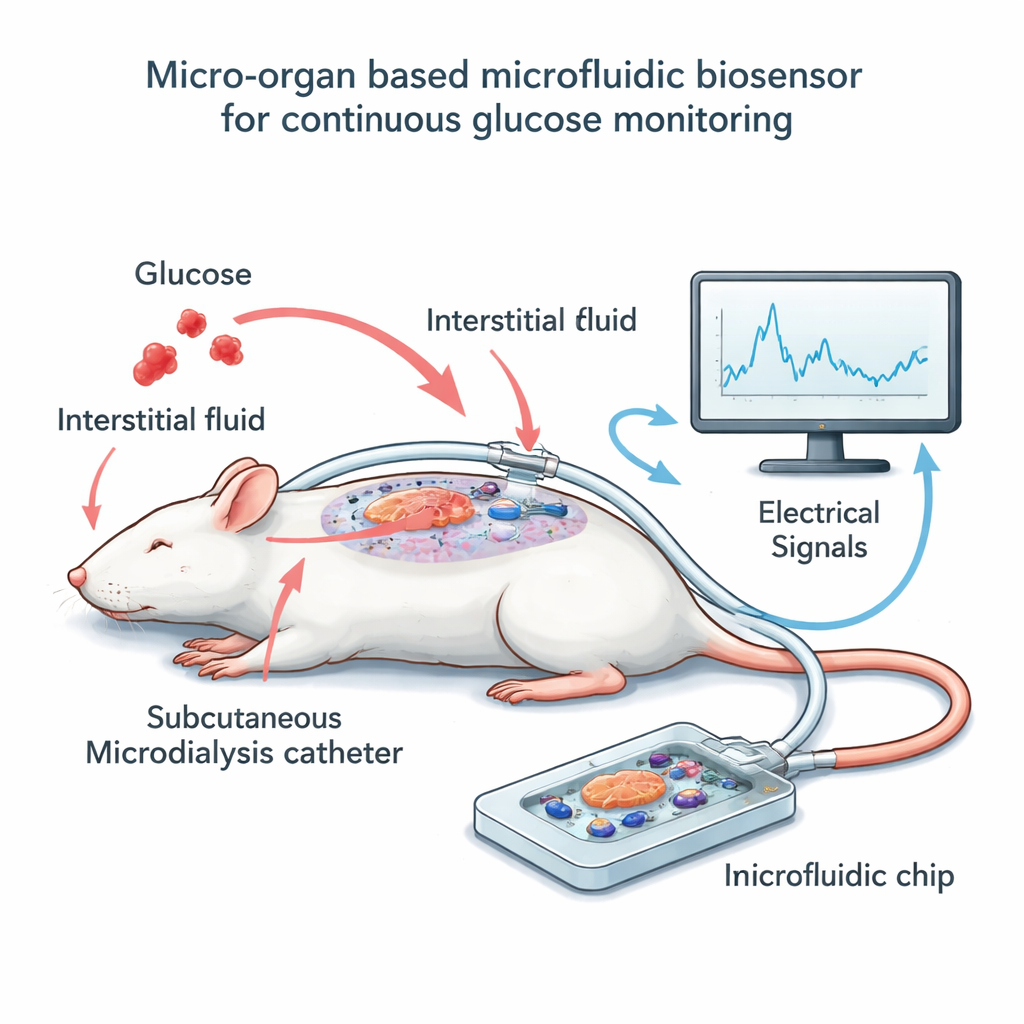
Çip ve kateter sisteminin inşası
Bu fikri test etmek için ekip, birkaç düzine fare adacığını mikroskobik elektrot ızgarasının üzerinde barındıran vücut dışı küçük bir cihaz inşa etti. Bu hücreleri doğrudan kanla yıkamak yerine mikrodiyaliz adı verilen bir teknik kullandılar: ince, esnek bir kateter anestezi altındaki sıçanların derisinin hemen altına yerleştirilir ve çevre doku sıvısını yavaşça toplar; bu sıvı kan şekerini kısa bir gecikmeyle yakından izler. Düşük, sabit bir akış bu sıvıyı çip üzerindeki adacıkların üzerinden dar bir kanal boyunca taşır. Dializat içindeki glikoz seviyeleri yükselip düştükçe adacıkların elektriksel aktivitesi değişir ve elektrotlar bunu yavaş, dalga benzeri sinyaller olarak yakalar. Paralel olarak, araştırmacılar periyodik olarak sıçanların kanında ve dializatta glikoz ölçerek elektriksel çıktıyı gerçek şeker seviyeleriyle zaman içinde hizalayabildiler.
Canlı sensörün değişen şekere tepkisi
Önce bilim insanları, elektrotlar üzerindeki adacıkların basit laboratuvar çözeltileri yerine gerçek kan bileşenlerine yanıt verip vermediğini test ettiler. Farklı glikoz seviyelerine sahip insan ve sıçan serumu ile maruz bırakıldıklarında, hem frekans hem de elektriksel dalga büyüklüğünde belirgin, derecelenmiş değişiklikler gözlediler. Tepkiler, diyabet için anlamlı aralıkta şeker konsantrasyonundaki küçük adımları ayırt edecek kadar güçlüydü. Ardından sıçan deneylerine geçtiler; kan şekerini yükseltmek için glikoz enjeksiyonu, sonra düşürmek için insülin enjeksiyonu verdiler. Glikozun kandan doku sıvısına ve tüpler aracılığıyla geçiş süresini hesaba kattıktan sonra, adacıkların yavaş elektriksel sinyallerinin frekansının kan şekeri ile neredeyse senkronize olarak yükselip düştüğünü buldular. Birkaç hayvan arasında yapılan istatistiksel analiz, sinyal frekansı ile glikoz seviyesi arasında dikkat çekici derecede sıkı ve tekrarlanabilir bir ilişki gösterirken, sinyal genliği bilgilendirici olmakla birlikte biraz daha değişken bulundu.
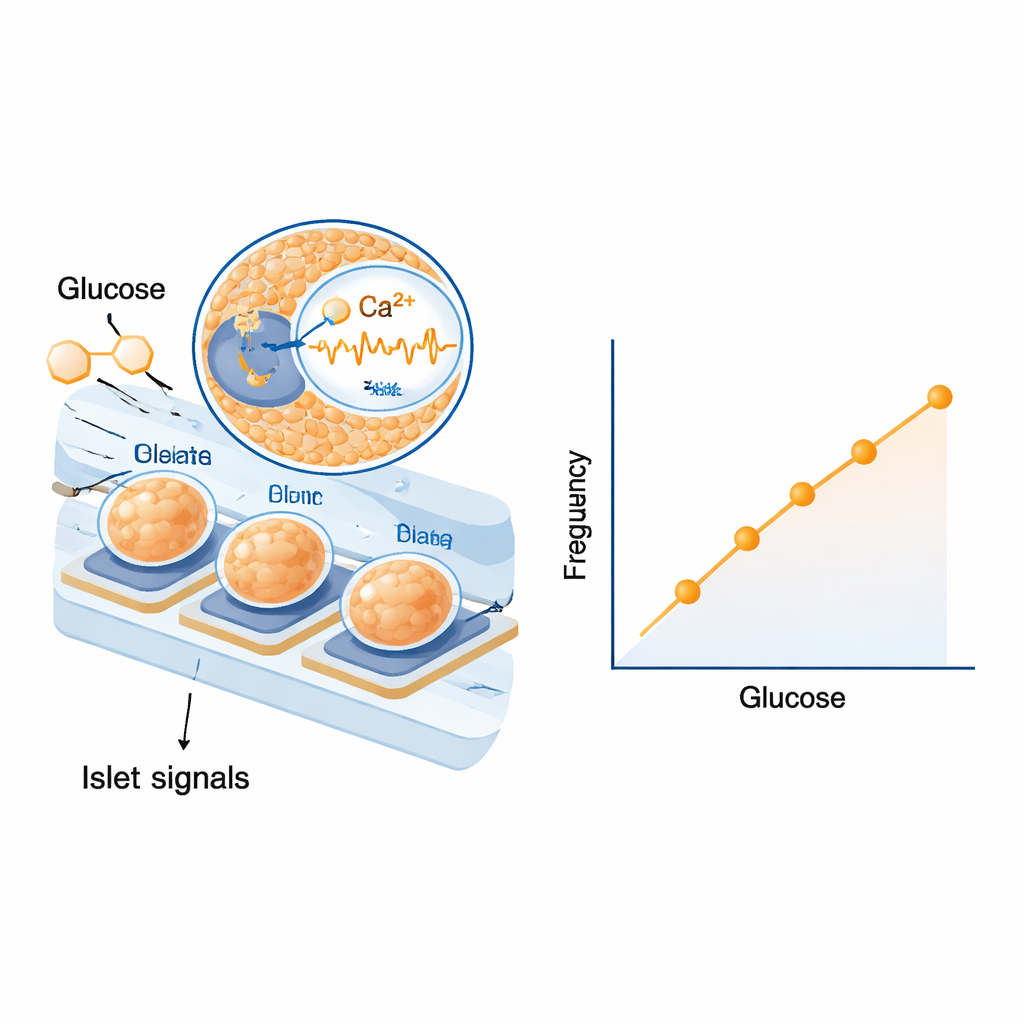
Biyolojiden gelen yerleşik güvenlik özellikleri
Tek bir molekül yerine bütün adacıkları kullanmanın önemli bir avantajı, davranışlarının evrim tarafından şekillendirilmiş güvenlik mekanizmalarını zaten içermesidir. Önceki çalışmalar ve bu çalışmadan gelen ipuçları, adacıkların glikoz düşerken yükselirken olduğundan daha güçlü tepki verdiğini gösteriyor—bu, tehlikeli hipoglisemiden korumaya yardımcı olan bir tür “histerezis”. Elektriksel desenler ayrıca vücudun ihtiyacına göre insülin salınımını artıran veya azaltan komşu hücre tipleri tarafından biçimlendirilir. Çip bu bütünleşik sinyalleri boya veya genetik değişiklik eklemeden dinlediğinden hücrelere zarar vermeden günlerce kayıt yapabilir. Yazarlar hava kabarcıklarından kaçınma, uzun vadeli mikrodiyaliz performansını sağlama ve nihayetinde hangi tip insan veya kök hücre kaynaklı adacıkların kullanılacağı gibi teknik zorluklara dikkat çekiyor. Yine de yerleşik bir diyabet modeli kullanılarak yapılan bilgisayar simülasyonları, böyle adacık tabanlı bir sensörün zorlu koşullarda bile günümüz glikoz izleyicileriyle eşleşebileceğini veya onları aşabileceğini öne sürüyor.
Geleceğin diyabet bakımına olası etkileri
Bu çalışma, küçük bir çip üzerinde canlı tutulan ve ince bir kateterle vücuda bağlı birkaç pankreas mikro-organının, doğal elektriksel “sohbetleri” sayesinde yaşayan hayvanlarda kan şekerini sürekli izleyebileceğini gösteriyor. Uzman olmayan biri için ana mesaj şudur: Basit bir kimyasal sensöre glikoz ölçmesini söyleyip sonra bilgisayarı bu sonucun vücut için ne anlama geldiğini tahmin etmeye zorlamak yerine, bu yaklaşım normalde ne kadar insülin salınacağına karar veren aynı tür canlı dokuya doğrudan kulak veriyor. İnsan kullanımı için geliştirilip pratik hale gelirse, bu tür canlı biyosensörler gerçekten otonom yapay pankreas sistemlerinin çekirdeğini oluşturabilir—vücudun ihtiyaçlarını sessizce önceden tahmin eden ve diyabet yönetiminin günlük yükünü azaltan aygıtlar.
Atıf: Puginier, E., Pirog, A., de Gannes, F.P. et al. A micro-organ based microfluidic biosensor for continuous monitoring of glucose levels in vivo. npj Biosensing 3, 12 (2026). https://doi.org/10.1038/s44328-025-00077-4
Anahtar kelimeler: sürekli glikoz izleme, yapay pankreas, pankreas adacıkları, mikroakışkan biyosensör, tip 1 diyabet