Clear Sky Science · tr
PET, SPECT ve terapötik radyoizotoplar için nanopartikülleri evrensel şelatör olarak kullanan tek aşamalı bir radyolabelleme stratejisi
Neden küçük radyoaktif parçacıklar önemli
Modern kanser bakımında tümörleri taramalarda görünür kılan ve bazı durumlarda içten yakabilen radyoaktif ilaçlarla hem görmek hem de tedavi etmek gittikçe daha fazla kullanılıyor. Ancak her yeni radyoaktif ilacı geliştirmek yavaş ve zahmetli; çünkü çoğu tasarım belirli bir radyoaktif metale göre özel olarak oluşturulmak zorunda. Bu çalışma çok farklı bir yaklaşımı inceliyor: birçok tıbbi izotopu tutabilecek bir “evrensel priz” olarak tek tip demir bazlı nanoparçacık kullanmak — bu, bu tür ilaçların oluşturulma ve ayarlanma hızını potansiyel olarak artırabilir.
Çok anahtarlıktan tek kilide
Günümüz radyoaktif ilaçları genellikle metalleri yakalayıp antikorlar veya diğer hedefleme moleküllerine bağlayan şelatör adı verilen kimyasal pençelere dayanır. Her radyoaktif metal genellikle kendi şelatörünü ve kendi protokolünü gerektirir — sıcaklık, asidite ve reaksiyon süresi gibi koşullar değişir. Özellikle güçlü alfa parçacıklı tedavilerde kullanılan bazı medikal açıdan önemli metaller için hâlâ ideal bir şelatör yoktur. Yazarlar, metal‑metal yaklaşımının bir darboğaz haline geldiğini savunuyor: faydalı izotopların listesi genişliyor, ancak bunları güvenle işleyebilecek kimya buna yetişemiyor.
Evrensel priz olarak nanopartiküller
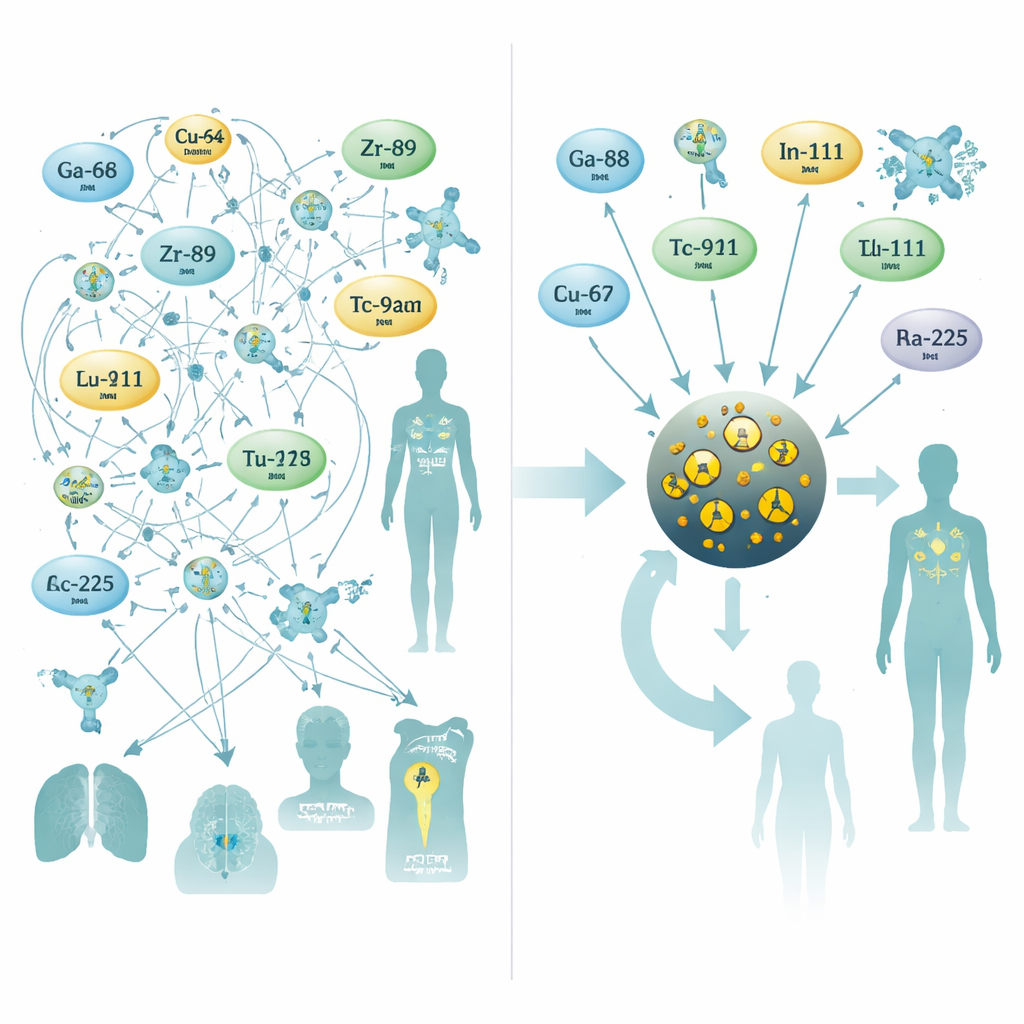
Bunu aşmak için araştırmacılar MRI kontrastı olarak zaten araştırılmış olan çok küçük demir oksit nanoparçacıklarına yöneldi. Yaklaşık üç nanometre genişliğinde bir demir oksit çekirdeği ve kan dolaşımında stabilite sağlayan sitrat molekülleriyle kaplı bir kaplamaya sahip parçacıklar tasarladılar. Tek aşamalı, 10 dakikalık mikrodalga destekli sentez adımında, çekirdeği PET, SPECT veya iç radyoterapi için yaygın olarak kullanılan on farklı radyoaktif metallerden biriyle dopleştiler. Bu tek kap işlemi, tutarlı boyutlarda parçacıklar, yüksek verimler ve en önemlisi insan serumu içinde mükemmel stabilite üretti — radyum‑223 ve aktinyum‑225 gibi bozunma ürünlerinin geleneksel şelatörlerden sıklıkla kaçtığı zorlu tedavi izotopları için bile.
Pıhtı ve beyin tümörlerini görüntülemek
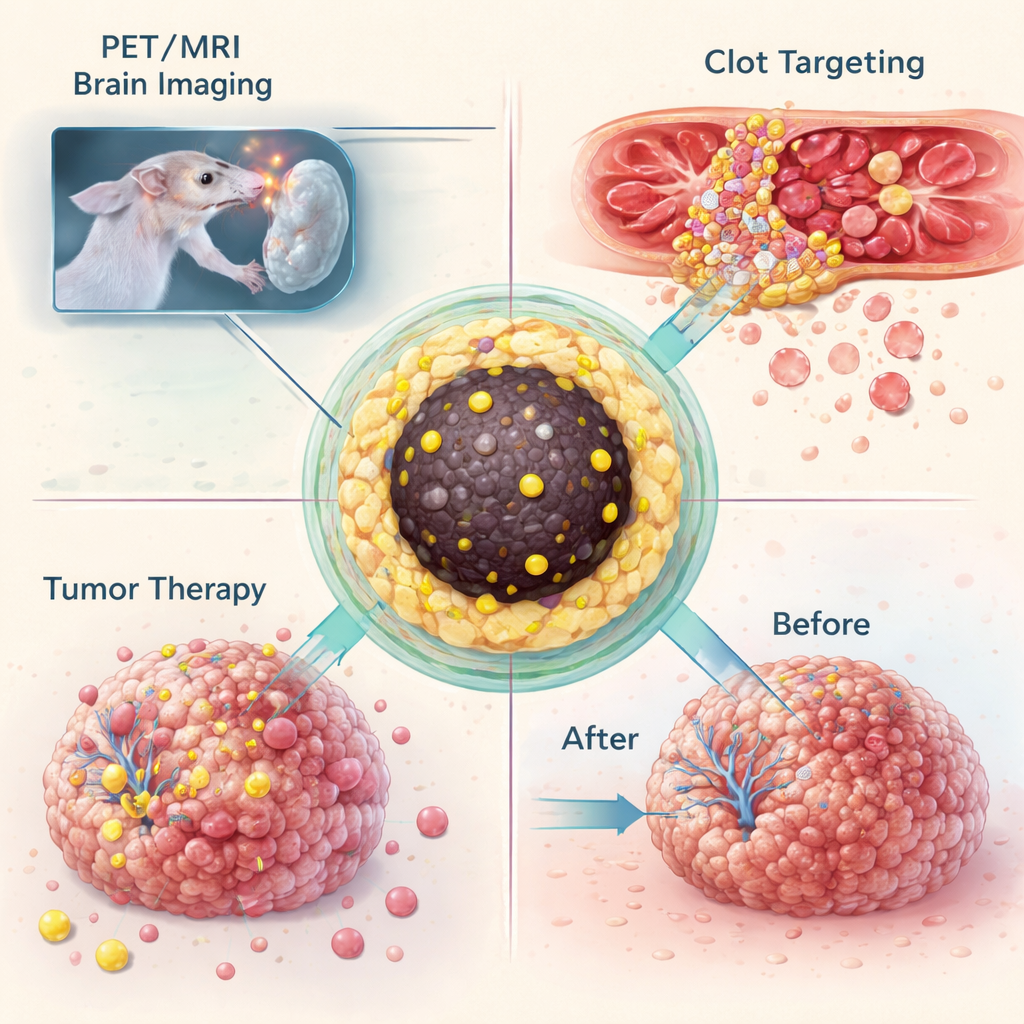
Aynı nanoparçacık tasarımında birçok farklı izotopu yakalayabildiklerini gösterdikten sonra ekip, bu “nanotracer”ların canlı hayvanlarda neler yapabileceğini test etti. Öldürücü bir beyin tümörü olan glioblastomun fare modelinde, gallium‑68 ile etiketlenmiş parçacıklar damar yoluyla enjekte edilip PET ve MRI eş zamanlı görüntülemeyle izlendi. Parçacıklar, kan‑beyin bariyerini bozabilecek kadar büyük tümörlerde birikti; böylece aynı formül hem parlak MRI kontrastı hem de hassas bir PET sinyali sağladı. Ayrı bir deneyde, parçacıklar kimyasal olarak modifiye edilerek yüksek seçiciliğe sahip bir “click” reaksiyonu ile kan pıhtıları içindeki aktive olmuş plateletlere yönelen bir antikorla hızlıca bağlanabilecek hale getirildi. Yaralanmış karotis arterli farelerde bu iki adımlı “önyerleştirme” stratejisi pıhtı bölgesinde net PET sinalleri üretti; kontrol hayvanlarda böyle bir sıcak nokta görülmedi.
Tanıdan tedaviye ve daha güvenli temizlenmeye
Aynı platform tedavi sağlamak için de kullanıldı. Lutezyum‑177 yüklü nanoparçacıklar farelerde doğrudan glioblastom tümörlerine enjekte edildiğinde, parçacıklar en az iki hafta boyunca büyük ölçüde tümör kütlesi içinde kaldı. Bu süre boyunca tedavi edilmeyen tümörler orijinal boyutlarının birkaç katına kadar büyürken, tedavi edilen tümörler büyümeyi durdurdu; bu da lokal radyasyon dozunun ilerlemeyi durdurmaya yeterli olduğunu düşündürdü. Tekrarlanan tedavilerin karaciğer ve dalakta demir birikimine yol açabileceğini fark eden ekip, böbrekler tarafından filtrasyona izin verecek kadar küçük — yaklaşık dört ila beş nanometre çapında — daha da küçük parçacıklar yapmak için sentez koşullarını ayarladı. Bu küçültülmüş parçacıklar radyoaktif yüklerini güvenle tutmaya devam etti ancak hızla mesaneye atılarak büyük organlarda uzun vadeli birikimi azalttı.
Gelecekteki kanser bakımına olası etkileri
Uzman olmayanlar için ana mesaj şudur: araştırmacılar, her seferinde kimyayı yeniden icat etmek zorunda kalmadan birçok farklı radyoaktif metal ile eşleştirilebilen tek, esnek bir nanoparçacık platformu geliştirdiler. Hayvan modellerinde aynı temel parçacık, beyin tümörlerini saptamaya, kan pıhtılarını vurgulamaya, radyasyonu doğrudan tümörlere teslim etmeye ve hatta vücuttan böbrekler yoluyla çıkacak şekilde ayarlanmaya yardımcı olabiliyor. Bu yaklaşım hastalara ulaşmadan önce daha fazla çalışma gerekse de, aynı davranışı paylaşan teşhis ve terapötik ajan aileleri tasarlamak için ümit verici bir yol sunuyor; aralarındaki tek fark taşıdıkları radyasyon türü olur. Bu tutarlılık geliştirmeyi basitleştirebilir, güvenlik testlerini iyileştirebilir ve sonuçta ileri nükleer tıp araçlarını daha geniş erişilebilir hale getirebilir.
Atıf: Herraiz, A., Rodríguez-San-Pedro, A., Casquero-Veiga, M. et al. A single-step radiolabeling strategy for PET, SPECT, and therapeutic radionuclides using nanoparticles as a universal chelator. npj Imaging 4, 8 (2026). https://doi.org/10.1038/s44303-026-00142-1
Anahtar kelimeler: radyoteranostikler, nanopartiküller, PET görüntüleme, glioblastom, hedefe yönelik radyoterapi