Clear Sky Science · tr
SARS-CoV-2 replikasyon dinamikleri ve antiviral ilaç etkinliklerinin adi diferansiyel denklem modelleri
Neden Yeni Bir Virüs İçin Sayılar Önemli
COVID-19 ortaya çıktığında hekimler virüsün hastalarda ne yaptığını görebiliyordu, ancak kimin ağır hasta olacağını ya da bir ilacın en iyi etki için ne zaman verilmesi gerektiğini kolayca öngöremiyorlardı. Bu derleme makalesi, araştırmacıların hasta, hayvan ve hücre kültürü verilerini beden içindeki enfeksiyonun matematiksel “filmlerine” nasıl dönüştürdüğünü inceliyor. Bu modeller, virüsün nasıl çoğaldığını, hücrelerimiz ve bağışıklık sistemimizin nasıl tepki verdiğini ve antiviral ilaçlar ile aşıların durumu lehimize nasıl çevirebileceğini izlemek için denklemler kullanır.
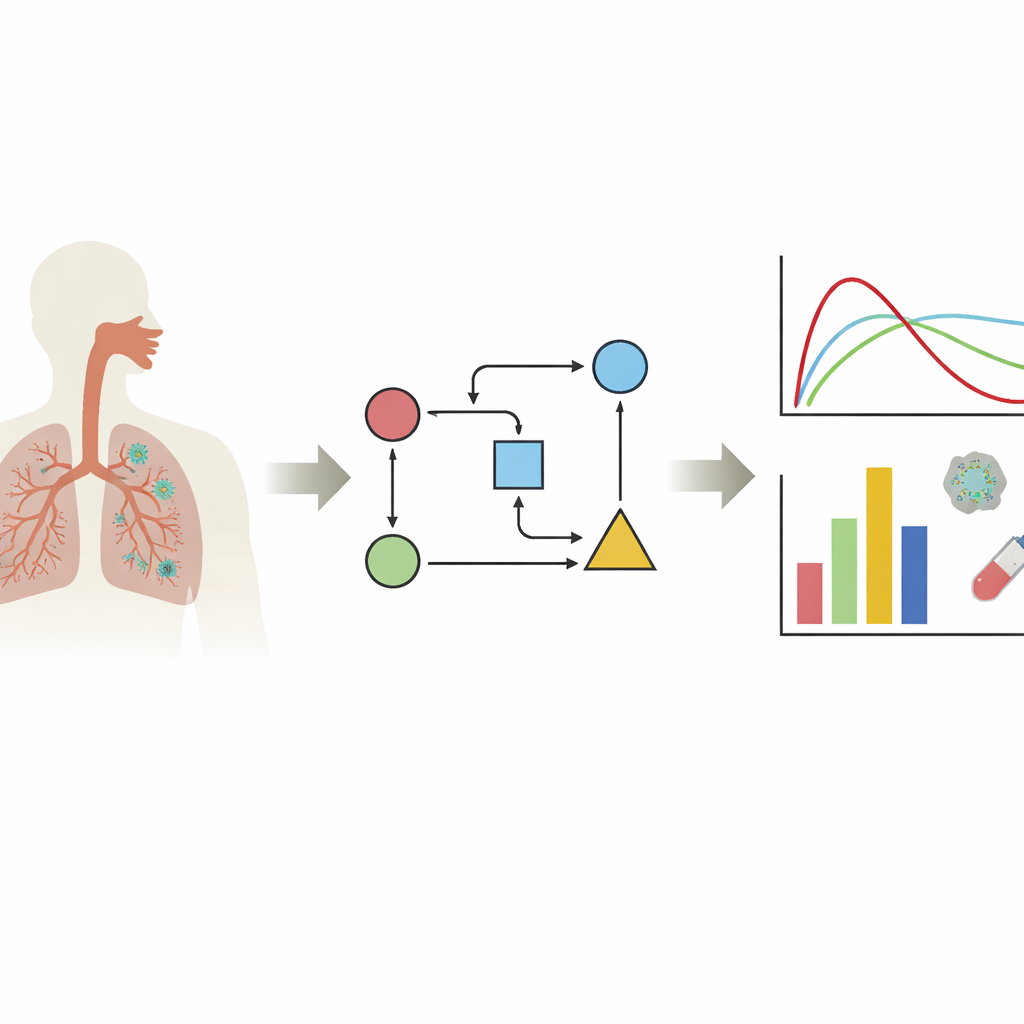
Vücudun İçindeki Virüsü İzlemek
Yazarlar hedef hücre sınırlı modeller adı verilen bir model ailesine odaklanıyor. Basitçe söylemek gerekirse, bu modeller üç ana aktörü takip eder: enfekte edilebilecek sağlıklı hücreler, zaten enfekte olmuş hücreler ve serbest virüs partikülleri. Gerçek viral düzey verilerini bu denklemlere vererek, araştırmacılar enfeksiyonun gizli özelliklerini tahmin edebilir: virüsün hücreleri ne kadar hızlı enfekte ettiği, enfekte bir hücrenin ne kadar süre virüs ürettiği ve virüsün ne kadar hızlı temizlendiği gibi. Derleme, çalışmaların çoğunun COVID-19 için en önemli dokular olan burun ve üst ile alt solunum yollarına yoğunlaştığını; sadece birkaç modelin diğer organları incelediğini gösteriyor. Önemli bir mesaj, hangi doku, hangi virüs varyantı ve hangi laboratuvar hücre hattının incelendiğine bağlı olarak virüs davranışının çok farklı görünebileceği, dolayısıyla tek bir “tipik” enfeksiyon eğrisi olmadığıdır.
Bağışıklık Sistemi Hakkında Neler Öğreniyoruz
Birçok model, bağışıklık sisteminin erken savunmalarını ve daha yavaş, daha hedefe yönelik yanıtlarını temsil eden katmanlar ekler. İlk savunma hattına odaklanan çalışmalar, doğal bağışıklık hücreleri ve sinyal moleküllerinin hızlı ve zamanında etkinliğinin enfeksiyonu zayıflatabileceğini, ancak nadiren tek başına ortadan kaldırdığını öne sürüyor. Diğer çalışmalar ise T hücreleri ve antikorların virüsü nihayet kontrol altına almada oynadığı hayati role vurgu yapıyor. Modeller ayrıca daha karanlık bir tarafı yakalıyor: hedefe yönelik bağışıklık yanıtı gecikirse veya yanlış yönlendirilirse, bizi koruması gereken aynı araçlar aşırı iltihap sinyalleriyle sağlıklı dokulara zarar veren “sitokin fırtınalarını” körükleyebilir. Bu simülasyonlarda yardımcı ve zararlı bağışıklık etkinliği arasındaki hassas denge genellikle hastalığın hafif kalıp kalmayacağını veya hayati tehlike oluşturup oluşturmayacağını belirliyor.
İlaçlar ve Aşılar En İyi Ne Zaman Etkili Olur
Denklemler farklı varsayımlar altında tekrar tekrar çalıştırılabildiği için, bunlar insanlarda denemeden önce tedavi stratejilerini bilgisayar ortamında test etmek için güçlü araçlardır. Birçok çalışma boyunca modeller bir ana noktada hemfikir: antiviral ilaçlar, virus zirveye ulaşmadan ve mevcut hücrelerin çoğunu enfekte etmeden çok önce verildiğinde en iyi şekilde çalışır. Virüsün genetik materyalini kopyalamasını engelleyen tedaviler özellikle umut verici çıkıyor; özellikle farklı mekanizmalarla etki eden diğer ilaçlarla kombinasyon halinde olduğunda. Buna karşılık geç tedavi, simülasyonlarda birkaç güçlü ilaç birlikte kullanılmadıkça genellikle çok az etki gösterme eğilimindedir. Aşılama, esas olarak bağışıklık sistemini virüsü hızla tanıyacak şekilde hazırlayarak yüksek viral düzeylerin kısa süreli olmasını sağladığı için tek başına ilaçlardan daha iyi performans gösterdiği sürekli öngörülür.
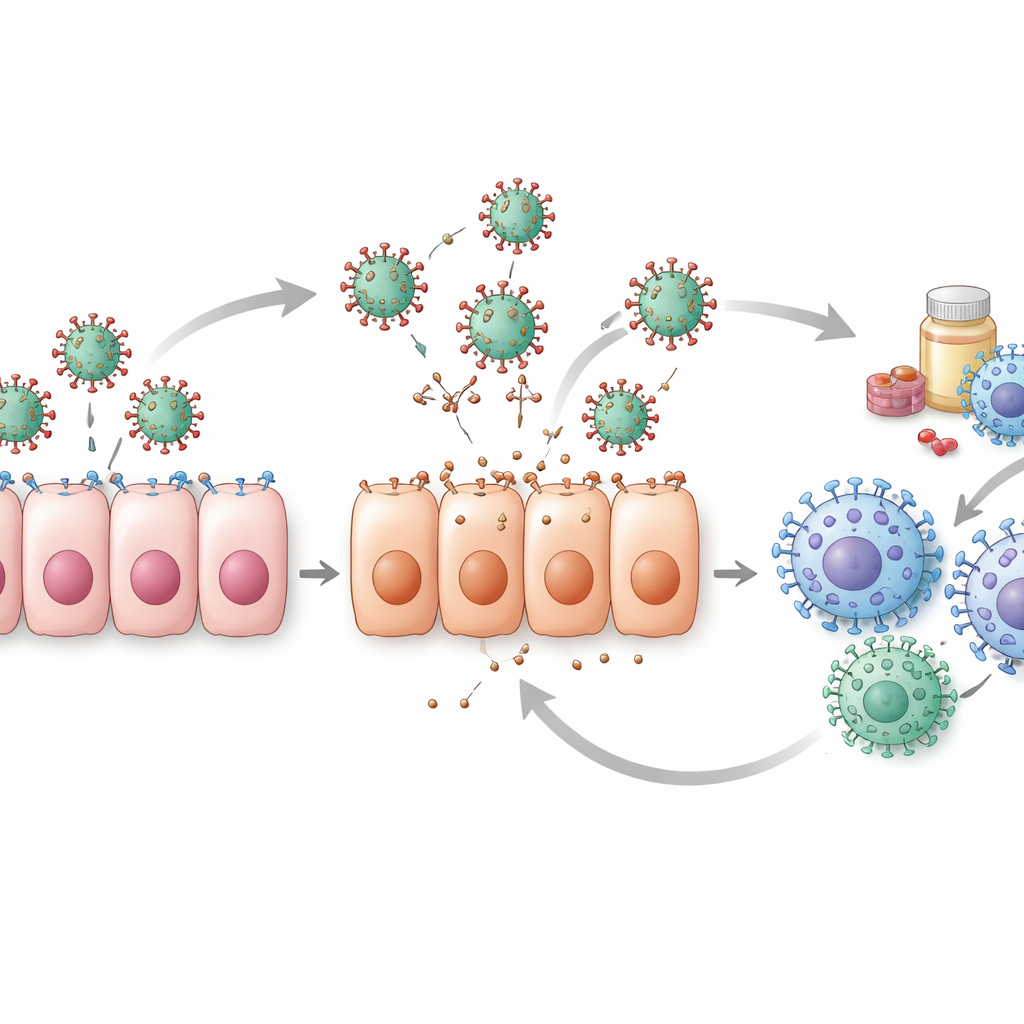
Verilerdeki Gizli Zorluklar
Derleme ayrıca sayıların arkasındaki zayıflıklara ışık tutuyor. Çoğu klinik veri seti, insanların zaten hasta hissetmeye başladıktan sonra ölçümlere başlar; bu da modellerin genellikle virüs düzeylerinin en hızlı yükseldiği enfeksiyonun kritik ilk günlerini kaçırdığı anlamına gelir. Bu erken ölçümler olmadan, model parametrelerinin farklı kombinasyonları aynı veriyi açıklayabilir ve hangi açıklamanın doğru olduğundan emin olmayı zorlaştırır. Çalışmaların yalnızca azınlığı parametre tahminlerinin gerçekten eşsiz ve güvenilir olup olmadığını görmek için sağlam kontroller yapar. Hayvan çalışmaları ve hücre kültürü deneyleri bazı boşlukları, özellikle erken zaman noktaları için doldurmaya yardımcı olur, ancak türler ve laboratuvar sistemleri arasındaki farklılıklar bu sonuçların insanlara ne kadar doğrudan uygulanabileceğini sınırlar.
Gelecek İçin Ne Anlama Geliyor
Uzman olmayan bir kişi için sonuç şudur: dikkatle inşa edilmiş matematiksel modeller, SARS-CoV-2'nin vücut içindeki davranışı ile zamanlama, ilaç kombinasyonları ve önceki aşılama gibi faktörlerin sonuçları nasıl şekillendirdiği konusunda anlayışımızı büyük ölçüde geliştirdi. Modeller genel olarak erken, güçlü müdahalenin—özellikle aşılama ve zamanında antiviraller yoluyla—bağışıklık sistemine kazanma şansını en iyi şekilde verdiği, gecikmiş yanıtların ise hem vücuttan hem de tedaviden kaynaklansa daha şiddetli hastalıkla ilişkilendirildiği konusunda hemfikirdir. Aynı zamanda yazarlar, bu araçların ancak içine konulan veriler kadar iyi olduğunu vurguluyor. Gelecekteki varyantlara veya yeni virüslere hazırlanmak için daha zengin, daha erken klinik örnekleme ve daha geniş bağışıklık ölçümleri çağrısında bulunuyorlar, böylece “enfeksiyonun ardındaki sayılar” gerçek salgınlarda daha hızlı, daha doğru kararları yönlendirebilir.
Atıf: Kapischke, T., Herrmann, S.T., Bertzbach, L.D. et al. Ordinary differential equation models of SARS-CoV-2 replication dynamics and antiviral drug efficacies. npj Viruses 4, 17 (2026). https://doi.org/10.1038/s44298-026-00183-8
Anahtar kelimeler: SARS-CoV-2 viral dinamikleri, konak içi modelleme, antiviral tedavi zamanlaması, bağışıklık yanıtı, COVID-19 aşılaması