Clear Sky Science · tr
Soluble RSV G proteini, TLR2 aracılı NLRP3 hazırlığı ve piroptoz yoluyla viral yayılmayı artırır
Bu akciğer virüsünün herkes için önemi
Respiratuar sinsityal virüs (RSV), bebekler için kışın sık görülen bir tehdit olarak bilinse de, yaşlılar ve bağışıklığı zayıf kişilerde de hastaneye yatışlara yol açar. Yeni aşılar ve koruyucu antikorlar olmasına rağmen RSV insanları tekrar tekrar yeniden enfekte eder ve ağır akciğer hasarına neden olabilir. Bu çalışma, RSV G proteininin az bilinen bir şekli olan çözünebilir G proteini üzerine odaklanıyor ve bu proteinin akciğer hücrelerini patlayıcı bir iltihaba hazırlayarak virüsün hava yollarında daha verimli yayılmasını nasıl kolaylaştırabileceğini ortaya koyuyor.
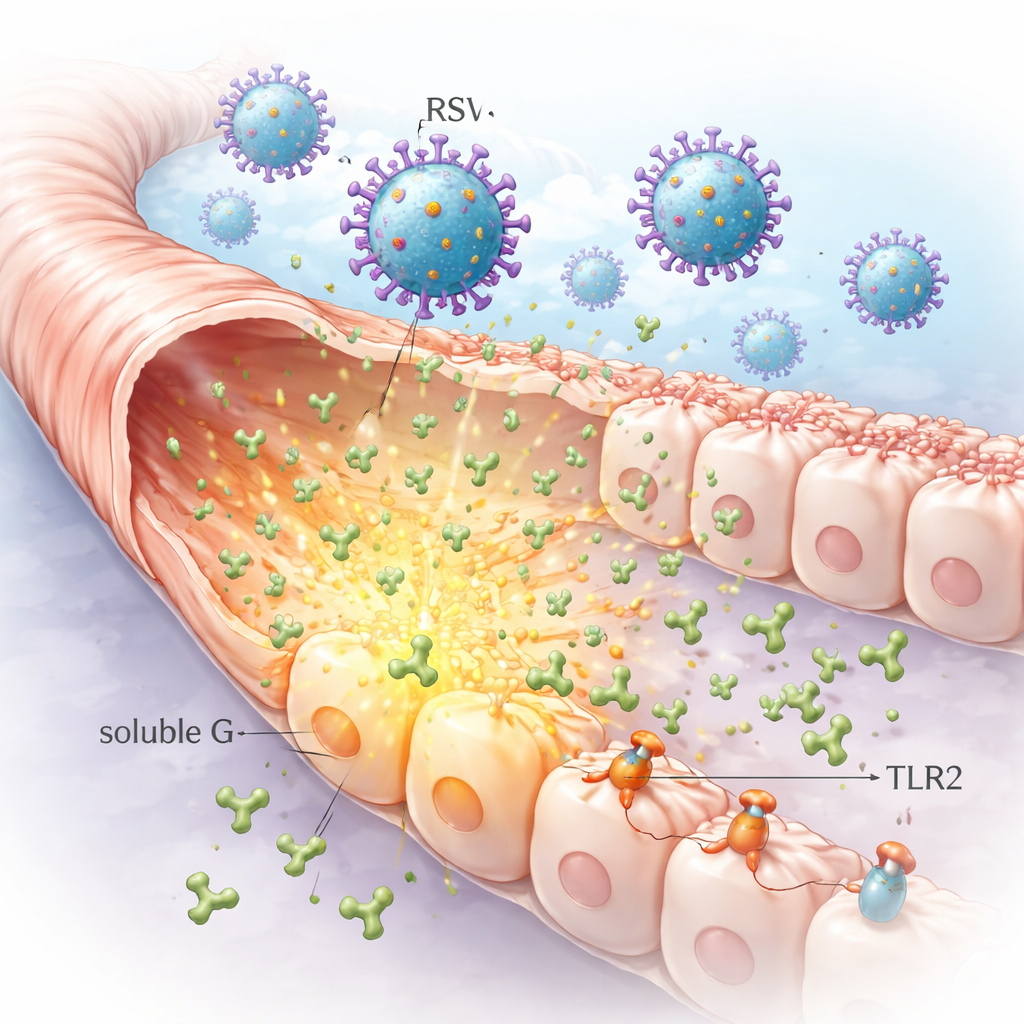
Enfeksiyonun önünde yol alan salgılanan bir viral protein
RSV yüzeyinde, hava yolu hücrelerine tutunmasına yardımcı olan G adlı bir yapışma proteini taşır. Alışılmadık şekilde, enfekte hücreler ayrıca bu proteinin serbest dolaşan bir formunu, yani çözünebilir G’yi büyük miktarlarda salgılar. Araştırmacılar laboratuvarda enfekte edilen akciğer hücrelerinin çevrelerine çok yüksek seviyelerde çözünebilir G bırakabildiğini gösterdi. Bu form orijinal enfeksiyon bölgesinden uzaklara difüze olabildiğinden henüz enfekte olmayan komşu hücrelere ulaşabilir ve virüsün tek başına yol açacağından daha geniş akciğer yüzeyi değişiklikleri için zemin hazırlayabilir.
Çözünebilir G: hücre yüzeylerine iki işlevli bir anahtar
Mikroskopi, biyokimyasal çekme testleri ve enzim işlemleri bir arada kullanılarak ekip, çözünebilir G’nin hücrelere nasıl tutunduğunu haritaladı. Bunun glikozaminoglikan adı verilen şeker zincirlerine ve bilinen bir RSV reseptörü olan CX3CR1’e bağlanabildiğini buldular. Kritik olarak, çözünebilir G aynı zamanda bağışıklık ve hava yolu hücrelerindeki bir desen algılayıcısı olan TLR2’ye de bağlanıyordu. G proteinindeki küçük bir motif olan CX3C, CX3CR1’e güçlü bağlanma ve TLR2’nin güçlü şekilde çekilmesi için önemli bulundu. Bu, çözünebilir G’nin önce hücre yüzeyinde gevşekçe tutulabileceği, ardından hücrelerin tehditlere verdiği yanıtları kontrol eden daha özel reseptörlerle etkileşime girebileceği anlamına gelir.
Akciğer hücrelerini iltihaplı bir hücre ölümü türüne hazırlamak
Çözünebilir G’nin TLR2 ile etkileşiminin zararsız olmadığı ortaya çıktı. Raporer bağışıklık hücrelerinde ve insan akciğer hücre hatlarında çözünebilir G, TLR2’nin aşağısındaki MyD88–NF-κB sinyal yolunu etkinleştirerek IL-6 ve IL-8 gibi iltihap yapıcı habercilerin salınmasına yol açtı. Aynı zamanda NLRP3 inflamazom adlı moleküler “alarm sistemi” bileşenlerinin ve nitrik oksit ve oksijen radikalleri gibi reaktif moleküller üreten enzimlerin üretimini artırdı. Bunlar tek başına sadece hafif hasara neden oldu. Ancak hazırlanan hücreler daha sonra RSV ile enfekte edildiğinde ikinci darbe tam inflamazom montajını, kaspaz-1 enziminin aktivasyonunu, hücre zarında gözenek oluşumunu ve piroptoz olarak bilinen ateşli bir hücre ölümü biçimini tetikledi. Bu süreç hücrelerde delikler açtı, iltihaplı içeriklerin dökülmesine yol açtı ve kültür sıvısına daha yüksek miktarda enfektif virüs salınmasıyla eş zamanlı oldu.
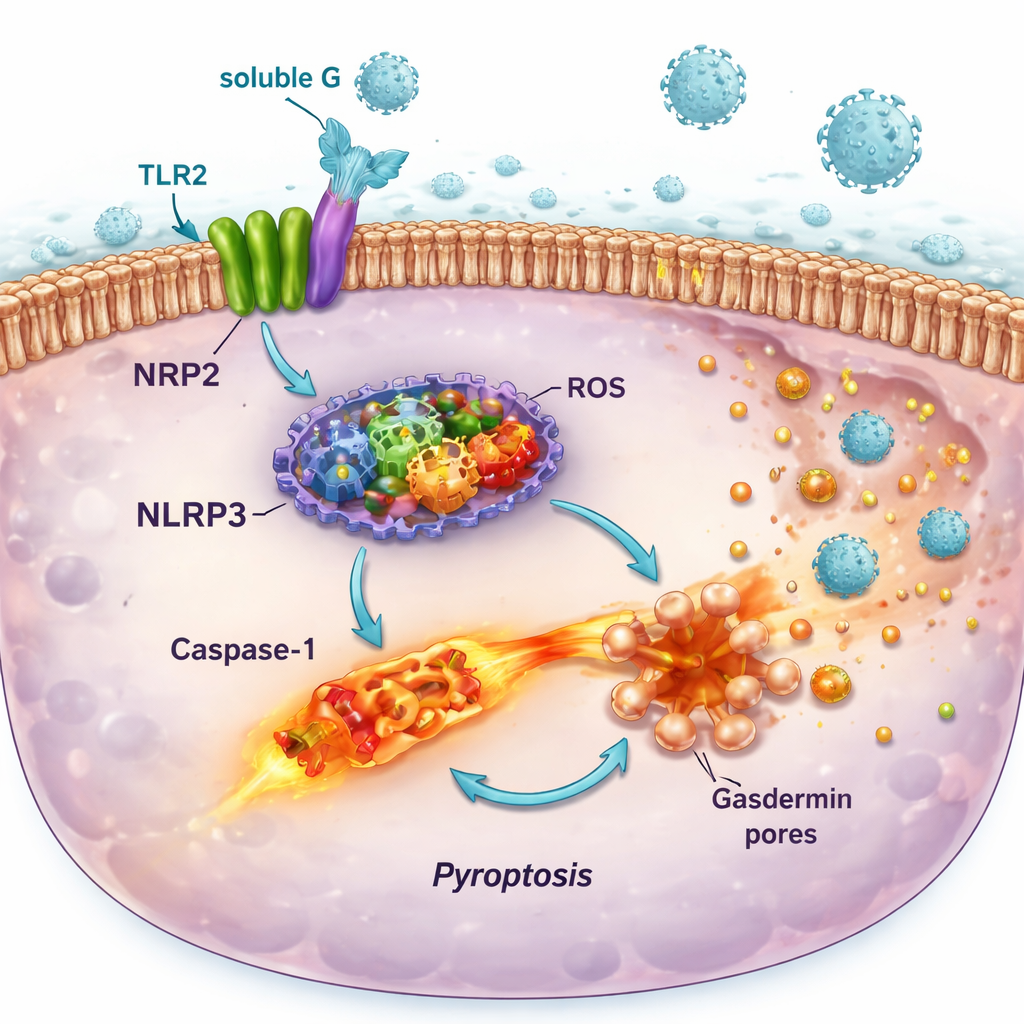
Bu zincirleme reaksiyonun akciğer hastalığını nasıl kötüleştirebileceği
Çözünebilir G’nin hücre ölümünü artıran etkisi RSV’nin tercih ettiği hücreler olan hava yolu epitel hücrelerinde en güçlüydü ve bu etkinin NLRP3 inflamazomuna bağlı olduğu görüldü; zira spesifik bir NLRP3 inhibitörü hücre yaşamsallığını büyük ölçüde korudu. Buna karşılık, TLR2 açısından zengin ancak CX3CR1 reseptörü açısından fakir bazı bağışıklık hücreleri aynı koşullar altında güçlü liztik ölüme uğramadı. Bu desen, RSV’nin çözünebilir G’yi hava yollarının koruyucu örtüsünü seçici olarak zayıflatmak ve yok etmek, aynı zamanda bazı bağışıklık hücrelerini sinyal üretmeye devam edebilecek şekilde korumak için kullandığını düşündürür. Sonuç, daha fazla iltihap, daha fazla hücre kalıntısı ve yeni virüs partiküllerinin kaçıp komşu hücreleri enfekte etmesi için daha fazla fırsat sağlayan bir akciğer ortamıdır.
Gelecekteki tedaviler için anlamı
Uzman olmayanlar için ana mesaj şudur: RSV sadece viral istilanın doğrudan verdiği hasara dayanmaz. Büyük miktarlarda çözünebilir G proteini salgılayarak, TLR2 aracılığıyla yakın hücreleri “yumuşatabilir”, böylece bunların iltihaplı bir şekilde ölme olasılığını ve virüs dökme eğilimini artırır. Bu çalışma zincirdeki birkaç adımı — çözünebilir G’nin kendisi, CX3C motifi, TLR2 ve NLRP3 inflamazomu — potansiyel ilaç hedefleri olarak belirliyor. Prensipte, çözünebilir G ile TLR2 arasındaki etkileşimi engelleyen veya NLRP3 aktivitesini azaltan tedaviler hem akciğer hasarını hem de viral yayılmayı azaltabilir. Bu tür yaklaşımlar, bir gün mevcut RSV aşıları ve antikorlarını tamamlayarak en genç ve en savunmasız hastalar için daha iyi koruma sağlayabilir.
Atıf: Meineke, R., Agac, A., Knittler, MC. et al. The soluble G protein of respiratory syncytial virus promotes viral dissemination via TLR2-mediated NLRP3 priming and pyroptosis. npj Viruses 4, 6 (2026). https://doi.org/10.1038/s44298-026-00172-x
Anahtar kelimeler: respiratuar sinsityal virüs, çözünebilir G proteini, TLR2 inflamazom, piroptoz, akciğer iltihabı