Clear Sky Science · tr
STAR (stroma-tumor AI risk) değerlendirmesi: Yapay zekâ kaynaklı tümör-stroma oranının hasta sağkalımıyla ilişkisi, epitelial over kanserinde KELIM’in ötesinde prognostik değer sağlar
Neden tümörün çevresindeki “mahalle” önemli?
Kanser hakkında düşünürken genellikle kötü huylu hücrelerin bir yığını aklımıza gelir. Oysa tümörler destek dokusu, kan damarları ve bağışıklık hücrelerinden oluşan yoğun bir mahallede yaşar; buna stroma denir. Bu çalışma basit ama güçlü bir soruyu gündeme getiriyor: rutin mikroskop camlarında yapay zekâ ile ölçülen tümör hücreleri ile çevre dokunun dengesi, tedavi başlamadan önce hangi over kanseri hastalarının daha iyi veya daha kötü sonuçlar alacağını öngörebilir mi?
Standart biyopsi lamlarını okumaya yeni bir yaklaşım
Epitelial over kanseri olan kadınlarda genellikle cerrahi veya biyopsi sırasında doku alınır. Bu örnekler boyanır ve her hastanede mikroskopla incelenir. Araştırmacılar, görüntüde destek dokusunun kanser hücrelerine kıyasla ne kadar yer kapladığını gösteren tümör–stroma oranı (TSP) adı verilen bir özelliğe odaklandı. Daha önce patologlar bu oranı gözle tahmin etmiş ve stroma açısından zengin tümörlerin sıklıkla daha agresif davrandığını ve standart platin bazlı kemoterapiye dirençli olduğunu bulmuşlardı. Mevcut çalışmada ekip, dijitalleştirilmiş lamlar üzerinde TSP’yi otomatik olarak ölçmek için derin öğrenme tabanlı bir yapay zekâ sistemi kullandı; amaç, el ile ve bir ölçüde öznel olan bu işi tanı anında hızlı ve tekrarlanabilir bir çıktıya dönüştürmekti.
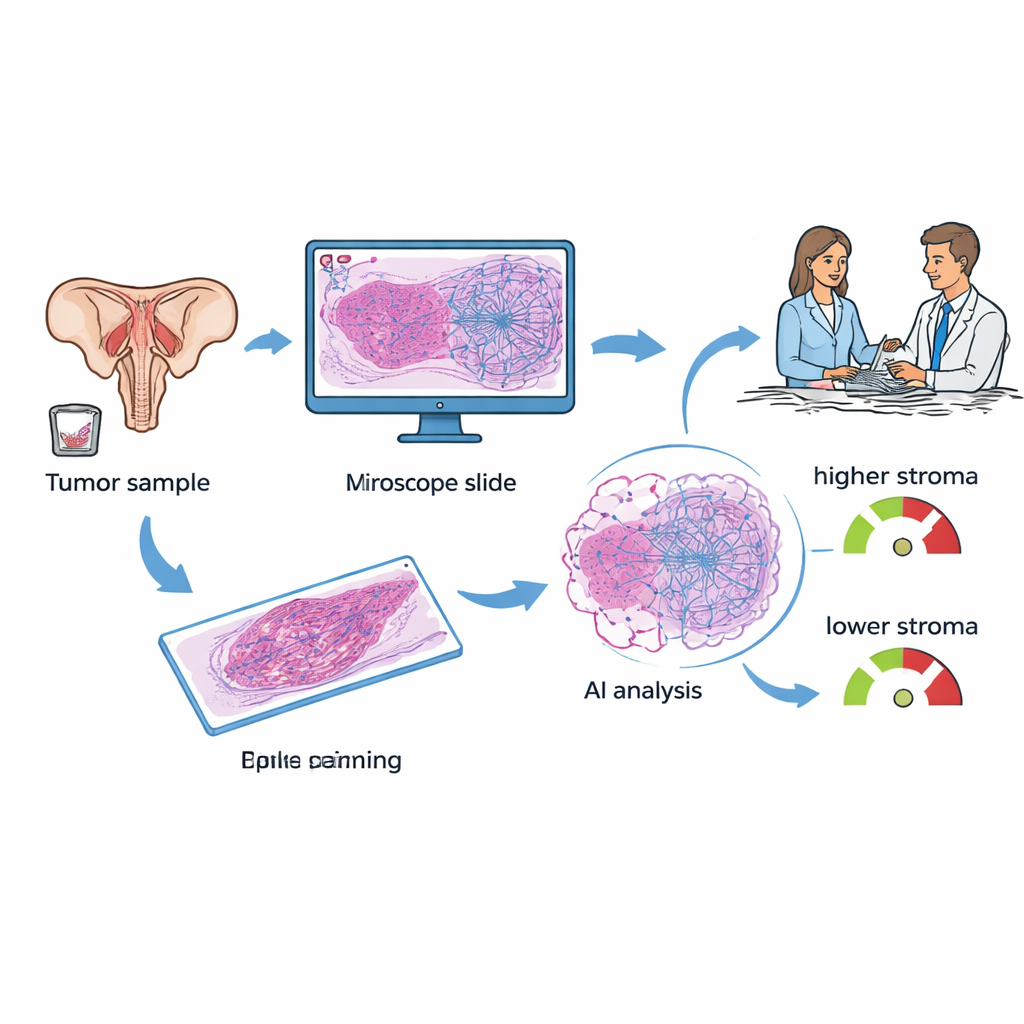
Yapay zekâ doku analizini kan temelli bir skorla karşılaştırmak
Bugün over kanserinde sıkça tartışılan araçlardan biri, kemoterapinin ilk 100 gününde CA-125 adlı kan belirteçinin ne kadar çabuk düştüğüne dayanan KELIM skorudur. KELIM ucuz ve yardımcı bir ölçüttür, ancak birkaç hafta süren tedaviden sonra hesaplanabilir ve tüm hastalarda skoru üretmek için yeterli erken kan testi olmayabilir. Araştırmacılar, hem doku lamlarına hem de en az üç CA‑125 ölçümüne sahip tek bir kanser merkezinde tedavi görmüş 89 kadından verileri topladı. Her hasta için KELIM hesaplandı, bir patolog lamlarda tümör bölgelerini işaretledi ve ardından yapay zekâ modeli TSP’yi tahmin ederek her vakayı “stroma-düşük” (%50’den az stroma) veya “stroma-yüksek” (%50 veya daha fazla) olarak sınıflandırdı.
Yapay zekâ uzmanlarla eşleşiyor ve daha yüksek riskli tümörleri işaretliyor
Yapay zekânın değerlendirmesi deneyimli patologlarla yakından örtüştü: otomatik TSP sınıflandırması vakaların %94’ünde manuel sınıflandırmayla aynıydı; bu, mükemmele yakın bir uyum düzeyi olarak değerlendirildi. Ekip hasta sonuçlarına baktığında, yapay zekâya göre stroma-yüksek olan tümörlere sahip kadınların, stroma-düşük olanlara göre anlamlı şekilde daha kötü genel sağkalıma sahip olduğunu buldu. İstatistiksel olarak yüksek TSP, takip süresi boyunca ölme riskini neredeyse iki katına çıkarıyordu ve bu etki KELIM skoru hesaba katıldıktan sonra bile devam etti. Buna karşılık, bu gerçek dünya hasta grubunda KELIM platin ilaçlara dirençle ilişkili bulunurken, hastaların yaşam süreleriyle açıkça bağlantılı değildi.
Bu, tedavi kararları için ne anlama gelebilir?
TSP tanı anında alınan rutin lamlardan ölçülebildiği için, yapay zekâ tabanlı TSP kemoterapi başlamadan önce, KELIM’e göre potansiyel olarak aylarca daha erken bir risk değerlendirme yolu sunar. Yüksek bir TSP sonucu, bir tümörün daha agresif ve tedaviye daha dirençli olma olasılığını klinisyenlere işaret edebilir; bu da daha sık izleme, ek tedavilere daha erken başvurma veya farklı cerrahi stratejilerin değerlendirilmesini tetikleyebilir. Yöntem aynı zamanda görece düşük maliyetlidir: yeni laboratuvar testleri gerektirmek yerine mevcut patoloji görüntülerine ve yazılım modeline dayanır. Yazarlar, otomatik TSP’nin genetik testler ve CA‑125 eğilimleri gibi diğer belirteçlerle birlikte çalışarak hastalar veya patoloji ekipleri üzerinde ek yük oluşturmadan prognozu iyileştirebileceğini savunuyorlar.
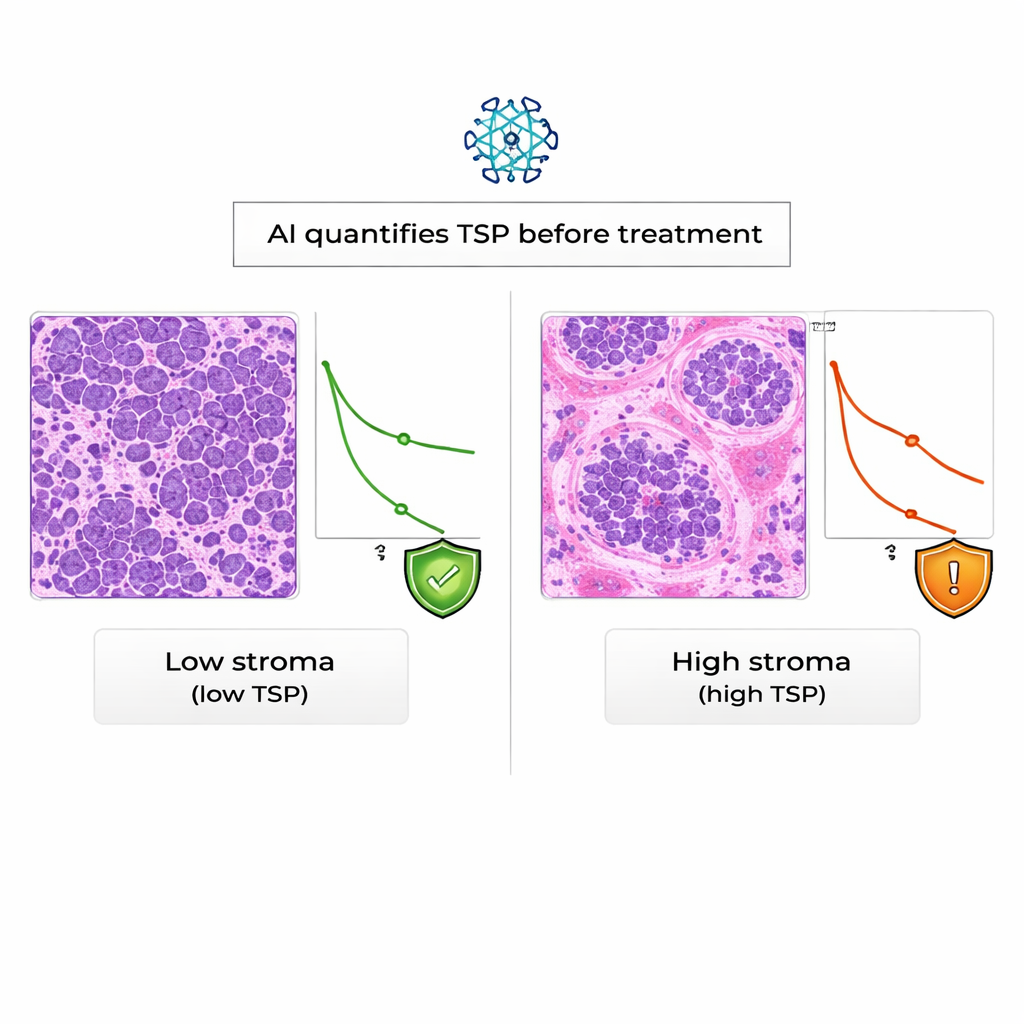
İleriye bakış: hastalar için daha akıllı, daha erken rehberlik
Bir okuyucu için temel mesaj, tüm over kanserlerinin aynı olmadığı ve tümörü çevreleyen destek dokunun hastalığın nasıl davranacağı hakkında önemli ipuçları taşıdığıdır. Bu çalışma, yapay zekânın bu ipuçlarını standart biyopsi lamlarında güvenilir biçimde okuyabildiğini ve stroma-ağırlıklı bir tümörün, var olan kan temelli skorların ötesinde kötü sağkalımla ilişkilendiğini gösteriyor. Bu yaklaşımın rutin bakıma girmeden önce daha geniş ve daha çeşitli çalışmalara ihtiyaç duyulsa da, yapay zekâdan türetilen TSP, doktorların tedavi planlarını kişiselleştirmesine ve hastalara en başından itibaren daha net beklentiler sunmasına yardımcı olabilecek erken bir uyarı işareti olma potansiyeli taşıyor.
Atıf: Aggarwal, A., Madill, M., Jana, M. et al. STAR (stroma-tumor AI risk) assessment: association of AI-derived tumor-stroma proportion with patient survival provides added prognostic value beyond KELIM in epithelial ovarian cancer. BJC Rep 4, 4 (2026). https://doi.org/10.1038/s44276-026-00205-1
Anahtar kelimeler: over kanseri, yapay zekâ, tümör mikroçevresi, prognostik biyobelirteç, dijital patoloji