Clear Sky Science · tr
Antibiyotik maruziyetine küresel yanıt, yüksek düzey β-laktam toleransında nükleotid metabolizminin kritik rolünü ortaya koyuyor
Bazı bakteriler en güçlü antibiyotiklerimize neden direniyor?
Antibiyotikler zararlı bakterileri yok etmek için tasarlanmıştır, ancak birçok enfeksiyon tedaviye rağmen inatla devam eder veya tedaviden sonra yeniden ortaya çıkar. Bu makale bunun az takdir edilen bir nedenini inceliyor: bazı bakteriler, penisilin gibi çok güçlü ilaçların çok yüksek dozlarına bile geçici olarak dayanabilir. Bu mikropların saldırı sırasında iç kimyalarını nasıl yeniden düzenleyerek hayatta kaldığını ortaya koyarak, araştırmacılar mevcut antibiyotiklerin etkinliğini geri kazanmamıza yardımcı olabilecek yeni yaklaşımlara işaret ediyor.
Enfeksiyonların içindeki sinsi bir hayatta kalma taktiği
Penisilin gibi beta-laktam antibiyotiklere maruz kaldıklarında, birçok tehlikeli Gram-negatif bakteri basitçe ölmez. Bunun yerine sert hücre duvarlarını dökebilir ve sferoplasti adı verilen kırılgan, yuvarlak yapılara dönüşebilirler. Bu biçimde çoğalmayı durdururlar ama hâlâ canlı ve metabolik olarak aktiftirler. İlaç ortadan kalktığında duvarlarını yeniden inşa eder, normal çubuk şekillerine döner ve enfeksiyonu yeniden başlatabilirler. Bu “tolerans” tam direnç ve tedavi başarısızlığına giden bir ara basamak olduğu için, sferoplastların nasıl hayatta kaldığını anlamak geleceğin tıbbı açısından kritiktir.
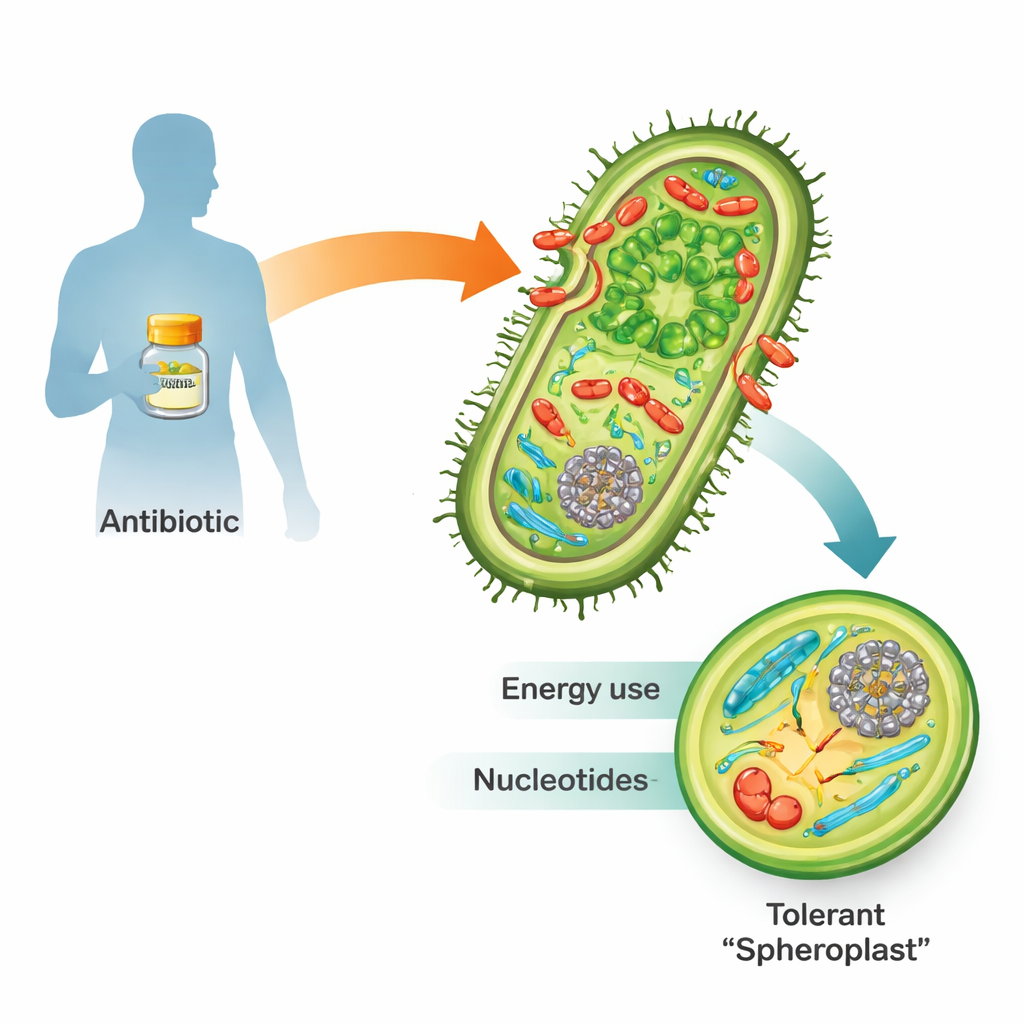
Hücrenin acil yayınını dinlemek
Araştırmacılar model olarak koleraya neden olan Vibrio cholerae bakterisini kullandılar; çünkü bu bakteri beta-laktamlara karşı olağanüstü derecede toleranslıdır ve genetik olarak kolayca değiştirilebilir. Bakterileri minimum öldürücü dozanın on katı kadar penisilinle muamele edip iki güçlü araçla zaman içinde yanıtı izlediler. Transkriptomik hangi genlerin açılıp kapandığını izlerken, metabolomik hücreyi besleyen ve inşa eden yüzlerce küçük molekülü ölçtü. Bu “çoklu omik” teknikler birlikte toleranslı bir hücrenin ilaç saldırısı sırasında iç işleyişini zaman çözünürlüğüyle yeniden düzenleme haritasını oluşturdu.
Metabolik yön değiştirme ve gizli bir zayıf nokta
Veriler çekirdek yolaklarda kapsamlı değişiklikleri ortaya koydu. Hücre duvarı inşası için gerekli genler güçlü şekilde açıldı; bu, hücrenin hasarı onarmaya ve iyileşmeye hazırlanma girişimiyle tutarlı. Isı şoku ve stres yanıtı sistemleri de alevlendi; muhtemelen antibiyotik kaynaklı stresten dolayı yanlış katlanmış, okside olmuş proteinlerle başa çıkıyorlar. Aynı zamanda merkezi karbon metabolizması kaydı: hücrenin ana enerji üreticisi olan TCA döngüsünün belirli adımları desteklenirken, glukoz-6-fosfat ve fruktoz-6-fosfat gibi anahtar glikoliz ara ürünleri dramatik şekilde azaldı. Bu ara ürünler normalde hem enerji üretimini hem de hücre duvarı inşasını beslediğinden, sürekli ve boşa giden bir “faydasız döngü”nün duvar materyalini tüketerek kaynakları boşalttığını düşündürüyor.
Nükleotidler baskı altında
En çarpıcı değişiklik nükleotidlerde, yani DNA, RNA ve birçok enerji taşıyan molekülün yapı taşlarında gözlendi. Penisilinle muamele edilen hücrelerde birçok nükleotid ve bunların öncüllerinin seviyeleri hızla düştü; oysa bunları sıfırdan üreten genler güçlü şekilde aktive olmuştu. Aynı zamanda nükleotidleri “geri dönüştürmeye” yarayan genler kapatıldı, sanki hücre kalan az miktarı korumaya çalışıyormuş gibiydi. Bu desenler sferoplastların şiddetli nükleotid stresi altında olduğunu gösteriyordu. Araştırmacılar pentoz fosfat yol gibi nükleotid öncüllerini sağlayan yolları kasıtlı olarak bozduklarında veya trimetoprim gibi başka bir ilaçla nükleotid üretimini engellediklerinde, beta-laktamlarla kombinasyon halinde tek başına olan ilaçlardan çok daha fazla bakteriyi öldürdü. Bu güçlü sinerji yalnızca Vibrio cholerae’de değil, aynı zamanda yüksek toleransa sahip Klebsiella pneumoniae ve Escherichia coli klinik suşlarında da görüldü.
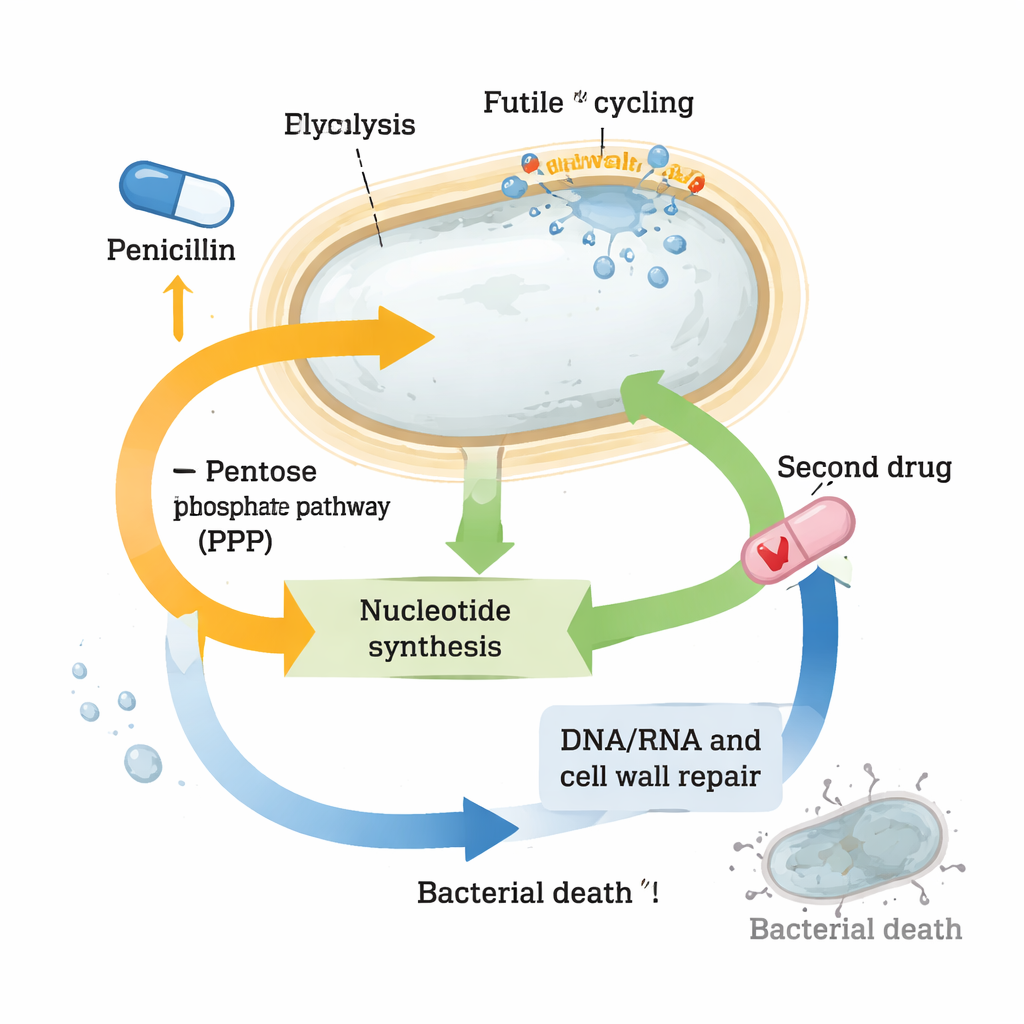
Hayatta kalma kimyasını terapötik bir avantaja çevirmek
Metabolizmalarını büyük ölçüde yeniden şekillendirmelerine rağmen, toleranslı sferoplastlar enerji parası ATP’lerini nispeten sabit tutmayı başarır ve yıkıcı hasardan kaçınır; bu da uzun antibiyotik maruziyetlerinde hayatta kalmalarına yardımcı olur. Ancak çalışma, bunu yaparken nükleotid havuzlarını uç noktaya kadar zorladıklarını gösteriyor. Bu hassas denge bir zayıflık yaratır: nükleotid metabolizmasını ikinci bir ilaçla biraz daha itmek savunmalarını çökerterek güçlü öldürmeyi geri getirir. Halkın anlayacağı şekilde sonuç şudur: bazı bakteriler antibiyotikleri hedefleri vuramadığı için değil, hücreler darbeyi atlatmak için hızla kimyalarını yeniden düzenledikleri için hayatta kalır. Bu hayatta kalma devrelerindeki —burada nükleotid metabolizmasındaki— zayıf bağlantıları bulup kullanarak, araştırmacılar eski antibiyotikleri bile yüksek toleransa sahip patojenleri alt edecek güçlü kombinasyon terapilerine dönüştürebilir.
Atıf: Keller, M.R., Kazi, M.I., Saleh, A. et al. Global response to antibiotic exposure reveals a critical role for nucleotide metabolism in high-level β-lactam tolerance. npj Antimicrob Resist 4, 11 (2026). https://doi.org/10.1038/s44259-026-00183-x
Anahtar kelimeler: antibiyotik toleransı, beta-laktam antibiyotikler, nükleotid metabolizması, bakteriyel persistanlık, ilaç kombinasyonları