Clear Sky Science · tr
Zebrafişte Fbln2–Nupr1b ekseni aracılığıyla epikardiyal aktivasyonun ve miyofibroblast bolluğunun azaltılması kalp rejenerasyonunu teşvik eder
Neden bazı kalpler kendilerini iyileştirebilir
Bir kişi kalp krizi geçirdiğinde, hasarlı kas genellikle asla tam olarak iyileşmeyen sert bir skar ile kaplanır. Akvaryumlarda yaşayan küçük çizgili balıklar olan zebrafişler ise bunun yerine dikkat çekici bir şey yapar: kalp dokusunu yeniden büyütür ve zamanla skarın çoğunu temizlerler. Bu çalışma, tıbbi sonuçları büyük olan yanıltıcı derecede basit bir soruyu soruyor: iyileşen bir kalp, ne zaman skar dokusu inşa edeceğini ve ne zaman onu kaldırıp yeni kasın büyümesine izin vereceğini nasıl bilir? Zebrafişteki bu dengeyi çözerek, çalışma yaralı insan kalplerinin başarısız olmak yerine kendilerini onarmasına yardımcı olabilecek stratejilere işaret ediyor.
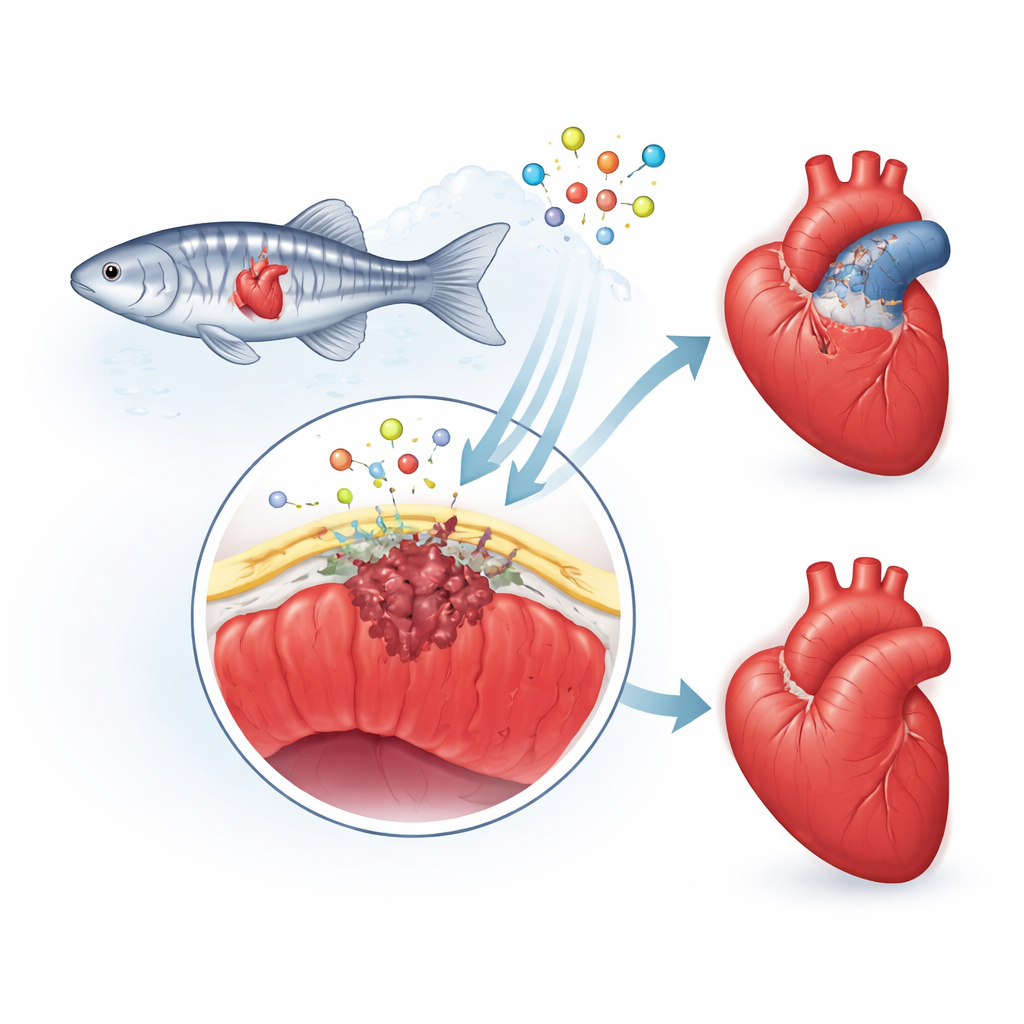
Kalbin koruyucu dış örtüsü
Araştırmacılar kalbi örten ince “deri” olan epikardiyuma odaklanıyor. Yaralanma sonrası bu katman uyanır, hücreleri kimlik değiştirir ve bazıları hasarlı bölgeye doğru ilerler. Orada destek hücreleri ve skar oluşturan hücreler haline gelirler ve yeni kan damarları ile kalp kası büyümesini yönlendiren kimyasal sinyaller salarlar. İnsanlarda bu onarım yanıtlama eğilimi aşırı olur ve geride kalın, kalıcı bir skar bırakır. Ancak zebrafişlerde skar geçicidir ve sağlıklı kas geri döndükçe kademeli olarak parçalanır. Ekip, kalbin çevresel iskelesinde bulunan fibulin-2 (Fbln2) adlı bir proteinin bu epikardiyal yanıtın hızını ve şiddetini belirlemeye yardımcı olabileceğini düşündü.
Skar oluşumunda moleküler bir kısma düğmesi
Zebrafişlerde gen düzenleme kullanarak, bilim insanları farklı Fbln2 düzeylerine sahip iki tür hayvan yarattılar: azaltılmış Fbln2’ye sahip bir soy ve proteinin tamamen çıkarıldığı başka bir soy. Balıkların kalplerini bir dondurma probuyla yaralayarak kalp krizini taklit ettiler ve iyileşmeyi haftalarca aylarca izlediler. Fbln2 düzeyleri düşürüldüğünde, erken aşamada kalp kası ve damar iç yüzeyi hücrelerinde bölünme azaldı, ancak oluşan lifli skar daha küçük ve yeniden modellenmesi daha kolaydı. Üç ayda bu kalpler iyi rejenerasyon göstermiş ve ana skar bileşeni olan kollajeni az tutmuştu. Buna karşılık, Fbln2 tamamen yok olan balıklarda TGFβ olarak bilinen sinyal ailesini içeren önemli bir büyüme ve skarlaşma yolunun daha güçlü bir şekilde kapanması görüldü ve epikardiyumun hemen altındaki skar oluşturucu hücre sayısı çok daha azdı. Erken skarları da daha küçüktü—ancak ilerleyen dönemde bu kalpler kollajeni temizleyemedi ve büyük, kalıcı skarlar ile kötü rejenerasyonla sonuçlandı.
Epikardiyal durum değişikliklerine yakın plan
Epikardiyal hücrelerin tek hücre çözünürlüğünde nasıl davrandığını görmek için ekip, yaralanmadan kısa süre sonra tek hücre RNA dizilemesi kullandı. Sessiz hücreler, yeni aktive olmuş hücreler, düşük oksijona uyum sağlayan stresli hücreler ve aktif olarak bölünen hücreler dahil olmak üzere birkaç epikardiyal hücre “durumu” tanımladılar. Normal Fbln2’ye sahip balıklarda epikardiyal hücreler sessiz halden aktive hale ve olgun hallerine sorunsuz şekilde ilerledi. Azaltılmış veya yok edilmiş Fbln2’ye sahip balıklarda bu ilerleme tıkandı: hücreler erken aşamalarda takıldı ve daha olgun aktive gruplar eksik kaldı, özellikle tam kayıp olanlarda. Normalde epikardiyal aktivasyon sırasında ve TGFβ sinyalleşmesine yanıt olarak açılan çok sayıda gen aşağıya çekildi; bu durum Fbln2’yi skar dokusunun oluşumu ve yeniden modellenmesi konusunda epikardiyumun ne kadar güçlü bir şekilde taahhütte bulunacağını belirleyen bir ayar düğmesi olarak işaretliyor.
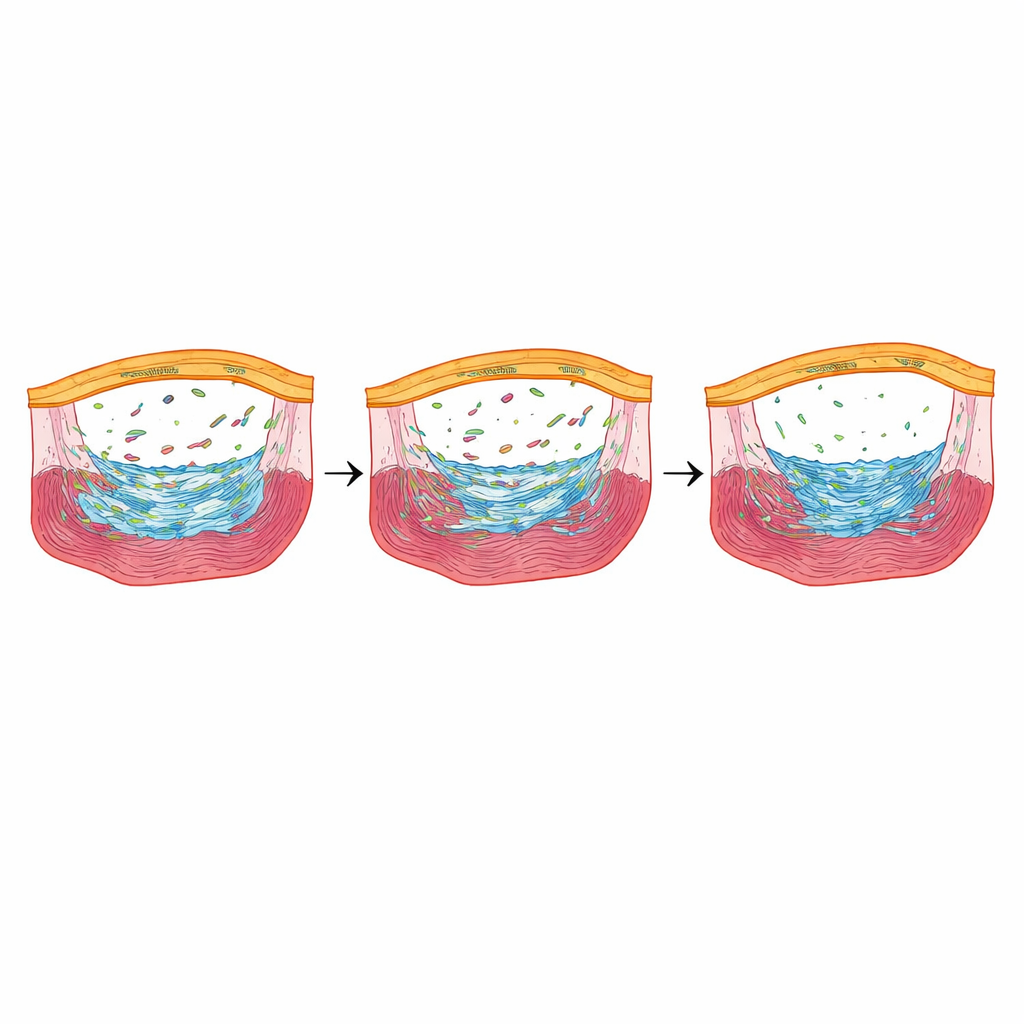
Onarma sürecini ince ayarlayan bir stres yanıtlayıcısı
Fbln2 azaltıldığında en belirgin şekilde azalan genler arasında bir tanesi öne çıktı: nupr1b, erken iyileşme sırasında epikardiyal hücrelerde aktif olan stres yanıtlayıcı bir düzenleyici. Araştırmacılar nupr1b’yi sildiklerinde, zebrafişlerde epikardiyal skar-forme eden hücreler daha az, kalp kası hücresi bölünmesi azalmış ve yaralanmadan aylar sonra büyük kollajen birikintileri korunmuştu—tamamen Fbln2 eksikliği gösteren balıklarla oldukça benzer. Çarpıcı şekilde, Fbln2 azaltılmış balıkların yalnızca epikardiyal hücrelerinde kısa süreli olarak nupr1b’yi yeniden etkinleştirdiklerinde, skar-forme eden hücre sayısı ve kalp kası hücre bölünmesi geri döndü ve geç dönemde skarlaşma arttı. TGFβ reseptörlerini kimyasal olarak bloke etmek nupr1b düzeylerini azalttı; bu da nupr1b’yi Fbln2–TGFβ sinyal ekseninin altında konumlandırdı.
İnsan kalbini iyileştirmek için bunun anlamı
Bu bulgular bir arada, zebrafiş kalplerinin çok az ile çok fazla fibrozis arasında ince bir ipte yürümelerine yardımcı olan bir “epikardiyal Fbln2–Nupr1b ekseni”ni ortaya koyuyor. Bu ekseni hafifçe azaltmak erken skar patlamasını yatıştırır ve verimli skar temizlemeyi teşvik ederken, onu tamamen kapatmak rejenerasyonu rayından çıkarır ve geride sert bir skar bırakır. İnsan tıbbı için ders, skarlaşmayı tamamen bloke etmenin hedef olmaması; bunun yerine onu ayarlamaktır—yırtılmayı önleyecek kadar yapı bırakırken skar dokusunun geçici olup sağlıklı kasa yerini almasını sağlayacak şekilde. Bu zebrafiş kontrol sisteminin anlaşılması ve nihayetinde kullanılması, yaralı insan kalbini kronik skarlaşma yerine gerçek rejenerasyona yönlendirebilecek gelecekteki tedavileri bilgilendirebilir.
Atıf: Kayman Kürekçi, G., Kaur Bajwa, G., Zhang, S. et al. Attenuation of epicardial activation and myofibroblast abundance via the Fbln2–Nupr1b axis stimulates cardiac regeneration in zebrafish. Nat Cardiovasc Res 5, 218–233 (2026). https://doi.org/10.1038/s44161-026-00785-8
Anahtar kelimeler: kalp rejenerasyonu, fibrozis, zebrafiş, epikardiyum, TGF-beta sinyalizasyonu