Clear Sky Science · tr
Gizli TGF-β1 aktivasyonunun seçici engellenmesi, iyi güvenlik ile doku fibrozisini baskılar
Neden gizli skarlaşma önemli
Birçok kronik hastalık, organlarımıza sert yara dokusu bırakarak (fibrozis olarak adlandırılan) sessizce zarar verir. Bu skarlaşma karaciğer, böbrekler, akciğerler ve hatta tümör çevresindeki normal fonksiyonu yavaşça boğabilir; tümör çevresindeki fibroz doku modern kanser immünoterapilerinin etkisini de azaltabilir. TGF-β1 proteini bu skarlaşma sürecinin merkezinde yer alır, ancak vücuttaki tüm TGF-β aktivitesini kapatmak tehlikeli oldu. Bu çalışma, zararlı TGF-β1 aktivasyonunu yalnızca seçici olarak engelleyecek şekilde tasarlanmış SOF10 adlı yeni bir antikoru tanımlıyor; SOF10 karaciğer hastalığı, böbrek yetmezliği ve kanserin hayvan modellerinde umut verici faydalar gösteriyor.
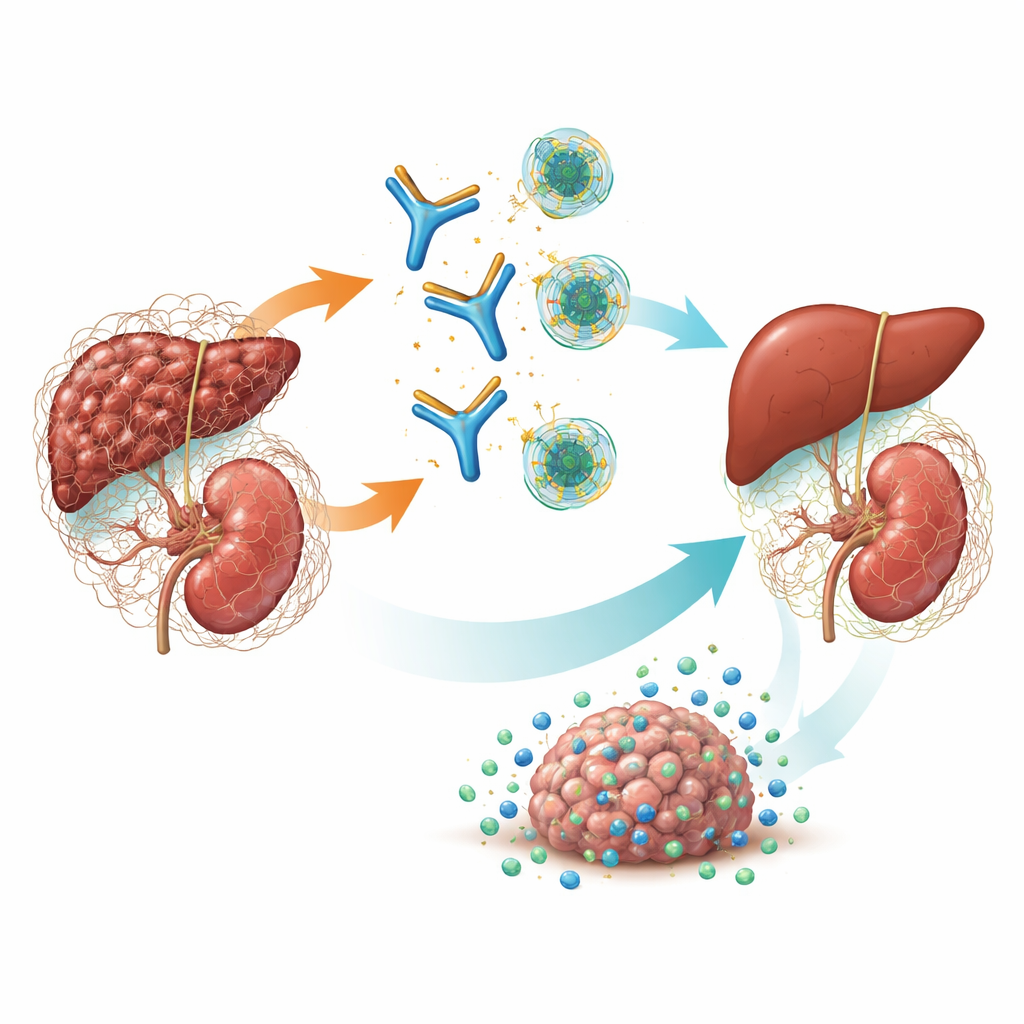
Skarlaşma ve kanser için bir ana anahtar
TGF-β, hücrelerin nasıl büyüdüğünü, iyileştiğini ve bağışıklık sistemiyle nasıl etkileştiğini kontrol etmeye yardımcı olan güçlü bir sinyal molekülüdür. Kronik hastalıkta bir formu—TGF-β1—fibroblastları aşırı bağ dokusu üretmeye yönlendirir; bu da organların sertleşmesine ve işlev kaybına yol açar. Ayrıca tümörlerin etrafında bağışıklığı baskılayan, fibrotik bir kabuk oluşturarak bağışıklık hücrelerinin ve ilaçların kanser hücrelerine ulaşmasını engeller. Önceki ilaçlar üç TGF-β formunun tümünü aynı anda kapatmaya çalıştı, ancak bu “pan-engelleme” kalp kapak hasarı, kanama ve cilt tümörleri gibi ciddi yan etkilere neden oldu. Genetik çalışmalar ve önceki modeller TGF-β1’in fibrotik böbrek hastalıkları ve birçok katı tümörde asıl suçlu olduğunu öne sürdü; bu da yalnızca bu izoformu dikkatli şekilde hedeflemenin etkili ve daha güvenli olabileceği olasılığını doğurdu.
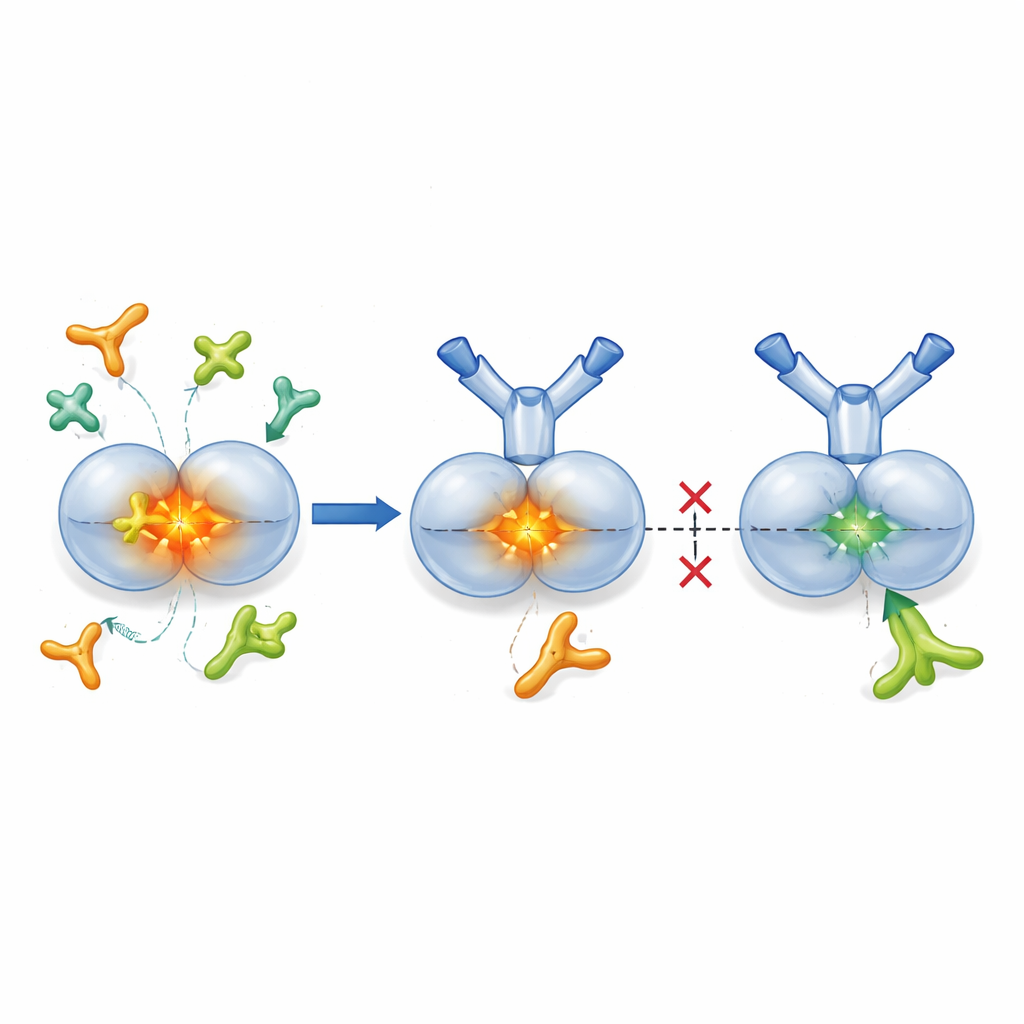
TGF-β1’i inaktif formunda kilitlemek
TGF-β1 normalde aktif çekirdeğin, gerektiğinde açılana kadar kapalı tutan bir partner proteiniyle sarıldığı “latent” bir paket içinde üretilir. Proteaz adı verilen enzimler ve integrinler olarak bilinen bazı hücre yüzeyi bağlayıcı proteinler bu paketi açarak aktif TGF-β1’in serbest kalmasına izin verebilir. Araştırmacılar SOF10’u, latent TGF-β1 formuna bağlanan—aktif hormona veya diğer izoformlara bağlanmayan—insanlaştırılmış bir antikor olarak tasarladı. X-ışını kristalografisi ile yapılan yapısal çalışmalar, SOF10’un latent kompleksin iki yarısı arasındaki arayüze yerleşerek onu bir kelepçe gibi stabilize ettiğini gösterdi. Laboratuvar testlerinde bu, proteazların ve bir integrin (αvβ8)’in aktif TGF-β1’i serbest bırakmasını engelledi; öte yandan sağlıklı dokulardaki bağışıklık dengesini korumada önemli olan başka bir integrin (αvβ6) büyük ölçüde etkilenmedi. Etkisi itibarıyla SOF10 zararlı aktivasyon yollarını seçici olarak sustururken ana bir homeostatik yolu koruyor.
Karaciğer ve böbrekleri yavaş hasardan korumak
Bu seçici TGF-β1 kelepçesinin gerçekten skarlaşmayı sınırlayıp sınırlayamayacağını görmek için ekip SOF10’u birkaç fare modelinde test etti. Karaciğer fibrotizine ilerleyen hızlı diyet kaynaklı bir yağlı karaciğer modeliyle yapılan çalışmada, SOF10 tedavisi karaciğerin TGF-β yanıtlı genler ve kollajen yapım genlerindeki ifadeyi azalttı ve biriken skar dokusunun kimyasal belirteci olan hidroksiprolini düşürdü. İki farklı böbrek modelinde—interstisyel fibrozise yol açan cerrahi tıkanma modeli ve hem glomerüler skarlaşma hem de böbrek yetmezliği gelişen genetik Alport sendromu modeli—SOF10 fibrotik gen aktivitesini azalttı, kollajen içeriğini düşürdü ve mikroskop altında skarlaşmış alanları görünür şekilde küçültti. Kronik Alport modelinde kan testleri böbrek fonksiyonunda düzelme gösterdi ve bu faydalar daha geniş TGF-β bloklayan bir antikorla benzer düzeydeydi—ancak diğer TGF-β izoformlarını bloklamadan sağlandı.
Tümör içindeki bağışıklık sistemini serbest bırakmak
Tümör çevresindeki fibrotik doku hem fiziksel bir bariyer hem de bağışıklığı frenleyen bir etki gösterebileceğinden, araştırmacılar SOF10’un kontrol noktası inhibitörü ilaçlara yanıtı iyileştirip iyileştirmeyeceğini sordular. Anti–PD-L1 tedavisine normalde zayıf yanıt veren fare meme ve kolon kanseri modellerinde, SOF10’u eklemek tümör büyümesini önemli ölçüde yavaşlattı; oysa SOF10 veya anti–PD-L1 tek başına pek etkili değildi. Kombinasyonla tedavi edilen hayvanların tümörlerinde daha fazla öldürücü CD8 T hücresi ve bu hücrelerin kanser hücrelerini yok etmek için kullandığı toksik enzimlerden daha fazla bulundu. Bu tümörlerden alınan fibroblastlar kollajen ve matris yapım yollarında daha düşük aktivite gösterirken interferon ve antijen sunumu yollarında daha yüksek aktivite sergiledi; bu, daha bağışıklık-destekleyici bir stroma yönünde bir kayışı işaret ediyor. Bu değişiklikler geniş TGF-β engelleme ile görülenleri yakından yansıtıyor; bu da yalnızca latent TGF-β1’i hedeflemenin tümör ortamını benzer şekilde yeniden programlayabileceğini düşündürüyor.
Hayvanlarda güvenlik sinyalleri
TGF-β’yi geniş çapta engelleme girişimleri önceki yıllarda güvenlik sorunlarıyla karşılaştığı için ekip farelerde ve siyrecus maymunlarında 13 haftalık toksikoloji çalışmaları yürüttü ve tekrarlı yüksek dozlarda SOF10 verdi. İlaç kanda tipik bir antikor davranışı sergiledi ve geniş bir doz aralığında başlıca organlarda hasar, kan hücresi sayımlarında bozulma veya kalp ve akciğer fonksiyonlarında bulgu görülmedi. Farelerde iki haftada bir 200 mg/kg’ye ve maymunlarda 100 mg/kg’ye kadar test edilen en yüksek dozlar zararlı etki gözlemlenemeyen düzeyler olarak belirlendi. Bu güvenlik profili, TGF-β2, TGF-β3 ve αvβ6 aracılı aktivasyonun korunmasının önceki, daha az seçici yaklaşımlarda görülen riskleri azalttığı fikrini destekliyor.
Bu hastalar için ne anlama gelebilir
Bir arada değerlendirildiğinde bulgular, tüm TGF-β sinyalini silmek yerine TGF-β1’i inaktif kabuğunda kilitlemenin birçok organdaki skarlaşmayı hafifletebileceğini, böbrek fonksiyonunu iyileştirebileceğini ve inatçı tümörleri immünoterapiye karşı daha hassas hale getirebileceğini; tümünün hayvan testlerinde cesaret verici bir güvenlik ile sağlanabileceğini öne sürüyor. İnsan çalışmalarının bu faydaları doğrulaması ve uzun vadeli etkileri izlemesi gerekir; yine de SOF10 ve benzeri stratejiler kronik fibrotik hastalıklar ve belirli kanserleri tedavi etmek için yara dokusunu azaltırken dokuların iyileştirici ve bağışıklık-dengeleyici rollerini koruyan yeni bir yol açabilir.
Atıf: Kanamori, M., Sato, I., Koo, C.X. et al. Selective blockade of latent TGF-β1 activation suppresses tissue fibrosis with good safety. Commun Med 6, 131 (2026). https://doi.org/10.1038/s43856-026-01408-w
Anahtar kelimeler: fibrozis, TGF-beta1, monoklonal antikor, böbrek ve karaciğer hastalığı, kanser immünoterapisi