Clear Sky Science · tr
Üçlü negatif meme kanserlerinin mekansal protein profillemesinden sonuç tahmini
Neden kanser hücrelerinin düzeni önemlidir
Hekimler agresif bir meme kanserini mikroskop altında incelediklerinde, tümör hücreleri, bağışıklık hücreleri ve destekleyici dokunun sıkışık bir manzarasını görürler. Ancak yakın zamana kadar çoğu test belirli bir molekülün ne kadar bulunduğuna odaklanmıştı; nerede bulunduğu ise göz ardı ediliyordu. Bu çalışma, üçlü negatif meme kanserlerindeki proteinlerin ve hücrelerin fiziksel düzeninin hastaların gidişatını öngörebildiğini gösteriyor ve bu mekansal desenleri yüksek ayrıntılı görüntülerden doğrudan okumaya yarayan yeni bir yöntem sunuyor.
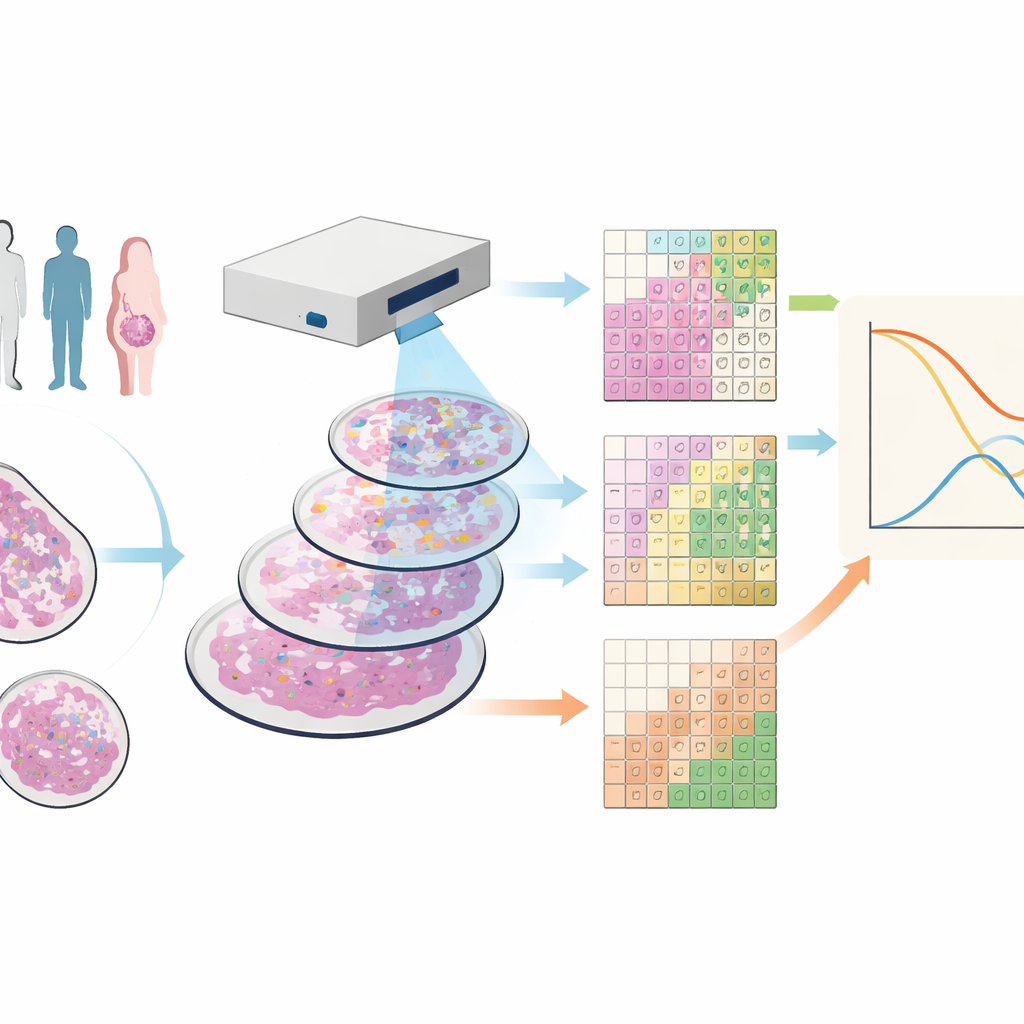
Kansere çok renkli bakmak
Araştırmacılar, sık görülen ilaç hedeflerinden yoksun ve sıklıkla kötü prognoza sahip bir hastalık türü olan üçlü negatif meme kanseri olan 88 kişiye ait doku örnekleri ile çalıştı. Her örneği onlarca metal etiketli antikorla boyayan görüntüleme kütle sitometrisi adlı bir teknik kullandılar. Özel bir tarayıcı altında bu, dokudaki her noktanın birçok farklı proteinin ayrıntılı bir parmak izini taşıdığı görüntüler üretiyor; böylece tümör hücreleri, çeşitli bağışıklık hücreleri, kan damarları ve yapısal lifler aynı anda ortaya çıkıyor.
Hücreler yerine görüntüyü karolara ayırmak
Mevcut araçların çoğu her hücrenin sınırlarını çizmeye ve ardından bunları türlerine göre sınıflandırmaya çalışıyor; bu süreç özellikle hücrelerin yalnızca kısmen yakalandığı ince doku kesitlerinde hata yapmaya ve yavaş olmaya elverişlidir. Ekip bunun yerine SparTile adlı bir yöntem geliştirdi; bu yöntem bireysel hücre çizgilerini atlıyor. SparTile her görüntüyü birçok küçük örtüşen kareye, yani karoya böler ve bu karolardaki protein kombinasyonlarının tekrarlayan desenlerini öğrenmek için matematiksel teknikler kullanır. Önce karoları tümör, destekleyici doku (stroma) veya bağışıklık açısından zengin bölgeler gibi geniş alanlara ayırır, ardından her bölgeyi kendi protein karışımı ve komşu hücre türleriyle daha spesifik “mikroçevreler” olarak daha ileri düzeyde böler.
Hastalık sonuçlarıyla bağlantılı gizli mahalleler
Bu mikroçevreler haritalandıktan sonra, bilim insanları her desenden her hastanın örneğinde ne kadar bulunduğunu ölçtüler ve bunu uzun dönem sağkalımla karşılaştırdılar. Bir dizi çarpıcı bağlantı ortaya çıktı. MX1 adlı bir protein ve myeloid bağışıklık hücrelerinin belirteçleri açısından zengin tümör merkezli bir mikroçevre, çok daha yüksek ölüm riski ile ilişkili bulundu. Vimentin ile işaretlenen başka bir tümör deseni—tümör hücrelerinin daha hareketli, invazif bir duruma kaydığının bir göstergesi—ayrıca kötü sağkalımla güçlü şekilde ilişkilendirildi. Buna karşılık, belirli T hücrelerinin hakim olduğu alanlar daha iyi sonuçlarla bağlantılıydı; B hücreleri açısından zengin bölgeler ise analiz edilen küçük doku çekirdeklerinde nadir oldukları için daha zayıf etkiler gösterdi.
Tümör ve bağışıklık hücreleri arasındaki mesafe uyarı işareti
Belli mahallelerin varlığının ötesinde, onların mekansal ilişkileri de önemliydi. Ekip, tümör bölgeleri ile myeloid bağışıklık bölgelerinin birbirine ne kadar yakın oturduğunu, protein sinyallerinin mekânda ne kadar örtüştüğünün istatistiksel bir ölçüsünü hesaplayarak sordu. Tümör hücreleri arasına sıkışmış myeloid açısından zengin alanlara sahip hastalar, bu iki popülasyonun daha ayrı olduğu hastalara göre genelde daha kötü sonuçlar gösterdi. Bu “mesafe” ölçüsü, standart klinik faktörler dikkate alındıktan sonra bile güçlü bir risk belirteci olarak kaldı ve öneminini, diğer araştırma gruplarından gelen iki bağımsız meme kanseri görüntü veri setinde test edildiğinde de korudu.
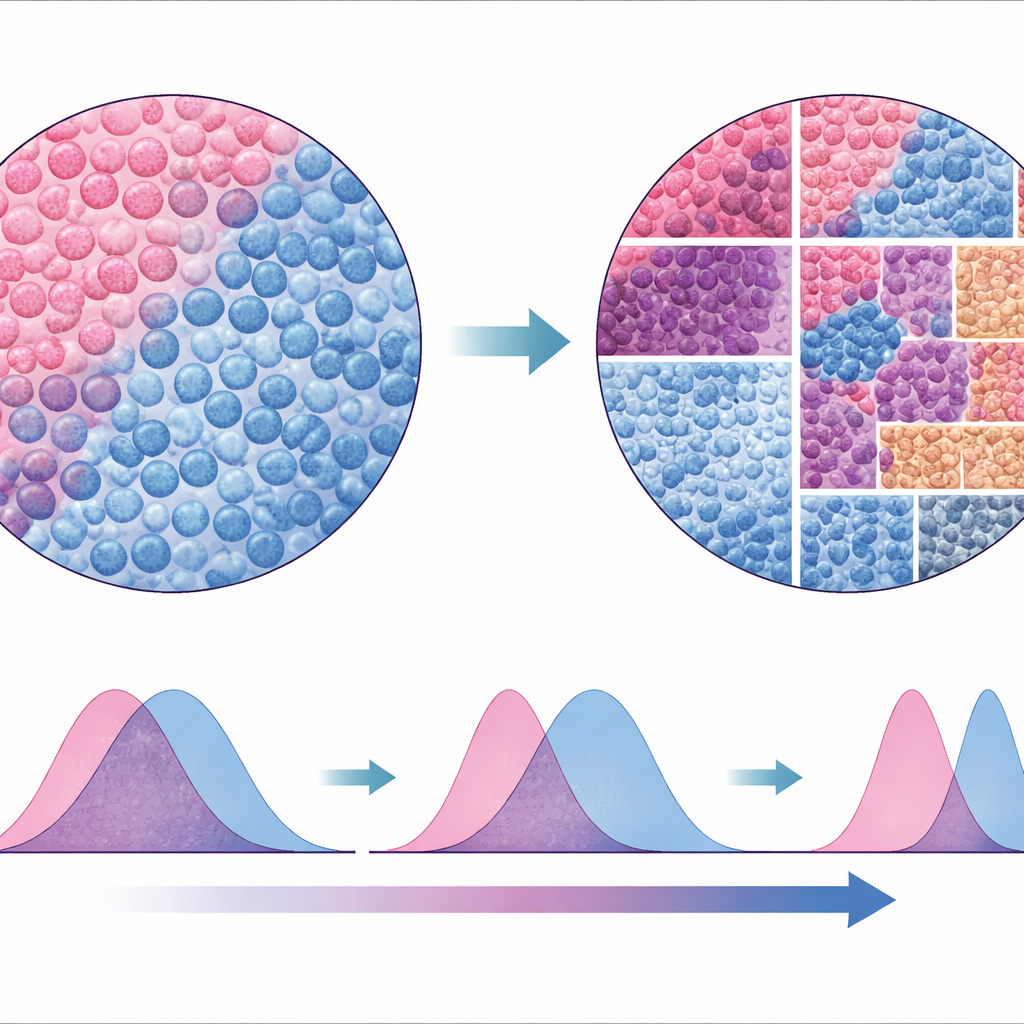
Tümör manzarasını okumak için yeni bir yol
Yaklaşımın ne kadar sağlam olduğunu test etmek için yazarlar SparTile’ı bireysel hücreleri segmentlemeye ve sınıflandırmaya, ardından etraflarında mahalleler oluşturmaya dayanan geleneksel yöntemlerle karşılaştırdı. Hücre tabanlı analizler bazı aynı desenleri geri getirse de, veri setleri arasında daha az tutarlıydı ve MX1 ile myeloid hücreleri içeren bazı riskli mikroçevreleri işaretlemede daha az güvenilir çıktılar verdi. SparTile ham protein görüntüleri üzerinde doğrudan çalıştığı için hücre bazlı yaklaşımların birçok varsayımından ve teknik tuzaklarından kaçınıyor; yine de deney veya tedavi planlaması için ayrıntılı hücre türlerine ihtiyaç duyulduğunda sonradan onlarla birleştirilebiliyor.
Bu hastalar ve gelecekteki bakım için ne anlama geliyor
Bu çalışma, bir tümörün yalnızca içerdiği bileşenlerin değil, aynı zamanda düzeninin de üçlü negatif meme kanseri hastasının gidişatını tahmin etmede önemli olduğunu gösteriyor. Karmaşık, çok-proteinli görüntüleri yorumlanabilir mekansal desenlere ve basit mesafe ölçülerine dönüştürerek SparTile, küçük doku örneklerinden yüksek riskli hastaları tespit etme ve gelecekteki tedavilerle hedeflenebilecek biyolojik düzenleri ortaya çıkarma yolu sunuyor. Rutin bakımda rehberlik etmeden önce daha fazla doğrulamaya ihtiyaç olsa da, yaklaşım tümörün “haritasının” moleküler parça listesi kadar önemli olduğu bir geleceğe işaret ediyor.
Atıf: Foroughi pour, A., Wu, TC., Noorbakhsh, J. et al. Prediction of outcome from spatial Protein profiling of triple-negative breast cancers. Commun Med 6, 133 (2026). https://doi.org/10.1038/s43856-026-01400-4
Anahtar kelimeler: üçlü negatif meme kanseri, tümör mikroçevresi, mekansal proteomik, görüntüleme kütle sitometrisi, prognostik biyobelirteçler