Clear Sky Science · tr
Primer ER-pozitif ve HER2-negatif meme kanserinde homolog rekombinasyon yetmezliği
Bu, meme kanseri hastaları için neden önemli
Meme kanserlerinin çoğu östrojen reseptör‑pozitif ve HER2‑negatif olarak adlandırılan geniş bir gruba girer. Bu tümörler genellikle hormon engelleyen ilaçlarla, bazen kemoterapi ile birlikte tedavi edilir. Yine de birçok hasta nüks eder ve doktorların kimlerin gerçekten yoğun tedaviye ihtiyacı olduğunu ya da kimlerin yeni hedefe yönelik ilaçlardan yararlanabileceğini kesin olarak belirleyecek hassas araçları eksiktir. Bu çalışma, bazı tümörlerde bulunan ve homolog rekombinasyon yetmezliği (HRD) olarak adlandırılan belirli bir zayıflığı inceliyor; bu zayıflık kanser hücrelerinin kırık DNA’yı onarmakta yetersiz kalmasına yol açıyor ve bu da daha kişiselleştirilmiş tedavi olanaklarını mümkün kılabilir.
Sadece bazı tümörlerde gizli bir zayıflık
Homolog rekombinasyon, hücrenin tehlikeli DNA kırıklarını onarmada kullandığı ana sistemlerden biridir. Bu sistem bozulduğunda—çoğunlukla BRCA1, BRCA2, PALB2 veya RAD51C gibi iyi bilinen genlerdeki kusurlar nedeniyle—hücreler mutasyon biriktirir ve platin bazlı kemoterapiler ile PARP inhibitörleri de dahil belirli ilaçlara karşı özellikle duyarlı hale gelebilir. HRD, triple‑negatif olarak adlandırılan daha agresif bir meme kanseri formunda yaygındır, ancak daha sık görülen östrojen‑reseptör pozitif, HER2‑negatif gruptaki rolü belirsiz kalmıştır. Bunu açıklığa kavuşturmak için araştırmacılar, İsveç SCAN‑B çalışmasından 502 böyle tümörü tüm‑genom dizileme ile, eşleşen gen aktivitesi, DNA metilasyonu, uygulanan tedaviler ve uzun dönem sonuç verileriyle birlikte analiz etti.
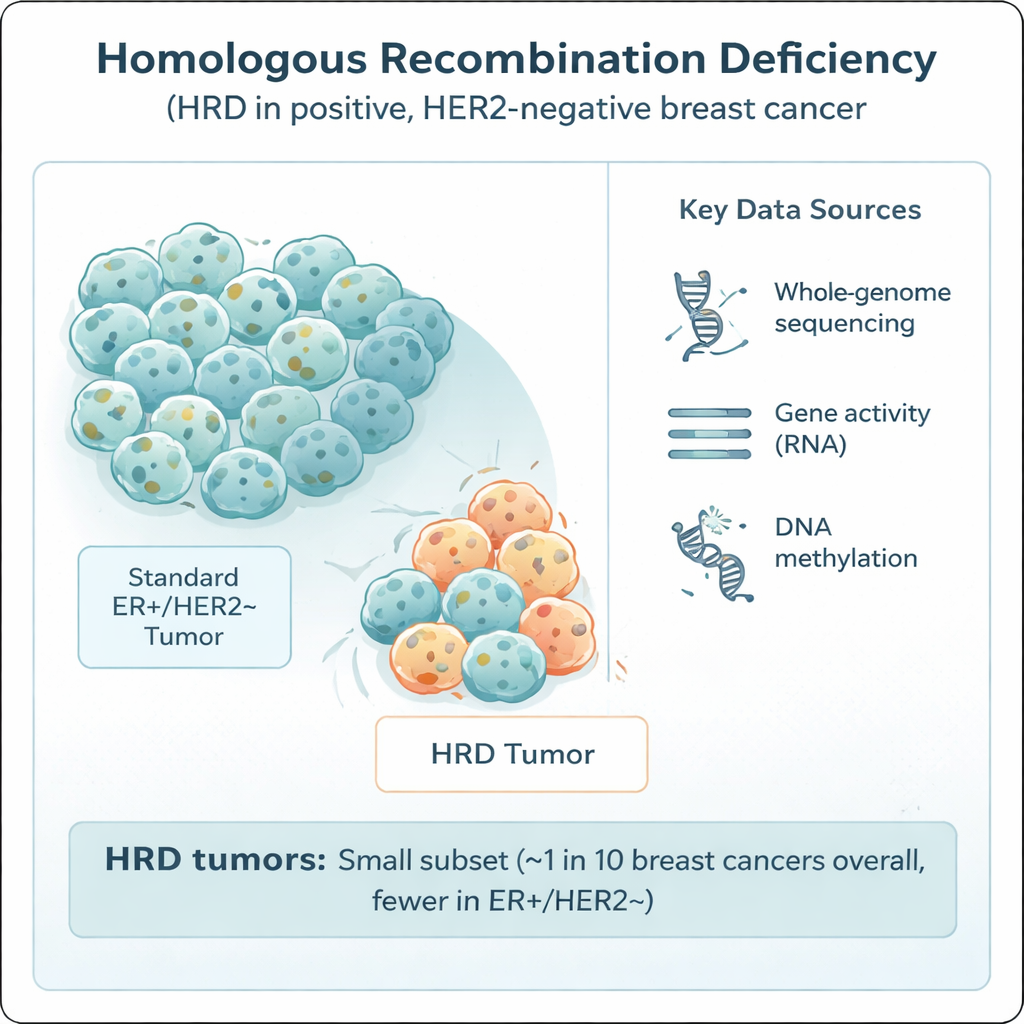
Çalışma nasıl yapıldı
Tüm tümörler cerrahi sırasında, herhangi bir ilaç tedavisinden önce toplandı; bu, orijinal biyolojilerinin net bir anlık görüntüsünü sağlar. Ekip, homolog rekombinasyon bozulduğunda kanser DNA’sında kalan "mutasyonel imzaları" okumak için gelişmiş bir desen tanıma aracı olan HRDetect’i kullandı. Tümörler, sıkı bir olasılık eşiğini aştıkları takdirde HRD olarak etiketlendi. Bilim insanları ayrıca HRD’yi tespit etmenin farklı yollarını—diğer DNA tabanlı skorlar ile RNA tabanlı gen ifade testini—karşılaştırarak farklı yöntemlerin ne kadar tutarlı olduğunu inceledi. Buna ek olarak daha geniş özellikler de incelendi: genel mutasyon yükü, kromozomal kazanç ve kayıp desenleri, bağışıklıkla ilişkili gen aktivitesi ve genleri açıp kapatabilen DNA üzerindeki kimyasal işaretler (metilasyon).
HRD ne kadar yaygın ve neden kaynaklanıyor?
Araştırmacılar dizilenen gruptaki östrojen‑reseptör pozitif, HER2‑negatif tümörlerin yalnızca %8,4’ünün güçlü HRD kanıtı gösterdiğini buldular—bu, triple‑negatif hastalıkta görülen yaklaşık %60’a kıyasla çok daha düşük. Bu verileri ulusal kayıt bilgileri ve diğer çalışmalarla birleştirerek, bu klinik altgruptaki tümörlerin yaklaşık yirmide birinin, Batı Avrupa/Kuzey Avrupa nüfuslarındaki tüm meme kanserlerinin ise yaklaşık dokuzda birinin HRD olduğunu tahmin ettiler. HRD tümörlerinde genellikle muhtemel bir neden saptanabiliyordu: yaklaşık %70’inde BRCA1, BRCA2, RAD51C veya PALB2’de kalıtsal mutasyonlar, tümöre özgü mutasyonlar veya delesyonlar ya da gen promotörlerinin epigenetik susturulması yoluyla açık hasar vardı. Dikkat çekici olarak HRD olgularının yaklaşık üçte birinde promotör hipermetilasyonu—DNA onarım genlerini diziyi değiştirmeden kapatan ek bir kimyasal kaplama—sorumluydu. Ancak yaklaşık %30’unda belirgin tek bir neden bulunamadı; bu da onarım yetmezliğine yol açan ek, henüz keşfedilmemiş yolların olduğunu düşündürüyor.
HRD tümörleri mikroskopta ve klinikte nasıl görünüyor
Bu yaygın meme kanseri grubundaki HRD tümörleri genellikle daha agresif hastalığın özelliklerini gösteriyordu: sıklıkla daha yüksek hücre bölünme oranları, daha düşük hormon reseptör boyanma seviyeleri ve HR‑yeterli tümörlere kıyasla daha karmaşık, mutasyon bakımından zengin genomlar vardı. Neredeyse tüm ana moleküler alt tiplere yayılmışlardı, ancak daha sinsi Luminal A sınıfında nadir, daha küçük bir basal‑benzeri alt kümede ise göreli olarak zengindi. Araştırmacılar toplam gen aktivitesi ve DNA metilasyon desenlerine baktıklarında ise HRD tümörleri tek, kolayca tanınan bir profile uymadı. Bunun yerine ifade desenleri çeşitlilik gösteriyordu ve belirli alt tipler içindeki farklılıklar ılımlıydı. Bazı HRD tümörleri, özellikle Luminal B ve basal‑benzeri gruplarda, daha yüksek bağışıklık aktivitesi sinyalleri ve artmış PD‑L1 ifadesi gösteriyordu; bu da onların bağışıklık sistemi tarafından daha görünür olabileceği ve potansiyel olarak immünoterapilere daha iyi yanıt verebileceği izlenimini veriyor.
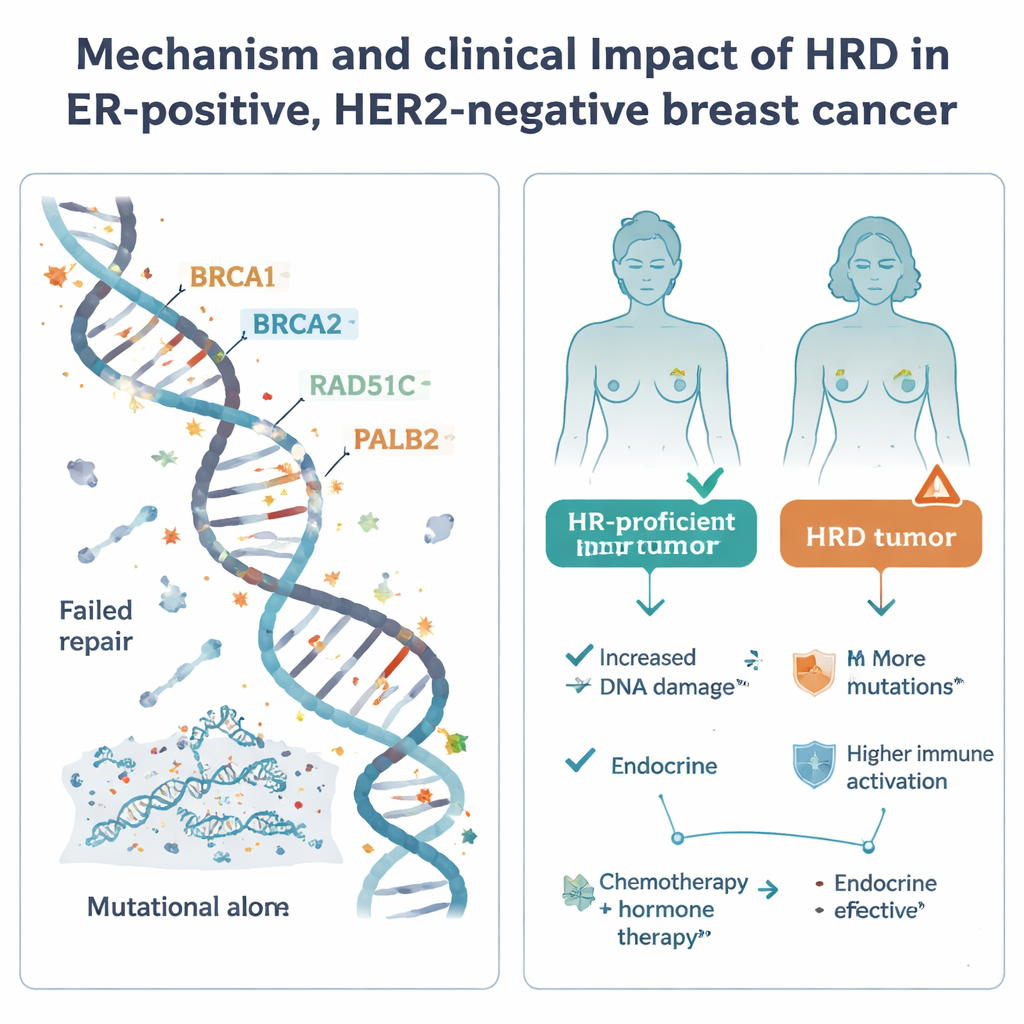
HRD hasta sonuçlarını değiştiriyor mu?
Çalışma sonra HRD durumunun standart bakım altındaki gerçek dünya sonuçlarıyla nasıl ilişkili olduğunu inceledi. Cerrahi sonrası yalnızca hormon tedavisi alan hastalarda HRD tümörleri uzak nüksten uzak‑serbest sağkalım açısından daha kötü olma eğilimi gösterdi; ancak HRD olgularının sayısı azdı ve sonuç resmi istatistiksel olarak anlamlılık sınırına ulaşmadı. Bu desen, agresif moleküler özellikleriyle birlikte, sadece endokrin tedaviye dayanmanın HRD olan hastalar için riskli olabileceğini düşündürüyor. Buna karşılık, hem kemoterapi hem hormon tedavisi alan hastalar arasında HRD durumu açıkça daha iyi ya da daha kötü sonuçlarla ilişkilendirilemedi; tüm gruplar genel olarak benzer nüks oranlarına sahipti ve kemoterapinin HRD tümörlerdeki ek riski bir ölçüde hafiflettiği düşünülebilir.
Bu, gelecekteki tedavi seçimleri için ne anlama geliyor
Genel okuyucu için temel mesaj, östrojen‑reseptör pozitif, HER2‑negatif meme kanserlerinin yalnızca azınlığında bu özel DNA‑onarım zayıflığının bulunduğudur; ancak mevcut olduğunda genellikle hormon tedavisiyle iyi kontrol edilmeyebilen daha agresif hastalığı işaret etme eğilimindedir. Çalışma, tüm‑genom dizilemenin HRD’yi güvenilir biçimde saptayabileceğini ve yalnızca kalıtsal BRCA1 veya BRCA2 testiyle sınırlı kalmayarak altında yatan nedenleri aydınlatabileceğini destekliyor. Çalışma henüz HRD durumuna göre tedaviyi değiştirmenin sağkalımı artırdığını kanıtlamasa da, HRD tümörlü hastaların kemoterapiden ve gelecekteki çalışmalarda PARP inhibitörleri ya da immünoterapilerden fayda görebileceğine dair erken kanıt sağlıyor. Kısacası, HRD testi her hastanın meme kanserinin biyolojisine göre tedavi yoğunluğunu ve yeni hedefe yönelik seçenekleri uyarlamak için daha rafine bir araç setinin bir parçası haline gelebilir.
Atıf: Davies, H.R., Black, D., Kvist, A. et al. Homologous recombination deficiency in primary ER-positive and HER2-negative breast cancer. Commun Med 6, 118 (2026). https://doi.org/10.1038/s43856-026-01385-0
Anahtar kelimeler: meme kanseri, DNA onarımı, BRCA genleri, genom dizilemesi, hedefe yönelik tedavi