Clear Sky Science · tr
Akciğer ve over kanserinde platin bazlı kemoterapiye karşı tedavi direnci, hedeflenebilir bir TGFβ yaşlanma salgı profili tarafından yönlendirilir
Kanser Tedavisi Geri Tepince
Platin bazlı kemoterapi, özellikle akciğer ve over kanserlerinde modern kanser tedavisinin temel taşlarından biridir. Amaç, tümör DNA’sını o kadar hasarlandırmaktır ki kanser hücreleri artık bölünemesin. Buna rağmen birçok hastada tümörler ilk başta küçülür, sonra hastalık geri döner ve daha zorlu bir hal alır. Bu çalışma basit ama rahatsız edici bir soruyu gündeme getiriyor: hayat kurtaran ilaçlar, sağ kalan kanser hücrelerinin toparlanmasına da yardım eder mi? Yazarlar bunun cevabını, özel bir grup hasar görmüş, yaşlanmaya benzer hücrede ve bunların gönderdiği güçlü kimyasal mesajlarda buluyorlar.
Yaşlanan Kanser Hücrelerinin Çift Hayatı
Kemoterapi tüm tümör hücrelerini aynı şekilde etkilemez. Bazıları doğrudan öldürülür, bazıları ise bölünmesi kalıcı olarak durdurulmuş ama hayatta kalan bir durum olan hücresel senesense girer. Bu senescent hücreler şişer ve sensensens ile ilişkili salgı fenotipi (SASP) olarak bilinen bir protein ve sinyal kokteyli salgılamaya başlar. Araştırmacılar insan akciğer ve over kanseri hücreleri ile fare modellerinde gösterdiler ki, sisplatin ve karboplatin gibi platin ilaçlar özellikle güçlü senescent hücreler oluşturur. Taze kanser hücreleri bu senescent kültürlerden alınan sıvıya maruz bırakıldığında, kontrol hücrelerine göre daha hızlı büyüdüler, daha kolay göç ettiler ve daha büyük, daha agresif kümeler ve küreler oluşturdular.
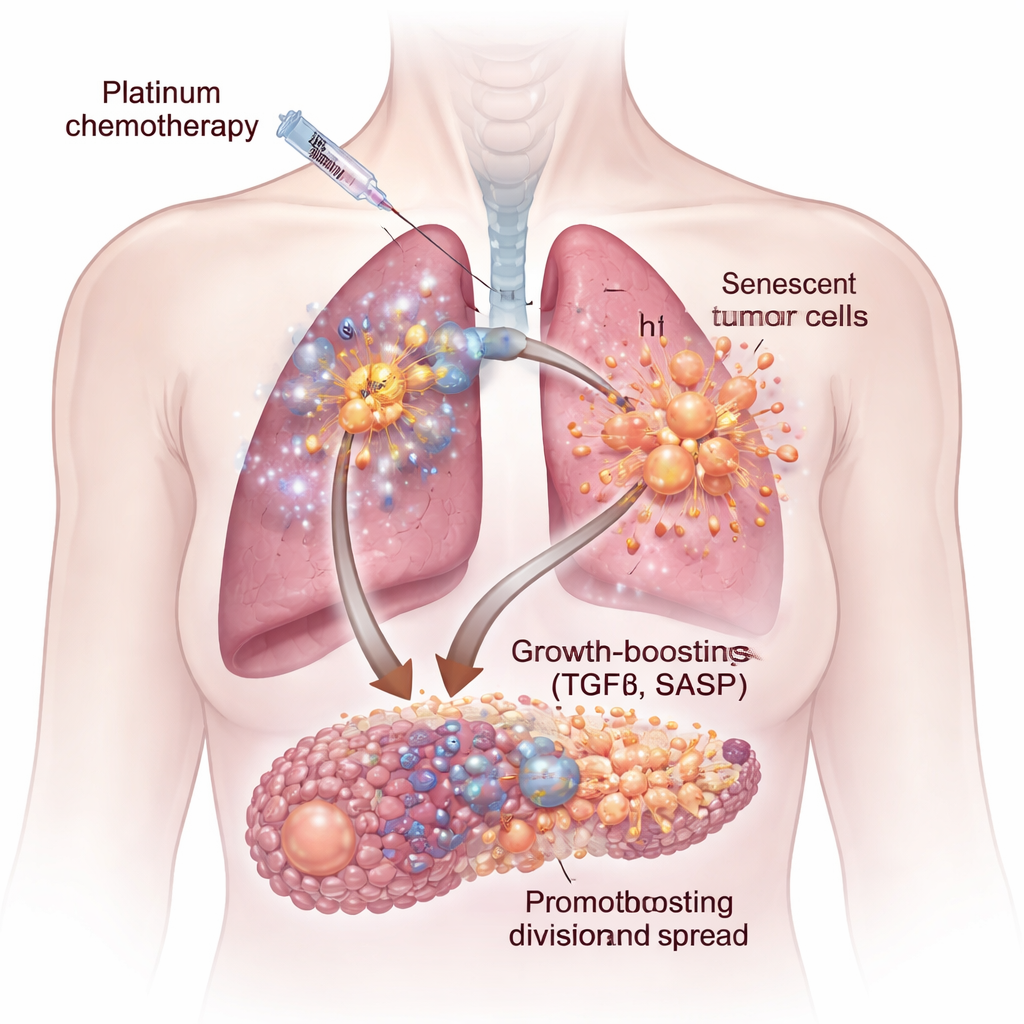
Gizli Bir Büyüme Sinyali: TGFβ
Tüm kemoterapiler aynı zararlı salgıları tetiklemedi. Araştırma ekibi platin ilaçları iki diğer yaygın ajan olan doksetaksel ve palbociklib ile karşılaştırdığında, yalnızca platinle muamele edilmiş hücrelerin tümör büyümesini güçlü biçimde destekleyen bir SASP ürettiğini buldu. Gen ekspresyon çalışmaları, protein ölçümleri ve yüksek verimli bir mikroçevre mikroarray’inin birleştirilmesiyle kilit bir suçlu tespit ettiler: dönüştürücü büyüme faktörü-beta yani TGFβ sinyal molekülü. Sisplatinin indüklediği senescent hücreler çoklu TGFβ formları ve ilgili yolaklar bakımından zengindi. Saflaştırılmış TGFβ’nin kanser hücrelerine eklenmesi, senescent hücre sıvısıyla gözlemlenen büyüme artışını taklit etti; bu da bu sitokin ailesini pro-tümör salgısının merkezi bir sürücüsü olarak öne çıkarıyor.
Sinyal Kanser Hücrelerini Nasıl Yeniden Programlıyor
Çalışma daha sonra bu TGFβ açısından zengin sinyallerin komşu tümör hücrelerinin davranışını nasıl değiştirdiğini izledi. Alıcı hücrelerin yüzeyinde TGFβ, TGFBR1 adlı bir reseptöre bağlanır. Bu da sırasıyla AKT ve mTOR yolakları başta olmak üzere hücre içi bir protein zincirini aktifleştirir; bu yolaklar hücre büyümesi, metabolizma ve hayatta kalımı kontrol eder. Hem insan hem fare akciğer kanseri hücrelerinde, cisplatinden türeyen salgılara maruz kalma AKT’ın ve onun aşağı akış hedefi p70S6K’nın aktive (fosforile) formlarını hızla artırdı ve hücre döngüsü genlerinin ekspresyonunu yükseltti. TGFBR1’i galunisertib adlı bir ilaçla bloke etmek veya doğrudan mTOR’u inhibe etmek, bu sinyal patlamasını büyük oranda durdurdu ve senescent salgısının tetiklediği fazladan proliferasyon, koloni oluşumu ve invaziv küre büyümesini azalttı.
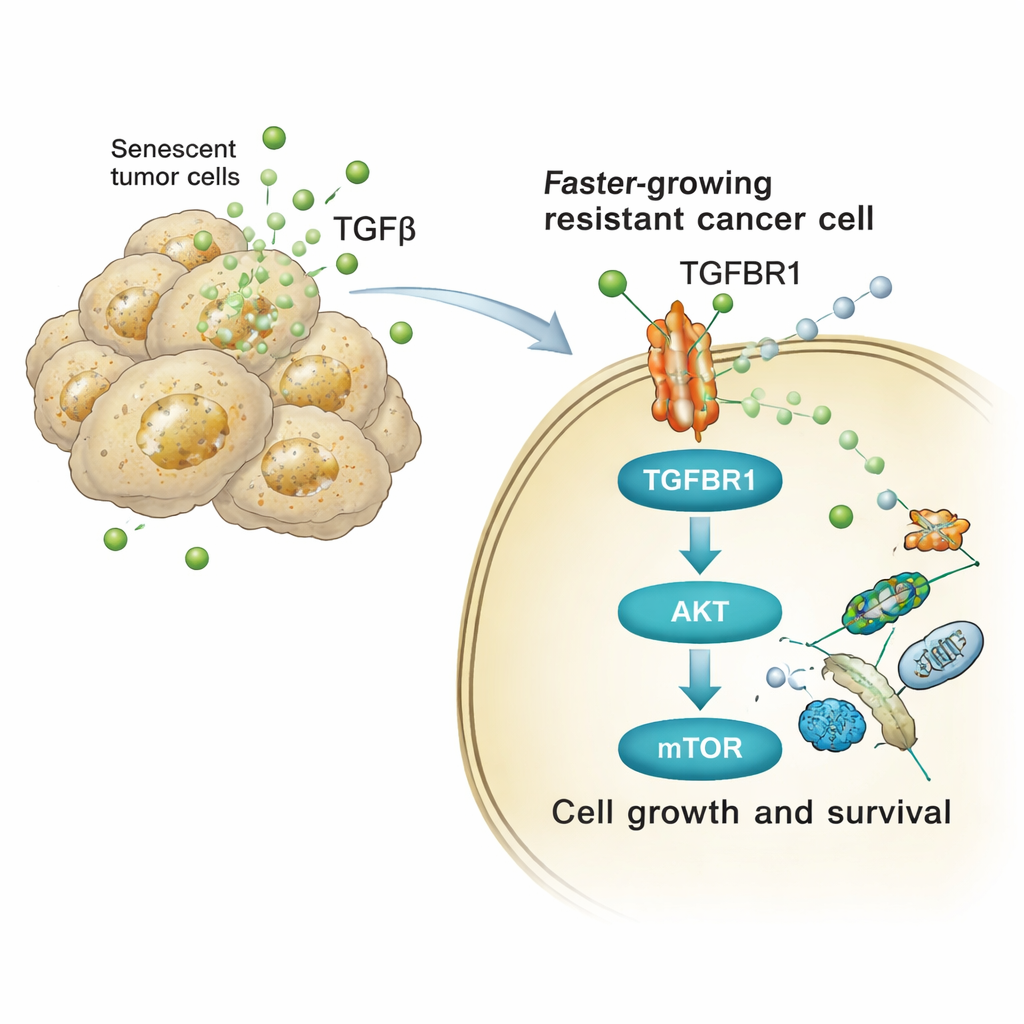
Farelerden Hastalara: Ortak Bir Zayıf Nokta
Bu mekanizmalar yalnızca petri kaplarında sınırlı kalmadı. Akciğer tümörü taşıyan farelerde senescent ve senescent olmayan kanser hücrelerinin karıştırılması daha hızlı büyüyen tümörlere ve daha kısa sağkalıma yol açarken, senescent hücrelerin ortadan kaldırılması veya TGFBR1’in bloke edilmesi bu etkiyi azalttı. Genetik olarak düzenlenmiş akciğer kanserleri olan farelere standart sisplatin verildiğinde, tümörlerde komşu hâlâ bölünen hücrelerde yüksek AKT/mTOR aktivitesi ile birlikte senesens işaretçileri birikti. Sisplatinin TGFBR1 inhibitörü veya senolitik ilaçlarla (seçici olarak senescent hücreleri öldüren) kombinasyonu, sadece kemoterapiye göre tümör yükünü azalttı ve sağkalımı uzattı. Kritik olarak, platin bazlı tedavi sonrası alınmış insan akciğer ve yüksek dereceli seröz over kanseri örneklerinin analizleri benzer desenleri ortaya koydu: özellikle senescent hücrelerin yoğun olduğu bölgelerde artmış senesens işaretçileri ve yükselmiş AKT/mTOR sinyalleşmesi görüldü.
Bir Zayıflığı Avantaja Çevirmek
Herkes için çıkarılacak ana mesaj şudur: platin kemoterapisi geride hasar görmüş ama tehlikeli bir “zombi” hücre nüfusu bırakabilir. Bu senescent tümör hücreleri artık kendileri bölünmese de çevreye TGFβ açısından zengin sinyaller pompalayarak yakındaki kanser hücrelerini uyandırır, tümörlerin yeniden büyümesine ve tedaviye direnç kazanmasına yardım eder. Ümit verici haber ise bu zayıflığın hedeflenebilir olmasıdır. Preklinik akciğer ve over kanseri modellerinde, TGFβ reseptörü TGFBR1’i bloke eden veya senescent hücreleri seçici olarak temizleyen ilaçların eklenmesi platin kemoterapisinin etkinliğini artırdı ve belirgin ek toksisite olmaksızın sağkalımı iyileştirdi. Bu çalışma, standart platin tedavisini senolitik veya anti-TGFβ stratejilerle birleştiren klinik denemelere doğru bir yol gösteriyor; amaç kemoterapinin faydalarını korurken onun gizli, senesens kaynaklı yan etkilerini etkisiz hale getirmektir.
Atıf: González-Gualda, E., Reinius, M.A.V., Macias, D. et al. Treatment resistance to platinum-based chemotherapy in lung and ovarian cancer is driven by a targetable TGFβ senescent secretome. Nat Aging 6, 368–392 (2026). https://doi.org/10.1038/s43587-025-01054-2
Anahtar kelimeler: kemoterapi direnci, hücresel senesens, TGFβ sinyalleşmesi, akciğer kanseri, over kanseri