Clear Sky Science · tr
Senotoksinler, lipid bağlanma özgüllüğü, iyon dengesizliği ve lipidom yeniden düzenlenmesi aracılığıyla senişans hedef alıyor
“Zombi” hücreleri öldürmenin kanser tedavisini neden keskinleştirebileceği
Yaşlandıkça—veya kemoterapi gibi ağır tedavilere maruz kaldığımızda—bazı hücreler bölünmeyi bırakır ama ölmek istemez. Bu “zombi” hücreler, senescent hücreler olarak bilinir, dokuya zarar verebilen ve tümörlerin yeniden ortaya çıkmasına yardımcı olabilecek iltihaplı moleküller salarlar. Bu çalışma, bir zehir kaynaklı protein kullanarak bu sorunlu hücreleri seçici şekilde ortadan kaldırmanın şaşırtıcı yeni bir yolunu araştırıyor; bu, kanser tedavilerini hem daha güçlü hem de daha güvenli hale getirebilir.
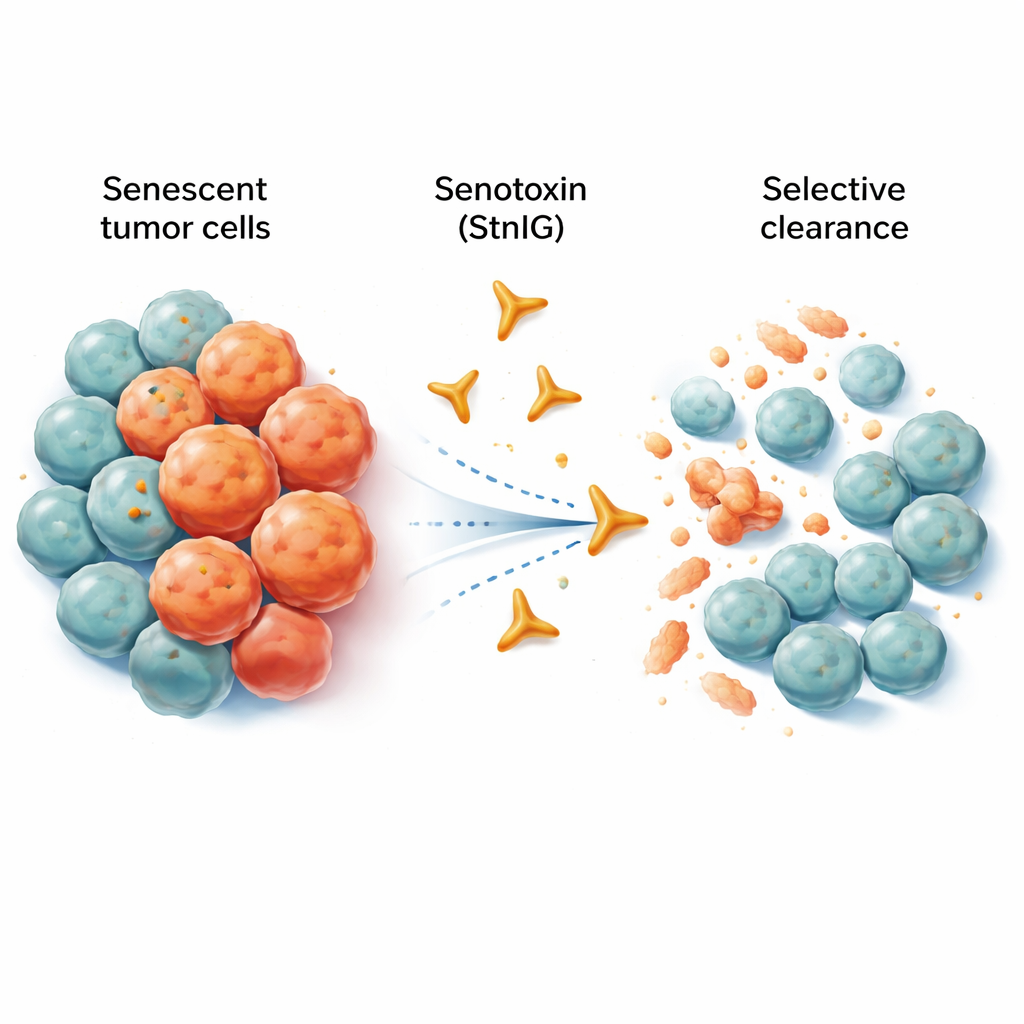
Vazgeçmeyen yaşlı hücreler
Senescent hücreler, hâlâ masalarını işgal eden ve ofisi bozan emekli çalışanlara benzer. Artık çoğalmazlar, ancak yakın dokuyu zayıflatabilecek, yaşlanmayı teşvik edebilecek ve hatta tümör büyümesi ile yayılımını destekleyebilecek bir dizi iltihaplı sinyal salarlar. Kemoterapi, birçok kanser hücresini öldürürken, genellikle tümörün içinde ve etrafında bir dizi senescent hücre bırakır. Bu kalan hücreler kronik iltihabı, yan etkileri ve nihayetinde nüksü körükleyebilir. Deneysel olarak geliştirilen senolitikler bu hücreleri ortadan kaldırmayı hedefliyor, ancak birçoğu ya sağlıklı hücrelere de zarar veriyor, çok dar doz aralığında etkili oluyor ya da vücut tarafından zor emiliyor.
Deniz anemonu zehrini hassas bir araca dönüştürmek
Araştırmacılar doğanın hücre öldürme uzmanlarına, yani hayvan zehirlerine yöneldiler. Karayip deniz anemonunda bulunan gözenek oluşturan bir protein olan sticholysin I (StnI) üzerinde yoğunlaştılar. Bu protein hücre zarlarında küçük delikler açabiliyor. Ekip, StnI ve mühendislik yapılarak geliştirilen StnIG adlı rafine versiyonunun, komşu aktif hücrelere göre senescent kanser hücrelerini öldürmede dikkat çekici derecede daha iyi olduğunu keşfetti. Kemoterapi ilaçlarıyla senesense sokulan çeşitli insan kanser hücre tiplerinde (melanom, karaciğer, akciğer ve sinir kaynaklı tümörler) StnI ve özellikle StnIG, aktif olarak büyüyen hücreleri etkilemek için gereken dozlardan çok daha düşük dozlarda yaşlanmış hücreleri yok etti. StnIG, önde gelen deneysel bir senolitik olan navitoclax’dan daha seçiciydi; bu da dikkatle ayarlanmış toksinlerin mevcut yaklaşımları geride bırakabileceğini gösteriyor.
Değişmiş hücre zarlarının nasıl bir talihsiz nokta haline geldiği
Senescent hücreler sadece iç yapılarını değiştirmez; her hücreyi saran yağlı deri olan dış zarları da yeniden düzenlenir. Sağlıklı hücrelerde belirli lipitler ağırlıklı olarak zarın iç tarafında yer alır, dış dünyadan gizlidir. Senescent hücrelerde bu denge bozulur ve bu lipitler açığa çıkar. Ayrıntılı kimyasal analizler ve bilgisayar simülasyonları kullanarak ekip, StnIG’nin bu değişmiş lipid manzarasını tanıdığını ve ona yapıştığını gösterdi. Yapısı, senescent hücrelerin yüzeyinde açığa çıkan belirli lipitlere özellikle iyi tutunacak şekilde uygundu. Bir kez bağlandığında, StnIG iyonların dengesiz akışına izin veren gözenekler oluşturdu.
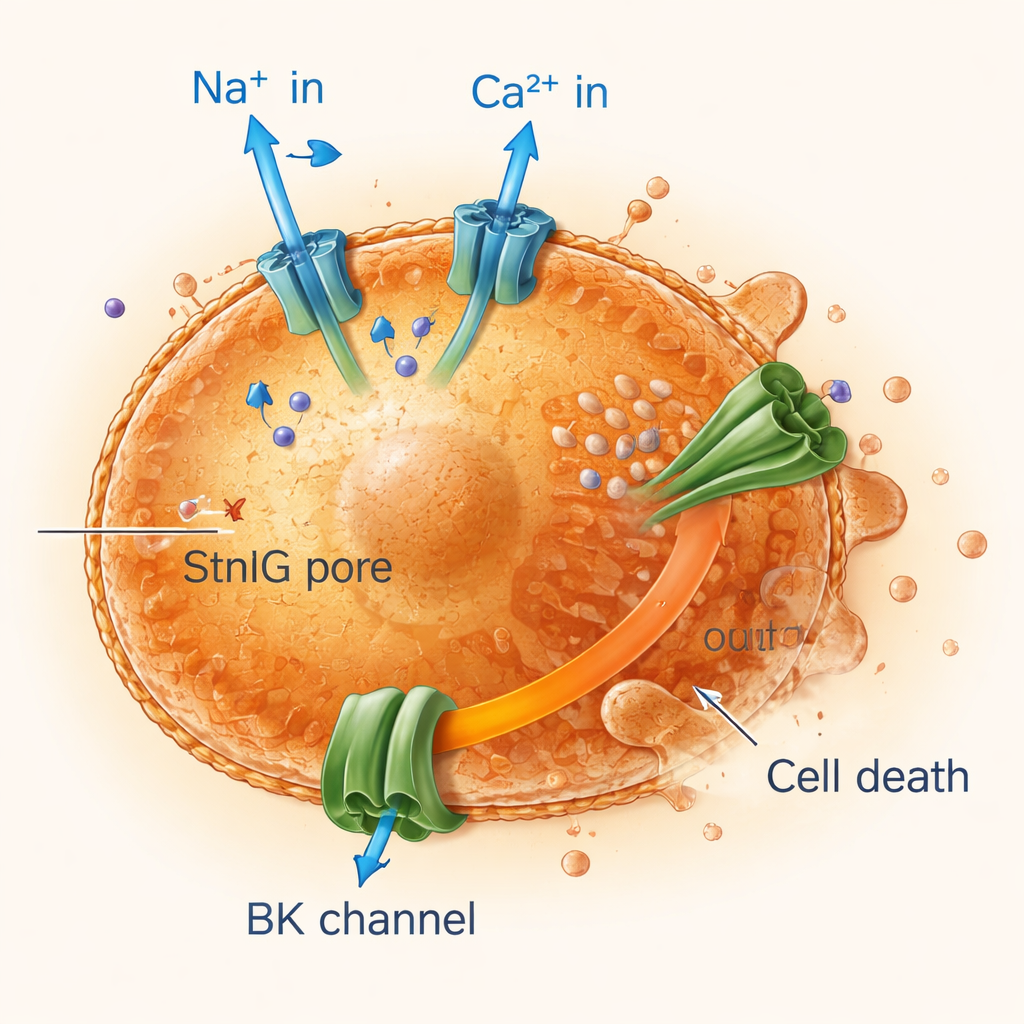
İyon dengesizliğiyle yaşlanan hücrelerin elektriklerini kestirmek
Hücre zarları boyunca elektrik ve iyon hareketini izleyerek araştırmacılar, StnIG gözeneklerinin sodyum ve kalsiyum iyonlarının senescent hücrelere hızla girmesine izin verirken potasyumun sürekli sızmasına yol açtığını buldular. Kalsiyum dalgalanması büyük potasyum kanallarını açıyor ve potasyum kaybını artırıyordu; potasyum hücre hacmini ve hayatta kalmasını korumak için çok önemlidir. Senescent hücreler, zaten sağlıklı hücrelere göre daha az esnek ve daha kırılgan olduklarından bu süregelen iyon bozukluğuyla başa çıkamıyorlar. Mitokondrileri—hücresel enerji santralleri—elektriksel yüklerini kaybediyor, enerji üretimi düşüyor ve hücreler programlı ölüm biçimleri olan apoptoz ile iltihaplı bir ölüm türü olan piroptozis dahil ölüm yollarına giriyor. Kalsiyum girişini veya potasyum kanallarını engellemek senescent hücreleri korudu; bu da iyon bozukluğunun toksinin etkisinin merkezinde olduğunu doğruluyor.
Hücre kültürlerinden canlı hayvanlara
Ekip sonra bu stratejinin canlı organizmalarda işe yarayıp yaramadığını test etti. İnsan senescent melanom hücreleri taşıyan zebrafish embriyolarında düşük doz StnIG, navitoclax kadar etkili bir şekilde bu hücrelerin sayısını azalttı ve belirgin bir toksisite gözlenmedi. Melanom ve karaciğer kanseri fare modellerinde, hücre döngüsü ilacı palbociklib ile yapılan kemoterapi birçok kanser hücresini senesense sokarak tümör büyümesini yavaşlattı. Araştırmacılar aralıklı olarak StnIG eklediklerinde, tümörler kemoterapi tek başına veya kemoterapi–navitoclax kombinasyonuna kıyasla daha etkili şekilde küçüldü veya remisyonda girdi. Önemli olarak, StnIG ile tedavi edilen farelerde sınırlı yan etki ve ana organlarda belirgin bir hasar gözlenmedi; ancak senescent tümörlere sahip hayvanlarda kan potasyumu yükseldi—bu muhtemelen tümör hücreleri yok edilirken büyük miktarda potasyum salınımını yansıtıyor.
Geleceğin kanser bakımına etkisi
Bu çalışma “senotoksinler”i tanıtıyor: mühendislik yapılmış, zehir ilhamlı proteinler; bunlar senescent hücrelerin benzersiz zar ve iyon yönetimi tuhaflıklarından yararlanıyor. Değişmiş lipitleri hedefleyip ölümcül iyon dengesizlikleri yaratarak, StnIG zararlı senescent hücreleri seçici olarak temizleyebilir ve çoğu sağlıklı dokuyu koruyabilir. Kemoterapi ile birlikte kullanıldıklarında, bu tür senotoksinler bir gün nüksü ve kronik iltihabı körükleyen zombi hücreleri ortadan kaldırmaya yardımcı olabilir, kanser tedavilerini daha dayanıklı kılabilir ve bazı uzun vadeli yan etkileri hafifletebilir.
Atıf: Moral-Sanz, J., Fernández-Carrasco, I., Ramponi, V. et al. Senotoxins target senescence via lipid binding specificity, ion imbalance and lipidome remodeling. Nat Aging 6, 349–367 (2026). https://doi.org/10.1038/s43587-025-01030-w
Anahtar kelimeler: hücresel senesans, senolitikler, kanser tedavisi, zehir kaynaklı ilaçlar, iyon kanalları