Clear Sky Science · tr
İskelet kası farklılaşması boyunca metabolik geçişleri PFKM yönetir
Kas hücrelerinin akıllı şeker kullanmasına neden ihtiyaç var
Egzersiz yaptığımızda veya sadece sandalyeden kalktığımızda, iskelet kaslarımız harekete geçer ve her kasılmayı güçlendirmek için şekeri yakar. Ancak genç kas kök hücreleri ile tam oluşmuş kas lifleri şekeri aynı şekilde işlemez. Bu çalışma, glukozun hemen enerji için yakılıp yakılmayacağına ya da hücreleri koruyup onarmak için yönlendirileceğine karar veren, tek bir enzim olan PFKM etrafında toplanan yerleşik bir anahtarlama sistemi ortaya koyuyor. Bu anahtarı anlamak, kas zayıflığı, yaşlanan kaslar ve kalıtsal metabolik hastalıkların tedavisi için yeni yollar açabilir.
Hücresel yakıt için bir trafik ışığı
Hücreye giren glukoz birkaç yoldan birini izleyebilir. Bir ana yol olan glikoliz, şekeri hızla enerjiye ve büyüyen kas lifleri için yapı taşlarına dönüştürür. Diğer bir yol olan pentoz fosfat yolu ise hücreleri oksidatif strese karşı koruyan moleküller üretir ve DNA ile lipid sentezini destekler. Araştırmacılar, glikolizin kilit bir ayrım noktasında duran fosfofruktokinaz-1 enziminin bir formu olan PFKM’e odaklandı. Wnt adlı bir büyüme sinyalini aktive ettikten sonra dakikalar ile saatler içinde yüzlerce metaboliti ölçerek, hücrelerin erken glikoliz ara ürünlerini hızla biriktirirken PFKM ürününün azaldığını ve pentoz fosfat yolu metabolitlerinin arttığını buldular. Bu, hücrelerin PFKM’i aktif olarak kısıtlayıp şekeri saf enerji üretimi yerine koruyucu kimyaya yönlendirdiğini düşündürdü. 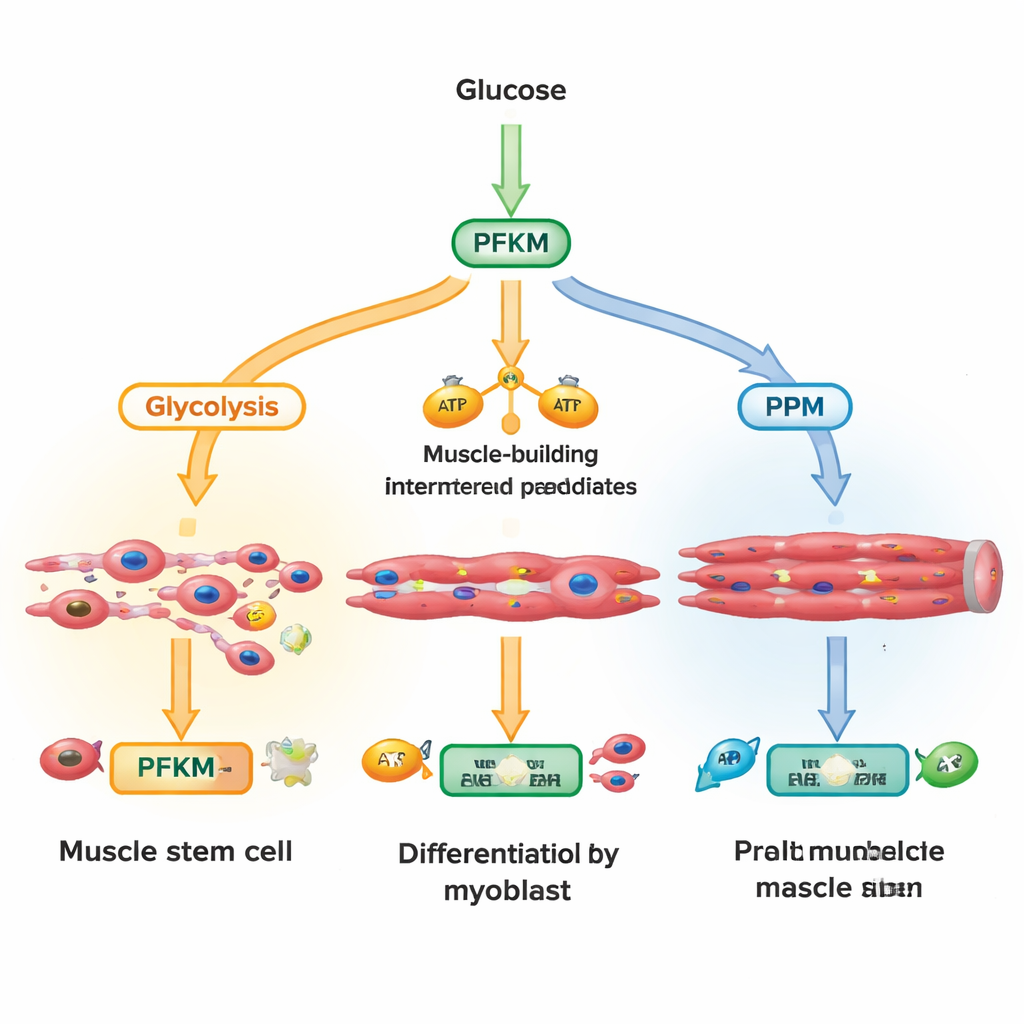
Kapı bekçisi enzimin etiketlenmesi ve uzaklaştırılması
PFKM’in nasıl kontrol edildiğini görmek için ekip proteinin hücre içindeki yerini izledi. Dinlenme koşullarında PFKM sitoplazma boyunca dağınık haldeydi. Wnt uyarısından dakikalar içinde parlak noktalara toplanarak hücrenin protein öğütme bölmeleri olan lizozomlarla örtüştü. İki kardeş enzim olan PFKL ve PFKP ne hareket etti ne de seviyelerinde değişiklik oldu; bu da sadece kas tipi PFKM’nin hedeflendiğini gösterdi. Biyokimyasal testler, lizozom fonksiyonunu engellemenin PFKM kaybını önlediğini, diğer ana protein imha sistemi olan proteazomun inhibisyonunun ise etkisi olmadığını gösterdi. Dizi analizi, PFKM’e özgü kısa bir “metil arginin degron” motifini ortaya çıkardı. PRMT1 enzimi bu motif içindeki bir argininde spesifik bir metil işareti ekledi ve bu etiket, VPS4 dahil olmak üzere mikrootofaji makinesinin PFKM’i lizozomlara çekip yıkmasına izin verdi. PRMT1 veya VPS4 devre dışı bırakıldığında PFKM stabil kaldı ve uzaklaştırılması engellendi.
Kök hücreden çalışan kas lifine
Büyük insan tek hücre veri setlerini kullanarak yazarlar PFKM seviyelerini birçok kas hücresi tipinde haritaladılar. Onarım için gerektiğinde uykuda kalan kas kök hücreleri çok az PFKM’ye sahipken, pentoz fosfat yolu genleri ve lizozomal bileşenleri yüksek düzeyde ifade ediyordu. Hücreler kas olmaya karar verip çok çekirdekli liflere füzyon yaptıkça PFKM transkriptleri ve proteini hızla arttı, Wnt hedefleri ve lizozomal genler azaldı. Kültürdeki insan ve fare kas hücrelerinde Wnt, erken tek çekirdekli hücrelerde PFKM’i hızla lizozomlara yönlendirirken olgun çok çekirdekli liflerde bunu yapmadı. Bu desen, farklılaşmamış hücrelerin koruyucu metabolizmayı desteklemek için PFKM’i lizozomal degradasyon yoluyla düşük tuttuğu, sonra enerji ihtiyacı yüksek kas liflerine dönüşürken tekrar PFKM’i yeniden ifade ettikleri bir modeli destekliyor.
Anahtar takılı kaldığında ne olur
PFKM’in kas inşası için ne kadar hayati olduğunu test etmek üzere ekip RNA enterferansı ile seviyesini düşürdü. Düşük PFKM’li hücreler karakteristik kas genlerini açmakta zorlandı, daha az miyozin proteini üretti ve hücre sayısı genel olarak değişmemesine rağmen daha az ve daha küçük çok çekirdekli lifler oluşturdu. Metabolit profillemesi, aşağı yöndeki glikoliz ara ürünleri ve trikarboksilik asit döngüsü yakıtlarının azaldığını, buna karşılık pentoz fosfat genleri ve işaretleyicilerinin arttığını ve oksidatif strese karşı direncin yükseldiğini gösterdi. Önemli olarak, hücrelere PFKM’in normalde altında yer alan bir glikoliz ara ürünü olan 3‑fosfogliserat verildiğinde birçok farklılaşma kusuru düzeltti. Kas belirteçleri ve lif oluşumu geri döndü; bu da asıl darboğazın PFKM proteininin yokluğu değil, eksik metabolitler olduğunu gösterdi. 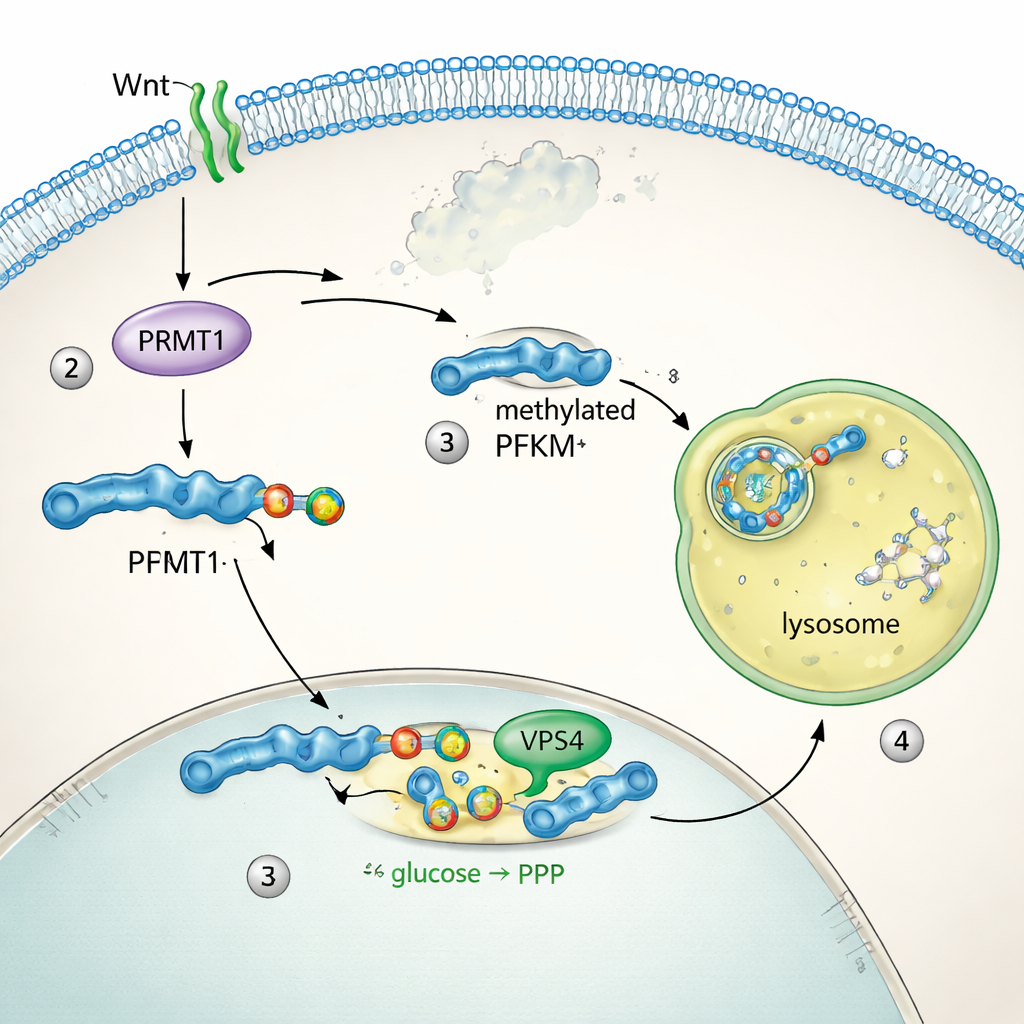
Kas sağlığı ve onarımı için çıkarımlar
Uzman olmayan bir okuyucu için merkezi mesaj şudur: kas hücreleri şekeri sadece “daha fazla veya daha az yakmaz”; yaşam evrelerine bağlı olarak onu enerji üretimi ile hücre koruması arasında dikkatle yeniden yönlendirirler. PFKM bu ayrım noktasında ayarlanabilir bir vana gibi davranır. Kök hücreye benzer hücrelerde Wnt kaynaklı etiketleme ve lizozomal yıkım PFKM’i ortadan kaldırarak glukozu hücreleri koruyan ve gelecekteki büyümeye hazırlayan bir yola yönlendirir. Hücreler çalışan liflere olgunlaştıkça PFKM depolarını yeniden kurar ve metabolizmayı yüksek verimli enerji kullanımına çevirirler. Bu dengenin bozulması, nadir görülen PFKM eksikliği hastalıklarında görüldüğü gibi, normal kas gelişimini aksatır. Bu anahtarın moleküler mekanizmasını ortaya koymak, gelecekteki tedavilerin PFKM aktivitesini hafifçe ayarlayarak veya uygun aşağı akış metabolitlerini sağlayarak kas rejenerasyonunu iyileştirebileceğini ya da hastalık ve yaşlanma durumlarında kasları koruyabileceğini düşündürüyor.
Atıf: Campos, M., Nguyen, S.T., Kong, X. et al. PFKM governs metabolic shifts throughout skeletal muscle differentiation. Nat Metab 8, 489–505 (2026). https://doi.org/10.1038/s42255-026-01457-4
Anahtar kelimeler: iskelet kası farklılaşması, glikoz metabolizması, PFKM enzimi, pentoz fosfat yolu, lizozomal protein degradasyonu