Clear Sky Science · tr
Cytosolik DHODH’nin dışarıdan ifade edilmesi de novo pirimidin biyosentezini mitokondriyal elektron taşıma zincirinden ayırır
Hücrelerimizdeki gizli bağın kırılmasının önemi
Vücudunuzdaki her hücre DNA’sını sürekli kopyalamak ve onarmak zorundadır; bu süreç pirimidin adı verilen kimyasal “harflerin” sürekli tedarikini gerektirir. Çoğu hayvanda bu harflerin üretilmesi, mitokondrilerin—hücrenin enerji santrallerinin—oksijen kullanarak yakıt yakma biçimiyle sıkı bir şekilde bağlıdır. Bu bağ, mitokondriyal solunum aksadığında DNA yapıtaşlarının tükenmesine ve hücrelerin büyümekte zorlanmasına yol açar. Burada özetlenen çalışma, mayadan alınan tek bir genin bu iki süreci temiz bir şekilde ayırabileceğini gösteriyor. Bu genetik değişiklik, memeli hücrelerinin mitokondrileri bozuk olsa bile DNA harflerini üretmeye devam etmesini sağlıyor; bu da bozuk enerji metabolizmasından kaynaklanan hastalıkları araştırmak ve belki bir gün tedavi etmek için yeni bir yol açıyor.
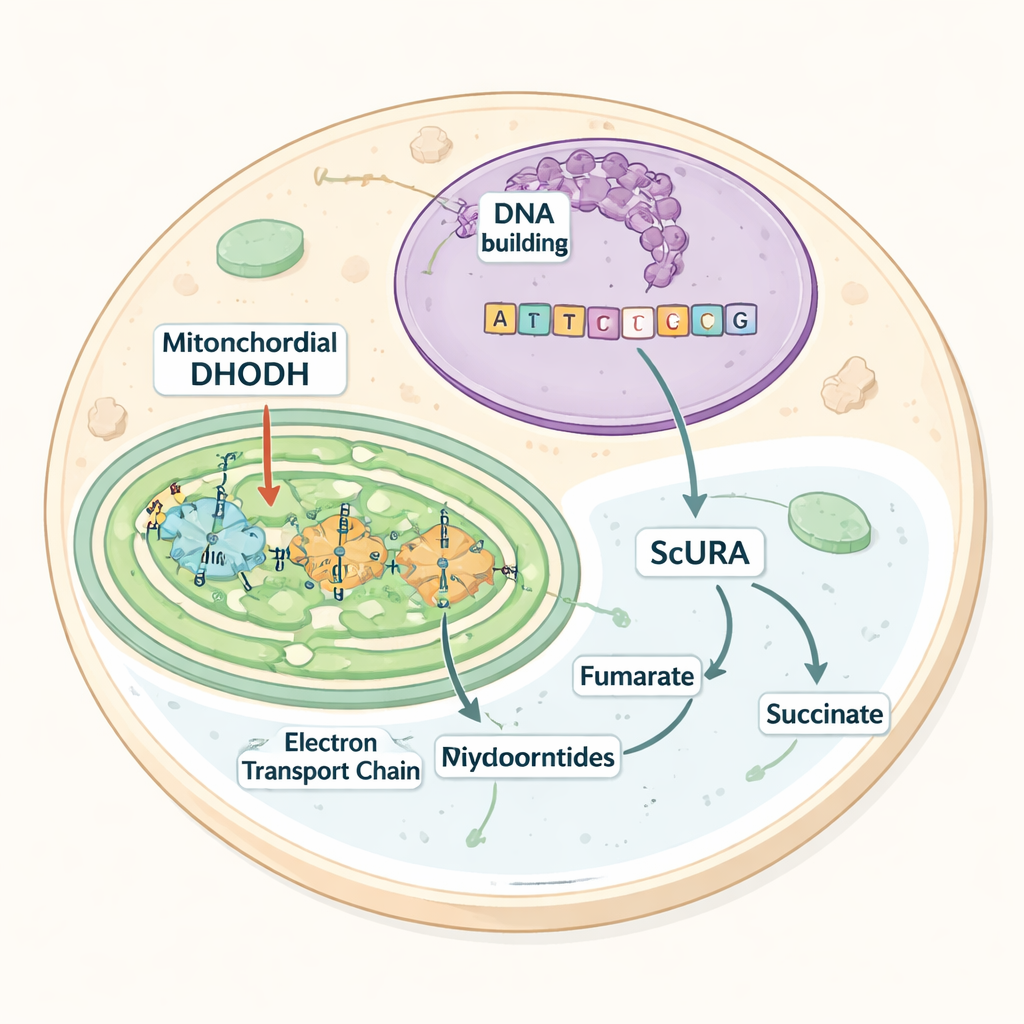
Mayadan ödünç alınmış bir araç
Çalışma, pirimidin inşasında anahtar bir adımı gerçekleştiren dihidroorotat dehidrogenaz (DHODH) adlı enzime odaklanıyor. Memelilerde DHODH, mitokondrinin iç zarında yer alır ve elektronları solunum zincirini besleyen bir taşıyıcıya verir. Bu elektron akışı engellenirse—örneğin ilaç inhibitörleri veya genetik kusurlar nedeniyle—DHODH durur, pirimidin üretimi kesilir ve hücreler hazır uridin gereksinimine bağımlı hale gelir. Oksijensiz yaşayan birçok mikroorganizma, hücre sıvısında yüzen ve farklı elektron kabul ediciler kullanan alternatif DHODH versiyonlarıyla bu darboğazdan kaçınır. Yazarlar, memeli hücrelerine böyle oksijenden bağımsız bir yol koyup koyamayacaklarını sordular.
DNA harflerinin nasıl yeniden yönlendirildiği
Araştırmacılar, maya Saccharomyces cerevisiae’den URA1 genini insan hücrelerine tanıttılar. URA1, ScURA adı verilen sitozolik bir enzim kodlar; bu enzim mitokondriyal DHODH ile aynı kimyasal adımı gerçekleştirir ama elektronları mitokondriyal taşıyıcı yerine fumarata verir. Biyokimyasal testler ScURA’nın sitozolde aktif dimerler oluşturduğunu ve yeni, ilaçlara dirençli bir DHODH aktivitesi eklediğini gösterdi. Normal koşullar altında ScURA eklenmesi mitokondri yapısını, solunumu veya büyümeyi bozmadı; bu da ScURA’nın ekstra bir yükten ziyade bir yedek yol olarak davrandığını gösteriyor.
Mitokondri engellerini umursamayan hücreler
Bu yedeğin yerli sistemi ikame edip edemeyeceğini görmek için ekip, DHODH’nin kendisini veya mitokondriyal elektron taşıma zincirini kimyasal olarak bloke etti; bu işlemler normalde uridin sağlanmadıkça hücre bölünmesini durdurur. ScURA eksprese eden hücreler, güçlü kompleks III inhibisyonu altında veya endojen DHODH geninin genetik silinmesinin ardından bile yardım almadan çoğalmaya devam etti. İşaretli glutaminden gelen azot ve karbon atomlarının ayrıntılı izlenmesi, ScURA-eksprese eden hücrelerin bu tıkanmalara rağmen pirimidin nükleotidlerini üretmeye devam ettiğini gösterdi. Metabolit ölçümleri, toksik öncüllerin birikmesi yerine ScURA hücrelerinin elektronları fumarata aktardığını, sukkinat ürettiklerini ve sitozol ile mitokondri arasında fumarat–sukkinat taşıma işlevini destekleyecek şekilde trikarboksilik asit (TCA) döngüsünü ince bir şekilde yeniden şekillendirdiklerini ortaya koydu.
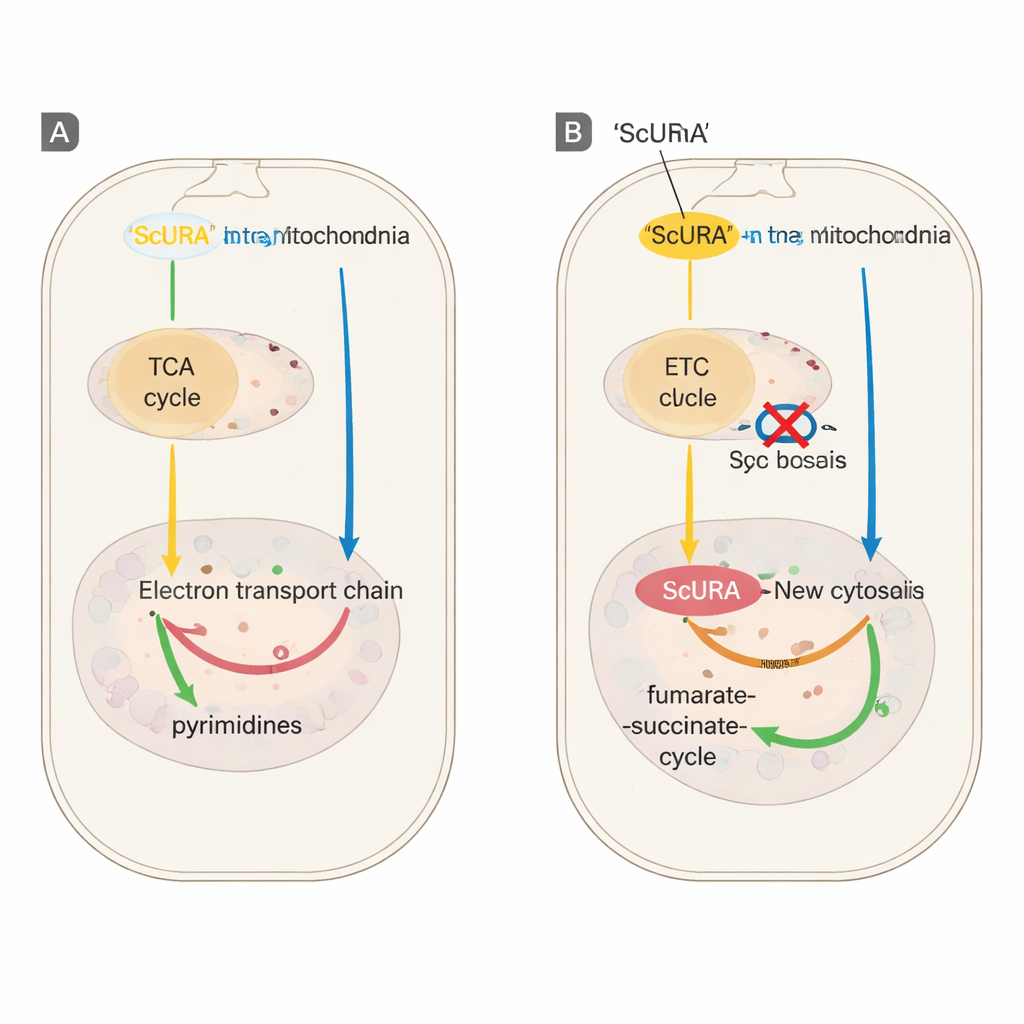
Hasarlı enerji santrallerine sahip hücrelerin kurtarılması
Yazarlar daha sonra ScURA’yı mitokondriyal hastalık hücre modellerinde test ettiler. Mitokondriyal DNA’dan yoksun hücreler veya solunum kompleksleri III veya IV’ü sakatlayan mutasyonlar taşıyan hücreler normalde büyümek için eklenmiş uridine bağımlıdır. ScURA eksprese edecek şekilde mühendislik yapıldıktan sonra, bu çeşitli mutant hücreler uridine olmadan çoğalabildi; ancak hala bir miktar mitokondriyal aktivite ihtiyacını yansıtan pirüvata ihtiyaç duymaya devam ettiler. Gen ifade düzeyinde ScURA, kronik elektron taşıma inhibisyonunu takiben genellikle kapanan ribozomal protein genlerinin kapatılmasını da önledi; bu, RNA üretimini sürdürecek kadar yüksek pirimidin yapıtaşı arzını koruyarak gerçekleşti.
Sağlık ve hastalık için anlamı
Pirimidin sentezini mitokondriyal solunumdan temiz bir şekilde ayırarak ScURA araştırmacılara güçlü bir yeni kaldıraç sunuyor: şimdi pek çok durumda, belirli bir kusurun veya ilacın etkisinin gerçekten enerji üretimindeki kayıptan mı yoksa DNA ve RNA öncüllerinin eksikliğinden mi kaynaklandığını sorgulayabilirler. Uzun vadede benzer stratejiler, mitokondriyal bozukluklar için mevcut gen terapilerine tamamlayıcı olabilir veya bazı tümörlerin neden mitokondriyal fonksiyonlarını geri kazanma konusunda bu kadar bağımlı olduğunu açıklamaya yardımcı olabilir. Bir maya enzimini insan tedavisine aktarmak büyük özen gerektirse de, bu çalışma tek, dikkatle seçilmiş bir genin evrim boyunca iç içe tutulan temel bir metabolik bağlantıyı yeniden yazabileceğini gösteriyor.
Atıf: Curtabbi, A., Jaroszewicz, S.N., Sanz-Cortés, R. et al. Ectopic expression of cytosolic DHODH uncouples de novo pyrimidine biosynthesis from mitochondrial electron transport. Nat Metab 8, 454–466 (2026). https://doi.org/10.1038/s42255-026-01454-7
Anahtar kelimeler: pirimidin metabolizması, mitokondriyal işlev, elektron taşıma zinciri, metabolik yeniden kablolama, mitokondriyal hastalık