Clear Sky Science · tr
Farklı küresel popülasyonlarda ve hastalıkla ilişkili dokularda tip 2 diyabete neden olan moleküler mekanizmaların çözümlenmesi
Diyabetin kökenlerini anlamak neden önemli
Tip 2 diyabet dünya genelinde yüz milyonlarca insanı etkiliyor, ancak vücutta hastalığa gerçekten neden olan moleküler anahtarların hangileri olduğu mı yoksa sadece eşlik eden değişiklikler mi olduğu konusunda hâlâ şaşırtıcı derecede az şey biliyoruz. Bu çalışma, kan şekerini diyabete sürükleyen veya onu koruyan genleri ve proteinleri belirlemek için DNA’mıza ve birden fazla organa derinlemesine bakıyor. Araştırmacılar, farklı kökenlerden gelen insanları dahil ederek ve birkaç kilit dokuyu inceleyerek, yalnızca Avrupa kökenli kişiler için değil, birçok popülasyon için işe yarayabilecek daha hassas koruma stratejilerine ve tedavilere doğru ilerlememizi sağlıyor.
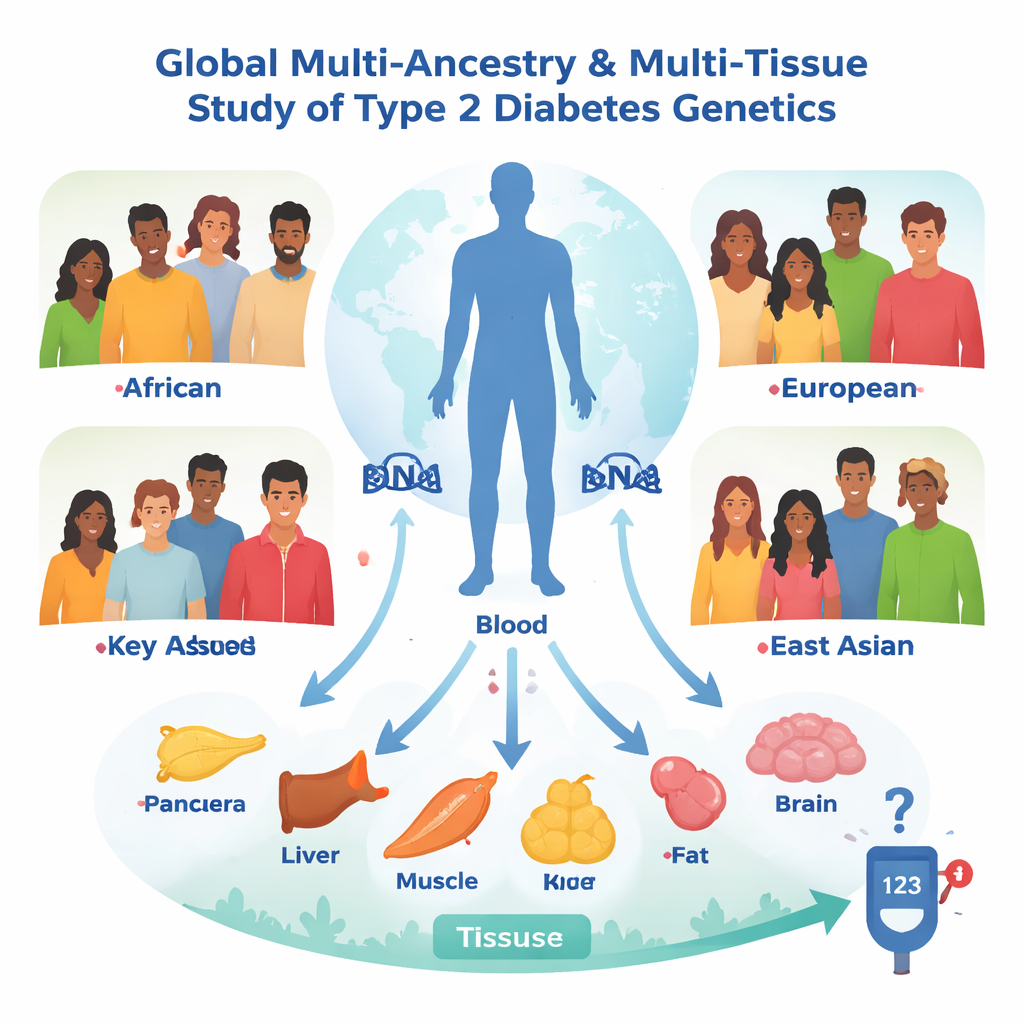
Dünya çapına ve vücudun içine bakmak
Çalışma ekibi, Tip 2 Diyabet Küresel Genomik Girişimi tarafından toplanan 2,5 milyondan fazla kişinin genetik verileriyle başladı. Sadece hangi DNA varyantlarının diyabetle ilişkili olduğunu sormak yerine daha güçlü bir soru sordular: Hangi varyantlar belirli genlerin veya proteinlerin etkinliğini değiştiriyor ve bu değişiklikler sırayla diyabet riskini gerçekten etkiliyor mu? Bunu yapmak için, doğal olarak ortaya çıkan genetik farklılıkları yerleşik bir randomize deneme gibi ele alan Mendelyen randomizasyonu adı verilen istatistiksel bir yaklaşım kullandılar. Avrupa, Afrika, melez Amerikan ve Doğu Asya olmak üzere dört köken grubundaki kişilerde 20.000’den fazla gen aktivite ölçümü ve 1.600’den fazla kan proteini analiz ettiler; ardından pankreas, insülin üreten adacıklar, karaciğer, kas ve farklı yağ depoları dahil olmak üzere kan şekeri kontrolünde merkezi rol oynayan yedi dokuda analizleri tekrarladılar.
Risk artıran veya azaltan moleküler kaldıraçları bulmak
Bu genetik yolları izleyerek, araştırmacılar genetik olarak öngörülen seviyelerinin tip 2 diyabet riski üzerinde nedensel etkisi olan 335 gen ve 46 kan proteini belirledi ve bu bulguların birçoğunu bağımsız kohortlarda doğruladılar. Buldukları moleküler kaldıraçlardan bazıları, pankreatik adacık hücrelerinden insülin salınımında rol oynayan MTNR1B gibi zaten bilinen şüpheliler veya pankreasta ve yağda hücre ölümünü etkileyen BAK1 gibi genlerdi. Diğerleri daha yeni veya daha az dikkate alınmış oyunculardı; örneğin yağ dokusu gelişimi ve insülin direnciyle ilişkilendirilen CPXM1 ve mitokondriyal işlevle ilişkili HIBCH gibi. Genel olarak, en az bir dokuda etkinlikleri değiştirildiğinde diyabet gelişme olasılığını etkileyebileceklerine dair kanıt bulunan 923 gen ve 46 proteini katalogladılar.
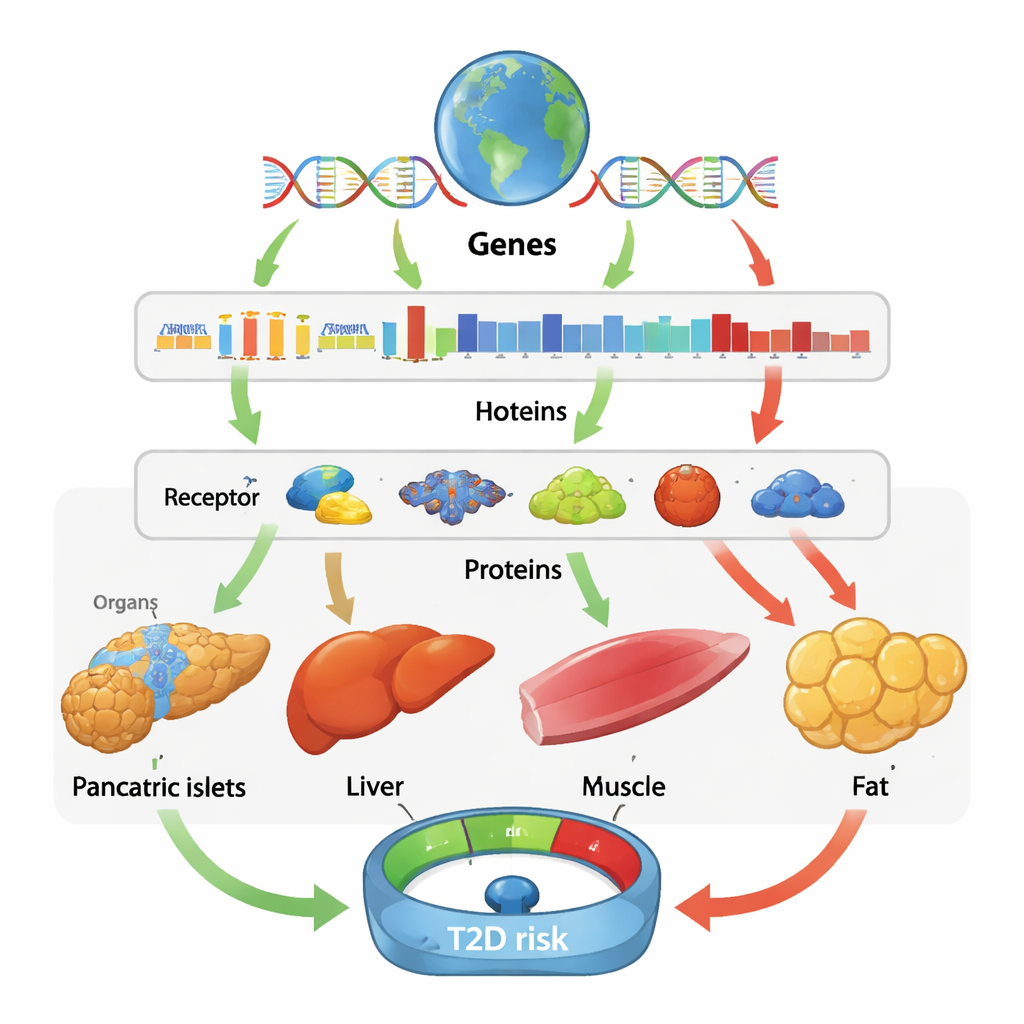
Aynı genler, dokular ve insanlar arasında farklı öyküler
Çarpıcı derslerden biri, bir genin etkisinin sıklıkla yüksek derecede doku-özgü olduğudur. Örneğin BAK1 aktivitesinin pankreas ve adacıklarda daha yüksek olması, muhtemelen insülin üreten hücrelerin kaybına katkıda bulunarak diyabet riskini artırırken; yağ ve kaslarda daha yüksek BAK1 düzeyleri koruyucu görünüyor. HIBCH de benzer şekilde karışık bir desen gösterdi: bazı dokularda daha fazla aktivite diyabet riskini düşürürken, diğerlerinde artırıyordu. Bu bulgular, yalnızca kana bakmanın organlar içinde gerçekleşen kritik biyolojiyi gözden kaçırabileceğini ve aynı molekülün bir dokuda yararlı, başka bir dokuda zararlı olabileceğini gösteriyor. Buna karşılık, ekip kökenler arasında sonuçları karşılaştırdığında, etki büyüklüklerinde nispeten az fark gördü; bu da birçok alttaki nedensel mekanizmanın küresel olarak paylaşıldığını, ancak Doğu Asya veya Afrika gruplarında belirli koruyucu veya risk proteinleri gibi bazı sinyallerin sadece Avrupalı olmayan veriler sayesinde tespit edilebildiğini düşündürüyor.
Yeni bulguları bilinen diyabet biyolojisine bağlamak
Yaklaşımlarının biyolojik açıdan anlamlı olup olmadığını kontrol etmek için yazarlar nedensel genlerini insan çalışmalarından ve fare deneylerinden derlenen diyabetle ilişkili gen listeleriyle karşılaştırdılar. Diyabette rol oynadığına dair daha güçlü ön kanıta sahip genlerin, rastgele seçilmiş genlere kıyasla analizlerinde nedensel etkiler gösterme olasılığı çok daha yüksekti. Dahası, bu nedensel etkilerin ortaya çıktığı dokular bilinen hastalık mekanizmalarıyla uyumlu çıktı: beta hücre yetmezliği ile ilişkili genler pankreatik adacıklarda en çok önem taşırken, metabolik sendromla bağlantılı genler en güçlü etkilerini visceral (derin karın) yağda gösteriyordu. Bu uyum, istatistiksel hattın sadece korelasyonları değil mekanizmaları hedeflediği fikrini destekliyor.
Gelecekteki tedavi ve önleme için bunun anlamı
Uzman olmayanlar için ana çıkarım şudur: Bu çalışma, uzun ve kişisel olmayan DNA varyant listelerini tip 2 diyabeti gerçekten yönlendiren belirli genler, proteinler ve organların daha net bir haritasına dönüştürüyor. Nedeni etkiden ayırarak ve aynı molekülün farklı dokularda zıt roller oynadığını ortaya koyarak ilaç geliştiricilere daha hassas hedefler veriyor ve tek tip bir tedavinin nerede ters tepebileceği konusunda uyarıyor. Önemli olarak, kasıtlı olarak farklı popülasyonları dahil ederek, bu içgörülerden yola çıkarak geliştirilecek gelecekteki ilaçların veya risk skorlarının sadece Avrupa kökenli insanlar için değil, daha geniş bir yelpazede etki etme şansını artırmasına yardımcı oluyor.
Atıf: Bocher, O., Arruda, A.L., Yoshiji, S. et al. Unravelling the molecular mechanisms causal to type 2 diabetes across global populations and disease-relevant tissues. Nat Metab 8, 506–520 (2026). https://doi.org/10.1038/s42255-025-01444-1
Anahtar kelimeler: tip 2 diyabet, genetik mekanizmalar, çok-kökenli genomik, doku-özgü gen ifadesi, nedensel çıkarım