Clear Sky Science · tr
Lamin A/C tarafından düzenlenen sistein katabolik akışı, epigenom yeniden programlaması yoluyla kök hücre kaderini değiştirir
Hücresel İskeletin Metabolizmayla Konuşması
Neden bazı hücreler genç ve hangi hücreye dönüşebilecekleri konusunda esnek kalırken, diğerleri yaşlanır veya yanlış kimliğe kilitlenir? Bu çalışma, DNA’yı şekillendiren nükleer “iskelet” ile sülfür içeren besin sistein arasında hücrelerimiz içinde şaşırtıcı bir konuşmayı ortaya koyuyor. Bu diyalogun kök hücreleri sağlıklı kaderlere—veya erken yaşlanmaya—nasıl yönlendirdiğini göstererek, hücrelerin “ne yediği” ve bunu nasıl işlediğinin belli genetik hastalıkları önlemek ve belki de yaşlanmanın bazı yönlerini yavaşlatmak için ayarlanabileceğini ima ediyor.
Nükleer Kabukun Gizli Rolü
Her hücrenin derininde DNA, nükleer lamina adı verilen ve kısmen lamin A ile C isimli proteinlerden oluşan bir protein ağına bastırılır. Bu laminler sadece çekirdeğe şekil vermekle kalmaz; ayrıca hangi genlerin kapatılacağına ve hangilerinin erişilebilir kalacağına karar verilmesine yardımcı olur. Yazarlar, fare embriyonik kök hücrelerini en esnek veya “naif” durumlarında incelediler ve lamin A/C’nin normalde sistein yapımında ve yıkımında rol alan iki metabolik enzim olan CBS ve CTH’yi kontrol altında tuttuğunu buldular. Lamin A/C mevcut ve aktif olduğunda, bu enzimler geri tutulur ve sistein işlenmesi düşük kalır; bu da kararlı, genç bir kök hücre durumunu destekler. 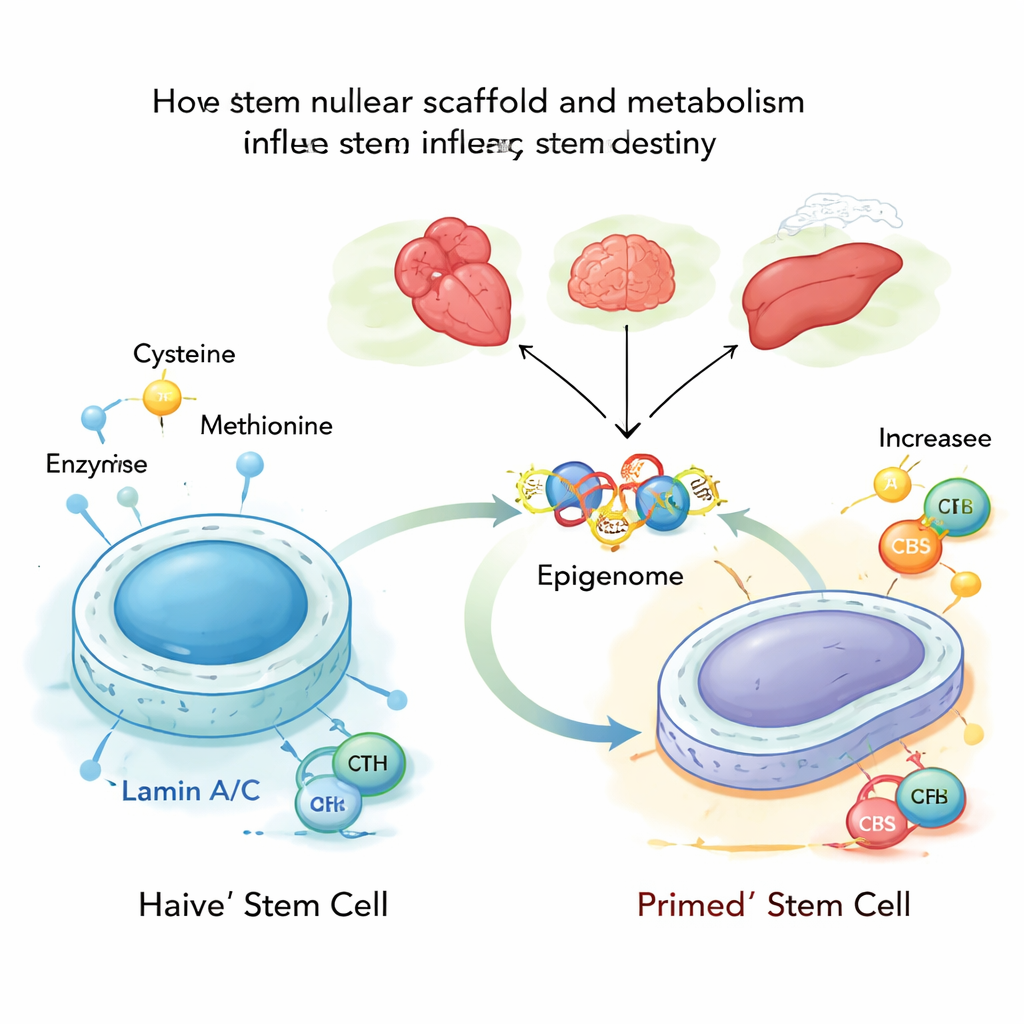
Yapı Bozulduğunda Metabolizma Hızlanır
Araştırmacılar daha sonra lamin A/C’yi kaldırdı veya Hutchinson–Gilford progeria olarak bilinen insan erken yaşlanma bozukluğunu taklit eden bir hastalık bağlantılı mutasyon tanıttı. Normal lamin A/C yoksa, CBS ve CTH genleri daha erişilebilir hale gelir ve SP1 adlı bir transkripsiyon faktörü tarafından daha güçlü bağlanırak etkinleşirler. Bu değişiklik, sisteinin asetil‑CoA ile sonuçlanan bir metabolik yola daha fazla yönlendirilmesine neden olur; asetil‑CoA, DNA paketlenmesini gevşetmek için kullanılan asetil gruplarını taşıyan küçük bir moleküldür. Sistein giderek daha fazla asetil‑CoA’ya kanalize oldukça, asetil grupları özellikle histon H3 üzerindeki K9 ve K27 olarak bilinen iki konuma öncelikli olarak eklenir ve böylece yakındaki genlerin açılması kolaylaşır.
Kimyasal İşaretlerden Hücre Kaderi Kararlarına
Histon “etiketlerindeki” bu kaymalar hücrenin kontrol panelinin küresel bir yeniden ayarlanması gibi davranır. Naif kök hücrelerde CBS ve CTH’yi artırmak veya basitçe daha fazla sistein sağlamak, hücreleri gerçek dokular oluşturmaya daha yakın, daha ileri bir “hazır” duruma iter. Kalp gelişimi ve diğer soylarla ilgili genler daha aktif hale gelir ve DNA’nın üç boyutlu katlanması bu programları destekleyecek şekilde değişir. Tersine, CBS ve CTH’yi azaltmak veya sisteini kısıtlamak, nükleer lamina hasarlı olsa bile daha naif, genç bir kimliğin yeniden sağlanmasına yardımcı olur. Embriyonik modellerde, bu metabolik yanlış bağlantı üç germ katmanının—tüm organların erken yapı taşlarının—dengesiz oluşumuna ve CBS ile CTH dengelenmediği sürece kalp kası hücrelerine anormal bir eğilim oluşmasına yol açtı. 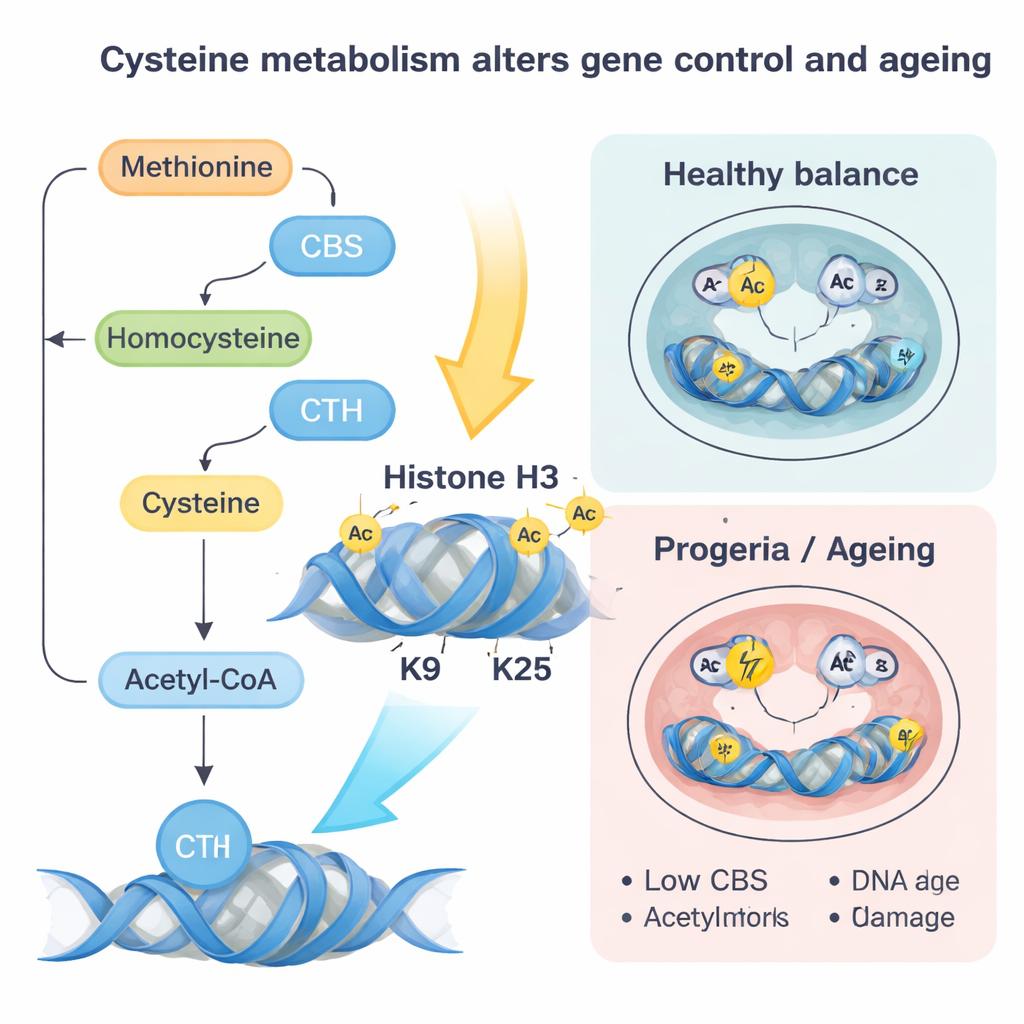
Metabolizma, DNA İşaretleri ve Erken Yaşlanma
Progeria‑benzeri lamin mutasyonu tamamlayıcı bir hikâye anlattı. Burada CBS ve CTH düzeyleri düşer, bu rota üzerinden sistein akışı ve asetil‑CoA azalır. Aynı zamanda homosistein metiyonin döngüsüne geri yönlendirilir ve SAM düzeyleri artar; SAM metil gruplarının evrensel bağışlayıcısıdır. Bu durum özellikle kromatini sıkılaştıran ve bozulmuş DNA onarımıyla ilişkilendirilen SUV39H1 enzimi tarafından konulan H3K9me3 adı verilen ek metil etiketlerinin artmasına yol açar. Yazarlar, CBS’yi nazikçe yeniden sağlmanın veya metiyonini sınırlamanın SAM’i düşürdüğünü, bu baskılayıcı metil işaretlerini azalttığını, DNA onarımını iyileştirdiğini, oksidatif stres ve senesans belirteçlerini azalttığını ve kalp hücresi farklılaşmasını kısmen kurtardığını gösterdiler. Benzer CBS düşüşleri ve baskılayıcı işaret artışları, normal yaşlı fare kalplerinde ve yaşlı insanlardan ile progeria hastalarından alınan insan fibroblastlarında görüldü; bu da bu devrenin doğal yaşlanmada da işlediğini düşündürüyor.
Sağlık ve Yaşlanma İçin Anlamı
Uzman olmayan bir okuyucu için mesaj şudur: lamin A/C’den oluşan nükleer kabukla hücrenin yapısal çerçevesi ve metabolizması sıkı bir şekilde bağlantılıdır: nükleer kabuk bozulduğunda, sisteinin kullanım şekli değişir ve bu da DNA paketleme proteinleri üzerindeki kimyasal işaretleri yeniden yazar. Bu işaretler, kök hücrelerin vücudu inşa ederken hangi genlerin açılacağını belirler ve hücrelerin yaşam boyu hasarı ne kadar iyi onardığını etkiler. CBS ve CTH gibi enzimleri dikkatlice ayarlayarak veya metiyonin ve sistein gibi besin arzını düzenleyerek, lamin temelli hastalıklarda bu işaretlerin yanlış yazılmasını düzeltmek ve muhtemelen erken veya normal yaşlanmanın bazı yönlerini hafifletmek mümkün olabilir.
Atıf: Wang, Y., Shi, H., Wittig, J. et al. Lamin A/C-regulated cysteine catabolic flux modulates stem cell fate through epigenome reprogramming. Nat Metab 8, 431–453 (2026). https://doi.org/10.1038/s42255-025-01443-2
Anahtar kelimeler: kök hücreler, nükleer lamina, sistein metabolizması, epigenetik, yaşlanma